Highlights beim Nierenzellkarzinom
Erstlinientherapie beim metastasierten Nierenzellkarzinom
Stand vor ESMO 2012: Wie aus den kurz vor ESMO 2012 publizierten Guidelines zur Behandlung von Nierenkrebs hervorgeht (Abb. 1), gibt es für Patienten mit günstigem oder intermediärem MSKCC-Risiko (Motzer R et al., J Clin Oncol 2002) in der Erstlinie drei Therapieoptionen: Sunitinib oder Bevacizumab + Interferon oder Pazopanib.
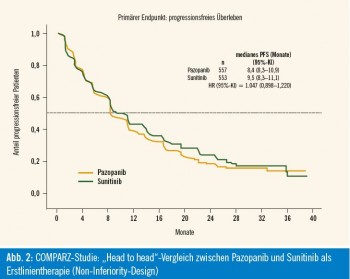
Neuigkeiten am ESMO 2012: Bei ESMO-Kongress 2012 wurde nun erstmals eine Vergleichsstudie zwischen Sunitinib und Pazopanib präsentiert, deren primärer Endpunkt das progressionsfreie Überleben (PFS) war. Die COMPARZ-Studie war als „Non-Inferiority“-Studie geplant, mit dem Ziel aufzuzeigen, dass Pazopanib in Bezug auf das PFS nicht schlechter als Sunitinib ist. (Non-Inferiority definiert als obere Grenze des 95%-KI eine Hazard Ratio < 1,25). Wie aus Abbildung 2 ersichtlich, war Pazopanib trotz numerischer Unterlegenheit beim PFS im Bezug auf den gewählten Endpunkt nicht schlechter als Sunitinib.
Die Ansprechraten waren bei Patienten im Pazopanibarm deutlich besser als im Sunitinibarm (31% versus 25%), interessant ist allerdings, dass dies nicht zu einer Verbesserung des PFS oder des Gesamtüberlebens führen konnte, was bislang in anderen RCC-Studien mit modernen Therapien fast immer beobachtet wurde. Ein möglicher Grund dafür ist eine Unterschätzung der Sunitinib-Ansprechraten in dieser Studie, was durch das für Sunitinib nachteilige Response-Assessment am Ende der Woche 6 (= Ende der 2. Pausewoche) zustande gekommen sein könnte: Es ist aus der Literatur bekannt, dass unter Sunitinib in der 2-wöchigen Pause ein Weiterwachsen des Tumors auftreten kann, was zwar für den Gesamtverlauf nicht relevant ist, aber bei Erfassung nach RECIST-Kriterien relevant werden kann.
Die Lebensqualität war unter Pazopanib deutlich besser als unter Sunitinib, auch hier wurde aber ein für Sunitinib nachteiliger Evaluierungszeitpunkt gewählt, nämlich das Ende der 4. Therapiewoche, in der die Nebenwirkungen naturgemäß am stärksten empfunden werden.
Zweitlinientherapie beim metastasierten Nierenzellkarzinom
Stand vor ESMO 2012: Wie aus Abbildung 3 ersichtlich, gab es vor ESMO 2012 zwei Therapieoptionen für die Zweitlinie: Everolimus oder Axitinib.
Neuigkeiten am ESMO 2012: An den Guidelines zur Zweitlinientherapie hat sich durch ESMO 2012 nichts Wesentliches verändert. Die Ergebnisse einer erstmals gezeigten Phase-III-Studie könnten jedoch dazu führen, dass das Konzept TKI gefolgt von TKI gegenüber TKI gefolgt von mTOR-Inhibitor bevorzugt wird. In dieser von Thomas Hutson präsentierten Studie (INTORSECT Trial, Hutson TE et al.) wurde nach Versagen einer Erstlinientherapie mit Sunitinib entweder mit dem intravenösen mTOR-Inhibitor Temsirolimus oder mit dem Tyrosinkinaseinhibitor Sorafenib behandelt. In Bezug auf das PFS gab es einen kleinen, statistisch nicht signifikanten numerischen Vorteil für Temsirolimus, in Bezug auf den zweiten Endpunkt, das Gesamtüberleben, gab es jedoch eine Überraschung: Das Gesamtüberleben war für Patienten im Sorafenib-Arm signifikant besser als im Temsirolimus-Arm (Abb. 4).
Eine weitere neue Information für die Zweitlinie war die Präsentation der Überlebensdaten aus der Phase-III-Studie mit Axitinib. In dieser im Lancet 2011 von Rini et al. publizierten Studie wurden Patienten, die in einer First-Line-Therapie versagt hatten (Sunitinib, Bevacizumab + Interferon, Temsirolimus oder Zytokine), entweder mit Axitinib oder Sorafenib behandelt. Aufgrund einer statistisch signifikanten Überlegenheit in Bezug auf das PFS im Vergleich zu Sorafenib wurde Axitinib als Zweitlinientherapie zugelassen (EMA, 3. September 2012). Einer der zweiten Endpunkte, das Gesamtüberleben, wurde nun am ESMO 2012 gezeigt: Es fand sich kein statistisch signifikanter Unterschied in Bezug auf das Gesamtüberleben zwischen Axitinib und Sorafenib, was der Autor unter anderem durch den möglichen Einfluss von Post-Studien-Therapien auf diesen Endpunkt erklärt.
Kombinationstherapie beim metastasierten Nierenzellkarzinom
Neuigkeiten am ESMO 2012: Die Vorstellung, durch Kombinationstherapien ein besseres Ergebnis zu erzielen, ist schon geraume Zeit ein Thema bei Patienten mit metastasiertem Nierenzellkarzinom. Kleine Phase-I-/-II-Studien haben hier für die Kombination von Anti-VEGF-Therapie mit mTOR-Inhibitor-Therapie sehr vielversprechende Ergebnisse geliefert und damit den Weg für randomisierte Phase-II- und Phase-III-Studien geebnet.
Wie aus Tabelle 1 ersichtlich, konnten in einer größeren Population die Ergebnisse dieser Phase-I-Studien nicht reproduziert werden: Die Kombination von Bevacizumab mit Temsirolimus oder Everolimus war nicht besser als mit IFN-alpha.
Prädiktion und Prognose beim metastasierten Nierenzellkarzinom
Neuigkeiten am ESMO 2012: Der Wunsch, durch prädiktive Marker die individuell beste Therapie zu wählen, wird schon lang gehegt und dementsprechend besonders intensiv beforscht.
Potenzielle prädiktive Parameter, welche allerdings noch im unabhängigen Setting validiert werden müssen, sind nach Untersuchungen von Motzer und Kollegen niedrige Angiopoietin-2- und hohe Metalloproteinase-2-Serumspiegel (Motzer R et al., Abstract 794). Diese korrelierten mit kompletter oder partieller Remission bei Patienten unter Sunitinib im „4 Wochen Therapie, 2 Wochen Pause“-Schema. Eine immunhistochemisch nachgewiesene niedrige HIF-1α-Expression am Tumor korrelierte mit einem besseren PFS. Keine Korrelation fand der Autor für bestimmte Single-Nukleotid-Polymorphismen sowie VHL-Inaktivierungsmechanismen und dem Krankheitsverlauf.
In einer anderen Arbeit (Zurita-Saavedra, Abstract 791) wurde der Serum-Interleukin-6-Spiegel als prädiktiver Marker für das PFS bei Patienten unter Pazopanibtherapie identifiziert (ungünstig, wenn hoch). Diese Untersuchung erlaubt jedoch keine Rückschlüsse für die Auswahl der Therapie generell, da hohe Zytokinspiegel immer mit einem schlechteren Ausgang assoziiert sind; diese Ergebnisse könnten also genauso auf Sunitinibpatienten zutreffen. Weiters zeigte der Autor in einer multivariaten Analyse, dass zirkulierende Zytokine (Interleukin-6 und Interleukin-8) sowie Osteopontin bessere Prognosemarker sind als die etablierten, nämlich Zeit zwischen Primum und Metastasen, korrigiertes Kalzium, Neutrophilie, Thrombozytose und Anämie (Tab. 2).