Innovationen in der onkologischen Bildgebung

Die klinische Onkologie erwartet sich von der radiologischen Bildgebung – als Basis sowohl für die Auswahl moderner therapeutischer Methoden als auch für das Therapiemonitoring – detaillierte Informationen über Tumorlokalisation, Tumorgröße, Ausmaß der Metastasierung und Mitbeteiligung von kritischen anatomischen Strukturen, typischerweise der Blutgefäße und der Nachbargewebe bzw. -organe. Im klinischen Alltag werden die meisten Fragestellungen durch konventionelle „morphologische“ Bildgebungstechniken wie Ultraschall (US), Computertomographie (CT) oder Magnetresonanztomographie (MRT) beantwortet. Diese Bildgebungstechniken haben im Laufe der letzten Jahre eine rasante Entwicklung durchgemacht. Wesentliche Verbesserungen betreffen beispielsweise die räumliche Auflösung der Bilder, wodurch immer kleinere Strukturen sichtbar gemacht werden können, sowie den Bildkontrast, welcher eine bessere Unterscheidung einerseits zwischen unterschiedlichen Gewebetypen und Organen, andererseits zwischen neoplastischem Gewebe und umgebendem gesunden Gewebe ermöglicht. Zu diesem verbesserten Kontrast tragen nicht zuletzt neue Kontrastmittel bei – exemplarisch sei hier die Gruppe der leberspezifischen Kontrastmittel in der MR-Bildgebung erwähnt – welche sich je nach Substanz spezifisch in Hepatozyten (Gd-EOB DTPA) oder in Kupffer’schen Sternzellen (superparamagnetische Eisenoxid-Nanopartikel) anreichern und so die Identifikation von nicht lebereigenem Gewebe erleichtern.
Die erwähnten Verbesserungen von Bildauflösung und Bildkontrast bedeuten für den befundenden Arzt ein höheres Maß an Sicherheit hinsichtlich seiner Diagnosen. Patienten hingegen profitieren vor allem von den ebenfalls immer kürzen Bildakquisitions- und dadurch Untersuchungszeiten. Dies trifft insbesondere auf solche Patienten zu, welche unter Platzangst leiden und für die eine MRT-Untersuchung in einer geschlossenen „Röhre“ nur schwer zu tolerieren ist. Bei CT-Untersuchungen wird durch neue, so genannte „iterative“ Bildrekonstruktionstechniken eine Verringerung der Strahlendosis um bis zu 50 % erreicht, was vor allem für jüngere Patienten von großer Relevanz ist.
Funktionelle Bildgebung – multimodale Bildgebung
Doch selbst die höchste derzeit erreichbare räumliche Auflösung von CT und MRT und der beste Gewebekontrast erlauben keine Rückschlüsse auf die funktionellen Vorgänge auf zellulärer und molekularer Ebene, obwohl diese eine wichtige Rolle für die Beurteilung des Tumors, für die Wahl der Therapie und schließlich für die Prognose des Patienten spielen. Die bekanntesten funktionellen Bildgebungstechniken stammen zweifellos aus dem nuklearmedizinischen Bereich, wobei die klassische Szintigraphie zwischenzeitlich von den tomographischen Verfahren, vor allem der Positronenemissionstomographie (PET) und in geringerem Ausmaß auch der Einzelphotonenemissionstomographie (SPECT) weitgehend abgelöst wurde. Vor allem die PET hat im letzten Jahrzehnt rasant an Popularität gewonnen, nicht zuletzt durch die Entwicklung PET-spezifischer Tracer. Bei PET-„Tracern“ handelt es sich vereinfacht gesagt um die Kombination eines Radionuklids mit einer aktiven Trägersubstanz. Einige der derzeit verbreitetsten PET-Tracer sind
- 18F-FDG (Fluordesoxyglukose), welcher den Zuckerstoffwechsel in Geweben abbildet, der in den meisten malignen Tumoren erhöht ist. Vorteile sind die beinahe universale Einsetzbarkeit in der onkologischen Bildgebung und der hohe Kontrast zwischen Tumor und gesundem Gewebe, ein Nachteil die fehlende Spezifität für bestimmte Tumorarten.
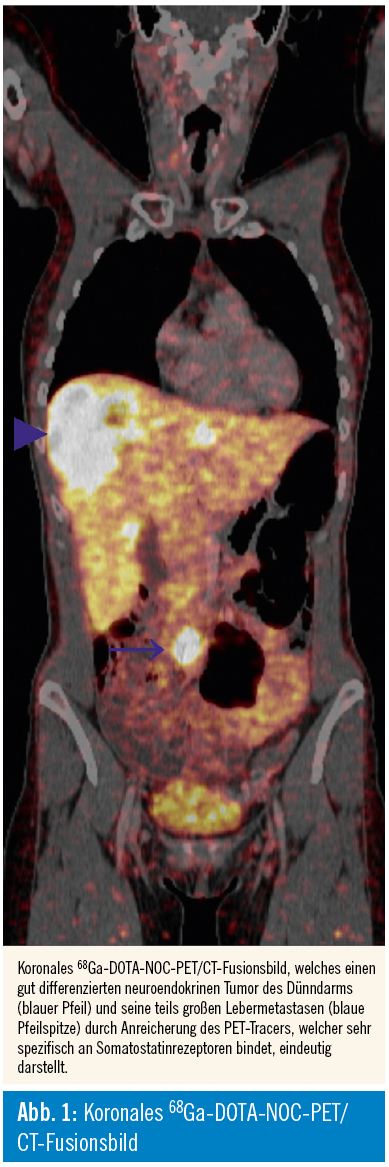
- 68Ga-DOTA-Peptide, z. B. DOTA-TOC, DOTA-NOC und DOTA-TATE, welche spezifisch an Somatostatinrezeptoren binden. Die Überexpression von Somatostatinrezeptoren ist ein Charakteristikum gut differenzierter neuroendokriner Tumoren, welche sich durch Verwendung eines Tracers dieser Gruppe direkt nachweisen lassen. Ein weiterer Vorteil besteht darin, dass die Anreicherung des Tracers auch gleichzeitig die Möglichkeit einer Radionuklidtherapie mit 177Lu-DOTA-TATE bedeutet.
- 18F-DOPA, welcher über die Dopamin-Vorstufe DOPA den Katecholaminstoffwechsel visualisiert und sich somit ebenfalls für die Erfassung neuroendokriner Tumore eignet, vor allem von Paragangliomen/Phäochromozytomen sowie von medullären Schilddrüsenkarzinomen.
- 11C-Cholin, welches zum Nachweis des Prostatakarzinoms (PCA) und seiner Metastasen eingesetzt wird. Spektroskopisch ist die Zunahme von Cholin gegenüber Kreatinin Kennzeichen der malignen Entartung und lässt auch eine Differenzierung von benigner Prostatahyperplasie und PCA zu. Cholin wird in Membran-Phospholipide eingebaut. Im direkten Vergleich von FDG- und Cholin-PET erweist sich Cholin aufgrund seiner fehlenden Ausscheidung mit dem Urin und seiner stärkeren Anreicherung in Läsionen als überlegen. Als Alternative kann auch 11C-Azetat eingesetzt werden. 11C-Azetat wird ebenfalls in den Lipidpool eingeschleust und akkumuliert damit ähnlich wie 11C-Cholin im PCA bzw. in Lymphknoten- und Fernmetastasen.
Unter multimodaler Bildgebung versteht man die Kombination von Informationen aus unterschiedlichen funktionellen und morphologischen Techniken, z. B. PET, MRT, optischer Bildgebung, Ultraschall und CT. Ziel der multimodalen Bildgebung ist die Erfassung einer Vielzahl von Parametern pathophysiologischer Vorgänge auf einem molekularen Niveau. Morphologische und funktionelle Einschränkungen der einzelnen Modalitäten treten dabei in den Hintergrund, die Stärken der einzelnen Techniken hingegen in den Vordergrund, sodass Synergieeffekte entstehen. Ihren aktuellen Höhepunkt hat die multimodale Bildgebung durch die Entwicklung von sogenannten „Hybridgeräten“ erreicht.
Hybridbildgebung: PET/CT und MR/PET
Die Entwicklung von Hybridtechniken eröffnet eine Vielzahl von Möglichkeiten sowohl im Rahmen der klinischen als auch präklinischen Bildgebung. Die derzeit am weitesten verbreitete Technik ist die Kombination von PET und CT in Form eines PET/CT-Kombinationsgerätes. Die PET-Bildakquisition und CT-Bildakquisition erfolgen zwar nacheinander, dies stellt allerdings aufgrund der kurzen Dauer des CT-Teils kein zeitliches Problem dar. Zwar bietet die Verwendung von jodhaltigem Kontrastmittel im Rahmen des PET/CT diagnostische Vorteile, vor allem hinsichtlich der Verifikation kleiner, nur schwach Tracer aufnehmender Herdläsionen, doch dient die CT in erster Linie der anatomischen Zuordnung der fokalen Tracer-Akkumulationen des PET, und aus diesem Grund wird in vielen Zentren die PET/CT-Untersuchung ohne Kontrastmittelapplikation („nativ“) durchgeführt.
Anders verhält sich dies bei einer weiteren Hybridtechnik, welche gerade Einzug in die klinische Routine hält: der MR/PET. Die erste Generation klinischer Geräte umfasst sowohl Geräte mit sequenzieller Technik (MRT und PET aufeinanderfolgend) als auch echte und damit zeitökonomische Simultangeräte. Verglichen mit CT-Bildern zeigen MR-Bilder durch unterschiedliche Gewichtungen und Pulssequenzen einen deutlich besseren Weichteilkontrast, auch ohne Verwendung von Kontrastmittel. Wenngleich derzeit noch wenige Studien zu dieser Thematik existieren, kann davon ausgegangen werden, dass die MR/PET der PET/CT zur anatomischen Lokalisation und Verifikation von Läsionen in den meisten Fällen überlegen sein wird. Zudem bietet die MRT selbst – ähnlich wie die PET, jedoch auf technisch anderem Wege und mit anderen Resultaten – die Möglichkeit, neben der makroskopischen Anatomie auch Informationen über Prozesse auf molekularer Ebene zu erhalten. So kann beispielsweise das Diffusionsverhalten von Wassermolekülen gemessen werden, was Rückschlüsse auf die Intaktheit der Zellmembranen und die Zelldichte zulässt. Auch kann die MRT durch Nutzung leicht unterschiedlicher Resonanzfrequenzen die Konzentration verschiedener Stoffwechselzwischenprodukte messen, um genauere Informationen über die biochemischen Prozesse in Geweben zu erhalten (MR-Spektroskopie). Auf diese Weise kann Information über das Ausmaß der Zellproliferation (Cholin), über den Energiestoffwechsel (Kreatin) und über Hypoxie und Nekrose (Laktat) von Tumoren gewonnen werden. Ferner ermöglicht die MR-Technologie die Darstellung von Blutgefäßen (MR-Angiographie) und die Analyse des Blutflusses und der Durchblutung von Geweben mit und ohne Verwendung von Kontrastmitteln (MR-Perfusion).
Aus obigen Ausführungen geht hervor, dass PET und MRT in vieler Hinsicht komplementär sind. Einerseits können Strukturalterationen im MRT durch PET besser charakterisiert werden, andererseits können Veränderungen von Tumoren in der PET erkannt werden, bevor sie im MRT zu Veränderungen der Morphologie führen. Da Änderungen auf molekularer Ebene vor Änderungen der Morphologie stattfinden, kann die Wirkung von Medikamenten oder Chemotherapeutika oft schon kurze Zeit nach Therapiebeginn evaluiert werden. Die ersten klinischen Erfahrungen mit MR/PETT deuten auf ein großes Potenzial dieser Bildgebungsmethode zur Verbesserung der nichtinvasiven Diagnostik und besseren Charakterisierung von Tumoren und ihres Verhaltens unter Therapie durch eine Kombination von PET- und MR-Parametern hin – besser als dies bisher mit PET bzw. PET/CT möglich war.
Bildbasierte Biomarker
Imaging-Biomarker sind Merkmale, die objektiv gemessen und analysiert werden und als Indikatoren für biologische und (patho-)physiologische Prozesse oder Ansprechen einer therapeutische Intervention gelten und demnach in der personalisierten Medizin vielfältige Anwendungen finden. Imaging-Biomarker erlauben frühzeitige Diagnosen, ein verbessertes Staging, eine individuelle Prognose und eine verbesserte Beurteilung des Behandlungsansprechens. Sie haben im Gegensatz zu Serum- oder Gewebebiomarkern den Vorteil, dass sie nichtinvasiv sind und wiederholt gemessen werden können. Imaging-Biomarker spielen daher eine bedeutende Rolle in allen Bereichen der Biomedizin von der Grundlagenforschung bis hin zur klinischen Anwendung.
Resümee
Die moderne onkologische Bildgebung eröffnet durch ihren multiparametrischen Ansatz zahlreiche Möglichkeiten nicht nur hinsichtlich der Detektion von Tumoren, sondern auch hinsichtlich der Beurteilung des Ansprechens der Tumoren auf eine Therapie. Daher stellt die bildgebende Diagnostik nicht nur ein unverzichtbares klinisches Werkzeug dar, sondern liefert auch eine stetig wachsende Anzahl an objektiven Parametern für die Erforschung und Evaluierung neuer onkologischer Therapieformen.