Nebenwirkungsmanagement bei Chemotherapie
Die Behandlung onkologischer Erkrankungen ist oft mit Komplikationen verbunden, die sich auf die Lebensqualität der Patienten auswirken können. Dass dadurch das Risiko eines Therapieabbruches erhöht wird und somit eine schlechtere Prognose bedeutet, konnte schon in den 1980er-Jahren nachgewiesen werden. Insgesamt variiert der Schweregrad der Nebenwirkungen häufig sehr individuell und hängt von der jeweiligen Zytostatikatherapie sowie von deren Dosierung und Applikationsweise ab. Dass geschlechtsspezifische Unterschiede nicht zu unterschätzen sind, konnte anhand neuerer Studien vor allem bei Nausea und Vomitus, wovon signifikant mehr Frauen betroffen sind, nachgewiesen werden. Aufgrund der Fortschritte im molekularen Targeting und der Nutzung der Pharmakogenomik und Pharmakogenetik können im Rahmen von Chemotherapien, Hormon- und zielgerichteten Therapien Patienten identifiziert werden, die ein erhöhtes Risiko für Toxizität und eine erhöhte Wahrscheinlichkeit des Ansprechens haben.
Nausea und Vomitus
Durch Chemotherapie ausgelöste Übelkeit und Erbrechen werden als akut, verzögert und antizipatorisch klassifiziert, wobei diese Formen auf verschiedene Mechanismen zurückgehen. Während die akute Symptomatik durch Stimulierung 1.) der Chemotherapietriggerzone am Boden des 4. Ventrikels und 2.) durch Freisetzung von 5-HT aus chromaffinen Zellen im Gastrointestinaltrakt bedingt ist und während oder kurz nach Verabreichung der Chemotherapie auftritt, basiert 3.) die antizipatorische Übelkeit auf einer Konditionierung oder Erwartungshaltung nach früheren Therapien und nimmt mit der Dauer der Chemotherapie zu.
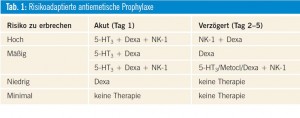
Auch durch die Karzinomerkrankung selbst, bei ausgeprägtem Leberbefall und zerebraler Metastasierung, können Übelkeit und Erbrechen auftreten. Das Ausmaß der therapiebedingten Symptomatik hängt stark von der Art der verwendeten Zytostatika und der Dosierung ab. Weitere Risikofaktoren sind spezielle Polymorphismen des Zytochroms P450, die für Variationen im Abbau der 5-HT3-Antagonisten verantwortlich sind sowie jüngeres Alter, weibliches Geschlecht, Erbrechen während der Schwangerschaft und vorhergegangener Chemotherapien und geringer Alkoholkonsum. Prophylaxe und Therapie der Übelkeit haben durch Einführung der 5-HT3-Antagonisten und des Neurokinin-1-Rezeptorantagonisten (NK-1-RA) Aprepitant große Fortschritte gemacht. Derzeit stehen vier 5-HT3-Antagonisten Ondansetron, Granisetron, Tropisetron, Dolasetron zur Verfügung. Palonosetron hat eine längere Halbwertszeit. Aprepitant penetriert ins ZNS, wirkt synergistisch mit 5-HT3-Antagonisten und ist bei hochemetogenen Substanzen wie Cisplatin oder Kombinationen indiziert. Benzodiazepine, besonders Lorazepam, verstärken die Wirksamkeit von Antiemetika und wirken durch die Sedierung besonders gegen antizipatorisches Erbrechen. Metoclopramid ist bei schwach emetogenen Substanzen indiziert (Tab. 1). Kortikoide haben ebenfalls eine antiemetische Wirkung und eignen sich als Monotherapie bei schwach emetogenen Therapien, besonders aber in Kombination mit 5-HT3-Antagonisten oder NK-1-Rezeptorantagonisten.
Diarrhö
Bei Karzinompatienten ist eine Diarrhö meist Ausdruck eines Schleimhautdefektes durch Zytostatika oder Radiotherapie, jedoch sollte eine umfassende Ursachenabklärung wie die bakteriologische und parasitologische Untersuchung des Stuhls, das Anlegen einer Kultur zwecks Toxinnachweis für Clostridium difficile sowie bei lang andauernder Immunsupression ein Zytomegalienachweis über PCR durchgeführt werden. Diarrhö tritt besonders unter Therapien mit Irinotecan, Capecitabin, den Tyrosinkinaseinhibitoren, Bortezomib oder nach Hochdosis-Chemotherapien auf. Die Symptome können von gering erhöhten Stuhlfrequenzen bis zu exzessivem Flüssigkeitsverlust, Hypokaliämie und septischen Zustandsbildern reichen. Als symptomatische Therapie sind 1.) Optifibre oder Benefiber als Stuhlregulantien und 2.) Loperamid und Diphenoxylat wirksam, da sie die Darmmotilität herabsetzen und die intestinale Kontraktilität verlangsamen. Bei infektiöser Ursache ist eine Darmmotilitätshemmung jedoch kontraindiziert. Alternativ oder additiv können Substanzen mit antisekretorischer Wirkung von Magensaft, Pepsin und gastrointestinalen Hormonen wie Somatostatin und Bismuth-Salizylate, aber auch Opiumtinkturen, verordnet werden. Symptomatisch sind Rehydrierung und Elektrolytsubstitution, je nach Labor, notwendig.
Obstipation
Eine Obstipation kann bei Karzinompatienten durch die Erkrankung oder häufiger durch die Therapie bedingt sein (Tab. 2). Therapeutisch sollte wenn möglich die Ursache angegangen werden. Dafür ist eine genaue Diagnose anhand physikalischer, bildgebender oder endoskopischer Untersuchungen Voraussetzung. Bei medikamentös verursachter Obstipation wie bei Opioiden ist das Absetzen meist nicht möglich, da eine ausreichende Analgesie gewährleistet sein muss. Daher sollen zeitgerecht Laxantien als Begleitmedikation, die über eine Steigerung der Osmose wirken, verordnet werden. Unterstützend wirken Prokinetika wie Gastrografin und Metoclopramid, die die Darmmotilität erhöhen. Gegen die morphininduzierte Obstipation steht als neuerer Therapieansatz die Blockade intestinaler Morphinrezeptoren durch hochaffine Antagonisten wie Methylnaltrexon oder Naloxon zur Verfügung. Als Allgemeinmaßnahmen sind adäquate Hydration, Zufuhr von Ballaststoffen und körperliche Aktivität zu empfehlen.
Mukositis
Die durch Chemo- und Radiotherapie bedingte Schleimhautschädigung verursacht Ulzerationen und Infektionen oder führt zur Reaktivierung von Herpes-Infektionen. Häufigkeit, Lokalisation und Intensität hängen von Art und Dosis der Therapie ab. Bei schweren Verläufen können Schluckunfähigkeit und starke Schmerzen bestehen. Eine orale Hygiene soll die Bakterienbelastung im Mund niedrig halten. Prophylaktische antibakterielle und antimykotische Mundspülungen können das Risiko systemischer Infektionen verringern (Tab. 3). Symptomatisch muss eine lokale und systemische Schmerztherapie erfolgen. Bei hohem Risiko für das Auftreten einer Mukositis bei Hochdosistherapien oder konkomitanter Radio- und Chemotherapie im HNO-Bereich ist der Einsatz von Palifermin, ein Keratinozytenwachstumsfaktor, der regenerierend auf die Schleimhaut wirkt, zugelassen.
Neutropenische Infektionen
Das Risiko für das Auftreten einer Neutropenie hängt von verschiedenen Faktoren ab (Tab. 4). Patienten mit mehreren Risikofaktoren sollten eine primäre Prophylaxe mit G-CSF (Granulocyte Colonystimulating Factor) erhalten. Filgrastim und Lenograstim müssen täglich injiziert werden, Pegfilgrastim kann auf Grund der längeren Halbwertszeit 1-mal pro Chemotherapiezyklus verabreicht werden. Eine sekundäre Prophylaxe mit Wachstumsfaktoren wird bei Patienten empfohlen, die bereits eine schwere febrile Neutropenie unter Chemotherapie hatten. Für den Benefit eines Einsatzes von G-CSF bei bereits bestehender febriler Neutropenie besteht nur wenig Evidenz. Sie sollte auf Patienten mit hohem Risiko beschränkt bleiben. Bei Verdacht auf eine Infektion muss eine genaue klinische Inspektion des Patienten erfolgen. An Laboruntersuchungen sind komplettes Blutbild, Laborchemie und Blutkulturen abzunehmen. Bildgebende Verfahren sowie Bronchiallavagen, Punktionen und Gewebeproben können notwendig werden. Bei akutem neutropenischem Fieber muss sofort nach Abnahme der Blutkulturen eine empirische Breitspektrum-Antibiose begonnen werden. Patienten mit einem niedrigen Risiko können eine orale Therapie erhalten. Die Wirksamkeit der Therapie muss überprüft werden. Wenn das Fieber auch nach 3-tägiger Therapie anhält, sollte eine neue Bestandsaufnahme gemacht und die Behandlung angepasst werden. Bei Patienten mit sehr hohem Infektionsrisiko auf Grund des Alters oder der Komorbiditäten sollten eine antibiotische Prophylaxe erhalten. Dadurch kann die Häufigkeit febriler Episoden und die Hospitalisierungen um 3050% gesenkt werden. Ebenso kann eine Herpesprophylaxe für Patienten mit einem hohen Infektionsoder Reexazerbationsrisiko indiziert sein.
Anämie
Je nach Art und Dosis der Chemotherapie, Grunderkrankung und Komorbiditäten beträgt die Inzidenz der Anämie bis zu 80%. Bei etwa 40% der Karzinompatienten beträgt der Hb-Wert < 12 g/dl. Bei Patienten, die eine rasche Substitution benötigen oder auf Erythropoetine nicht ansprechen, sind Transfusionen notwendig. Mögliche Nachteile sind kurzer Effekt, akute und späte Transfusionsreaktionen, Infektionen, Eisen- und Volumsüberladung. Bei immunsupprimierten Patienten müssen die Blutkonserven bestrahlt werden, um eine Graft-versus-Host-Reaktion hintanzuhalten. Für die Mehrheit der Patienten stehen Erythropoetine sowie Darbopoetine und deren Biosimilars zur Verfügung. Die Indikation zur Behandlung ist nach den ASCOGuide lines ein Hb 12 g/dl. Falls nach 4 Wochen Therapie kein Hb-Anstieg um 1 g/dl zu verzeichnen ist, soll eine Dosiserhöhung um 50% erfolgen, was bei 1012% ein zusätzliches Ansprechen bewirken kann. Ist das nicht der Fall, soll die Therapie abgesetzt werden.
Hand-Fuß-Syndrom
Das Hand-Fuß-Syndrom (die palmarplantare Erythrodysästhesie) ist eine schmerzhafte Rötung und Schwellung der Hand- und Fußflächen bis zur Hautablösung in Kombination mit Kribbeln und Taubheitsgefühl. Die Pathogenese ist unbekannt. Hervorgerufen wird es bevorzugt von Capecitabin, pegyliertes liposomales Doxorubicin und die VEGF-Tyrosinkinasehemmer Sunitinib und Sorafenib. Die Behandlung stützt sich auf symptomatische Maßnahmen. Patienten mit einem Dihydropyrimidin-Dehydrogenase- Mangel (DPD-Mangel) haben ein dramatisch erhöhtes Risiko, eine fatale Toxizität unter Fluorouracilen oder deren Prodrugs zu erleiden. Ebenso ist unter einer Fluorouraciltherapie und verwandten Substanzen eine antivirale Therapie mit Brivudin kontraindiziert, da es darunter zu einer Blockade des DPD kommt.
Neurotoxizität
Neuropathische Schmerzen können vor allem durch Taxane, Vincaalkaloide und Oxaliplatin zu einer Einschränkung der sensorischen Funktionen führen und sind durch schmerzhafte Parästhesien charakterisiert. Nicht selten wird durch diese unerwünschte Begleiterscheinung eine Weiterführung der Therapie begrenzt. Die Kombinationstherapie aus Kalzium- und Magnesiumsalzen zur Prophylaxe der oxaliplatininduzierten akuten sensorischen Neuropathie zeigt, dass oft in einfachen Mitteln eine effektive Option bestehen kann. Gegen die taxaninduzierte schmerzhafte Polyneuropathie wirkt eine Kombination aus Gabapentin und Opioiden, eventuell in Kombination mit dem Antidepressivum Venlafaxin.
FACT-BOX
Eine adäquate supportive Therapie ist in der Lage, die Lebensqualität der Patienten unter Chemotherapie wesentlich zu verbessern. In Zukunft wird dies durch den Einsatz von Pharmokogenomik und Pharmakogenetik noch weiter verbessert und die Therapie noch individueller gestaltet werden können.