Neue klinische Studiendirektive der Europäischen Kommission
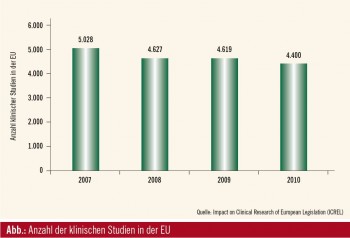
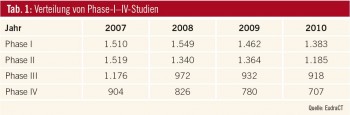
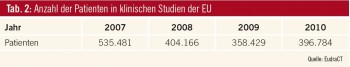
Die Europäische Kommission hat derzeit ein Papier in Begutachtung, mit dem das Durchführen klinischer Studien in Zukunft leichter werden soll. Es soll damit die „Clinical Trials Directive“ aus dem Jahr 2001 ersetzt werden, die mit „Standard Operating Procedures“ vor allem die Verlässlichkeit der Daten und die Patientensicherheit im Auge hatte. Ein überbordender bürokratischer Aufwand hat in Folge aber dazu geführt, dass in den Jahren 2007–2011 ein Rückgang klinischer Studien um 25 % verzeichnet wurde: Wurden im Jahr 2007 noch 5.000 Studien angemeldet, waren es im Jahr 2011 nur mehr 3.800 (Abb., Tab. 1, Tab. 2).
Generell hat sich der Aufwand für klinische Studien durch die EU-Regularien aus dem Jahr 2001 mit einem Plus von 107 % verdoppelt: Beispielsweise sind mit dem zunehmenden Dokumentationsaufwand auch die Personalkosten markant gestiegen. Die Zeit bis zur behördlichen Genehmigung einer Studie hat sich von 70 auf 150 Tage verlängert: Dieses Verfahren soll nunmehr durch ein harmonisiertes Genehmigungsdossier, das für alle EU-Länder gleich ist, flexibler und schneller werden. In der neuen Direktive liegt ein Schwerpunkt auf „nichtinterventionellen“ akademischen Studien. Studien mit Substanzen, die bereits zugelassen sind, sollen – ähnlich wie in den USA und Japan – von strengen Auflagen für Zulassungsstudien ausgenommen werden. Hürden für „nichtkommerzielle“ Sponsoren (Universitäten, akademische Institute, Stiftungen) sollen fallen.
EU-weit werden jährlich mehr als 20 Milliarden Euro in klinische Forschung investiert. Mit dem neuen Vorstoß sollen 800 Millionen Euro jährlich an unnötigen oder redundanten Behördenkosten gespart werden. Was im Detail dahintersteckt, haben wir bei Univ.-Prof. Dr. Günther Gastl als Präsident der ÖGHO nachgefragt.
Situation in Österreich: Der EU-weite Kontext großer Multicenterstudien kann natürlich nicht darüber hinwegtäuschen, dass klinische Studien in Österreich mit minimalsten Fördermitteln der öffentlichen Hand betrieben werden und nahezu ausschließlich oder überhaupt allein auf das Engagement einzelner Führungspersönlichkeiten zurückgehen, die den Spitzenplatz Österreichs im Bereich der Onkologie durch Selbstausbeutung behaupten. Univ.-Prof. Dr. Christoph Zielinski spricht in diesem Zusammenhang von einer außerordentlichen Bringschuld des Wissenschaftsressorts. Nur zum Vergleich: Das Institut Gustave Roussy, das größte onkologische Zentrum Europas, erhält derzeit eine Tranche von 50 Millionen Euro zur Errichtung eines Zentrums für personalisierte Medizin. Wer diesen Gedanken in Österreich mit innovativen Studien vorantreiben will, kann schon einmal an einigen 100.000 Euro scheitern, ein Betrag, der an sich schon nicht konkurrenzfähig ist. Wie man auf diese Weise im onkologischen Kernthema schlechthin klinische Forschung leisten soll, sei dahingestellt. Es ist aber auch nicht zu übersehen, dass sich eine Negativspirale in letzter Konsequenz bis zum Patienten zieht, und – wie Professor Zielinski in solchen Momenten gerne betont – 300.000 an Krebs erkrankte Menschen in Österreich sind eine wahlentscheidende Gruppe.