Prädiktive Faktoren beim Bronchialkarzinom
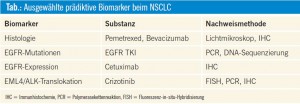
Die maßgeschneiderte Therapie mit Hilfe von prädiktiven Biomarkern zählt zu den vielversprechendsten Strategien, um die Prognose von Patienten mit nichtkleinzelligen Bronchialkarzinomen (NSCLC) weiter zu verbessern. Der Einsatz von klinischen Parametern oder molekularen Tests zur Unterscheidung von Respondern und Non-Respondern führt zu höheren Ansprechraten, reduziert die behandlungsassoziierte Toxizität und verbessert auch die Kosteneffizienz. In der Tabelle sind prädiktive Faktoren zusammengefasst, die entweder bereits heute im klinischen Alltag eingesetzt werden oder kurz vor einer routinemäßigen Anwendung stehen.
Tumorhistologie
Die Histologie entpuppte sich als ein wichtiger prädiktiver Faktor. Diese Tatsache basiert auf den Ergebnissen einer Phase-III-Studie, in der die Wirksamkeit von Cisplatin/Gemcitabin mit Cisplatin/Pemetrexed bei Patienten mit fortgeschrittenem NSCLC verglichen wurde (Scagliotti, J Clin Oncol 2008). Bei Patienten mit nichtsquamöser Histologie führte Cisplatin/Pemetrexed verglichen mit Cisplatin/Gemcitabin zu einem längeren Gesamtüberleben, während bei Patienten mit Plattenepithelkarzinomen eine Behandlung mit Cisplatin/Gemcitabin im Vergleich zu Cisplatin/Pemetrexed zu einer längeren Überlebenszeit führte. Ähnliche Resultate wurden auch bei einer Phase-III-Studie zur Pemetrexed-Erhaltungstherapie beim fortgeschrittenen NSCLC erzielt (Ciuleanu, Lancet 2009).
Eine antiangiogentische Therapie mit Bevacizumab wird mittlerweile in der täglichen klinisch-onkologischen Praxis beim NSCLC eingesetzt. Im Rahmen einer randomisierten Phase-II-Studie konnte jedoch ein substanzielles Risiko für schwere Blutungen unter einer Bevacizumab-Therapie nachgewiesen werden (Johnson, J Clin Oncol 2004). In Folge wurden Patienten mit Plattenepithelkarzinomen und Hämoptysen von der Teilnahme an den weiteren Phase-III-Studien ausgeschlossen, und auch die Zulassung für Bevacizumab wurde auf NSCLC-Patienten ohne diese Risikofaktoren beschränkt.
Basierend auf diesen Ergebnissen sollten daher NSCLC-Patienten mit Plattenepithelkarzinomen nicht mit Pemetrexed und/oder Bevacizumab behandelt werden.
EGFR-Mutationen
Mutationen in der Tyrosinkinase-Domäne des epidermalen Wachstumsfaktor-Rezeptors („epidermal growth factor receptor“, EGFR) treten bei etwa 10 % kaukasischer NSCLC-Patienten auf.
Deletionen im Exon 19 und die L858R-Punktmutation im Exon 21 sind die am häufigsten beobachteten Mutationen (85–90 % aller EGFR-Mutationen). Beim metastasierten NSCLC sind diese aktivierenden EGFR-Mutationen mit einer hohen Ansprechrate auf EGFR-Tyrosinkinaseinhibitoren (Erlotinib, Gefitinib) und einem verlängerten progressionsfreien Überleben assoziiert (Mok, N Engl J Med 2009; Mitsudomi, Lancet Oncol 2010; Maemondo, N Engl J Med 2010; Zhou, Lancet Oncol 2011; Rosell, Lancet Oncol 2012). Auf Grund dieser Resultate sind NSCLC-Patienten mit aktivierenden EGFR-Mutationen Kandidaten für eine Therapie mit EGFR-Tyrosinkinaseinhibitoren.
EGFR-Expression
In der FLEX-Studie konnte gezeigt werden, dass die Zugabe von Cetuximab zu einer platinhältigen Chemotherapie das Gesamtüberleben von Patienten mit fortgeschrittenem NSCLC verlängert (Pirker, Lancet 2009). Nachfolgende Untersuchungen von Biomarkern im Rahmen der FLEX-Studie zeigten, dass vor allem Patienten mit einer hohen EGFR-Expression (immunhistochemisch bestimmt) von der Zugabe von Cetuximab zur Chemotherapie profitieren (Pirker, Lancet Oncol 2012).
EML4-ALK-Translokation
In etwa 3–5 % der Adenokarzinome der Lunge führt eine Inversion im Chromosom 2p zu einem Fusionsgen (EML4-ALK-Fusion) bestehend aus Teilen des „Anaplastic lymphoma kinase“-Gens (ALK-Gens) und des „Echinoderm microtubule-associated protein-like 4“ Gens (EML4-Gens; Soda, Nature 2007). Diese ALK-Aberrationen können mittels Fluoreszenz-in-situ-Hybridisierung (FISH), PCR oder immunhistochemisch nachgewiesen werden. Welche dieser Methoden die optimale Nachweismethode ist, wird derzeit noch ermittelt. NSCLC-Patienten mit ALK-Veränderungen sprechen exzellent auf eine Behandlung mit dem ALK-Tyrosinkinaseinhibitor Crizotinib an (Kwak, N Engl J Med 2010). In einer retrospektiven Analyse konnte gezeigt werden, dass eine Therapie mit Crizotinib bei Patienten mit fortgeschrittenem, ALK-positivem NSCLC zu einer signifikanten Verlängerung der Gesamtüberlebenszeit führt (Shaw, Lancet Oncol 2011). Auf Grund der außergewöhnlichen Ergebnisse hat die US-Behörde FDA Crizotinib zur Therapie von Patienten mit lokal fortgeschrittenem oder bereits metastasiertem NSCLC zugelassen. Voraussetzung für den Einsatz von Crizotinib ist der Nachweis des ALK-Fusionsgens im Tumor. Die Zulassung für Crizotinib wurde unter anderem auch in Europa beantragt. Zusätzlich werden die Sicherheit und Anti-Tumor Aktivität von Crizotinib im Vergleich zur Standardchemotherapie derzeit in einer Phase-III-Studie untersucht (ClinicalTrials.gov: NCT00932893).
Fazit
Die maßgeschneiderte Therapie mit Hilfe von prädiktiven Biomarkern ist ein wesentlicher Schritt zu einer verbesserten Behandlung von Patienten mit NSCLC. In den letzten Jahren konnten einige Faktoren identifiziert werden, die das Ansprechen auf bestimmte Therapien vorhersagen können. Die Analyse von Biomarkern auf RNA-, DNA- oder Proteinebene erlaubt bereits heute eine Selektion von NSCLC-Patienten für die effektivste Behandlung. Eine individuell angepasste Therapie hat mittlerweile Einzug in die tägliche klinisch-onkologische Praxis gehalten und wird zukünftig zu einer weiteren Verbesserung der Prognose von NSCLC-Patienten führen.