Was Pathologen über die Immuntherapie wissen sollten
Die Immuntherapie ist mehr als ein plötzlicher substanzieller Umsturz in der Betreuung auch von Patienten mit nichtkleinzelligem Lungenkarzinom (NSCLC)“, hielt Professor Dr. Paul Hofman, Krankenhaus Nizza und Universität von Nizza Sophia Antipolis, fest. „Klinische Studien zum NSCLC brachten großartige Ergebnisse“, sagte Hofman.1 „Wir werden in Zukunft überlegen müssen, ob wir diesen Patienten eine Immuntherapie oder eine Chemotherapie geben.“ Hofman gab im Rahmen der dritten gemeinsamen Jahrestagung der Schweizer und Österreichischen Gesellschaften für Pathologie in Wien* einen Überblick über die für Pathologen relevanten Aspekte dieser therapeutischen Revolution.
Mit dem Anti-CTLA4-Antikörper Ipilimumab und den PD-1-Hemmern Nivolumab und Pembrolizumab haben derzeit drei Immuntherapeutika eine Zulassung der European Medicines Agency (EMA). Der PD-L1-Antikörper Atezolizumab ist in den USA zugelassen, und weitere Immuntherapien sind in Entwicklung.
Gegen PD-1 und PD-L1 gerichtete Immuntherapien verhindern die Interaktion zwischen PD-1 und PD-L. Eine Bindung von PD-1 an PD-L1 unterdrückt den zytotoxischen Effekt der T-Zellen. Hier setzen PD-1-Hemmer und PD-L-1-Hemmer an und stellen die Antitumorwirkung der T-Zellen wieder her. In diesen Prozess sind, wie Hofman ausführte, zahlreiche weitere Faktoren, wie PD-L2, dendritische Zellen, OX40 oder Lag3 involviert.
PD-L1-Immunhistochemie (IHC): Status quo und Herausforderungen
PD-L1 ist derzeit der einzige klinisch relevante Biomarker für die Immuntherapie, er ist allerdings kein sehr robuster Prädiktor für das Ansprechen auf eine Immuntherapie. Für die Analyse der PD-L1-Expression werden aktuell folgende PD-L1-Klone angewendet: für Nivolumab 28-8 (Dako), für Pembrolizumab 22C3 (Dako), für Atezolizumab SP142 (Ventana) und für Durvalumab SP263 (Ventana). Nur SP142 bezieht sich auf infiltrierende Tumorzellen, die anderen auf die Tumorzellmembran.
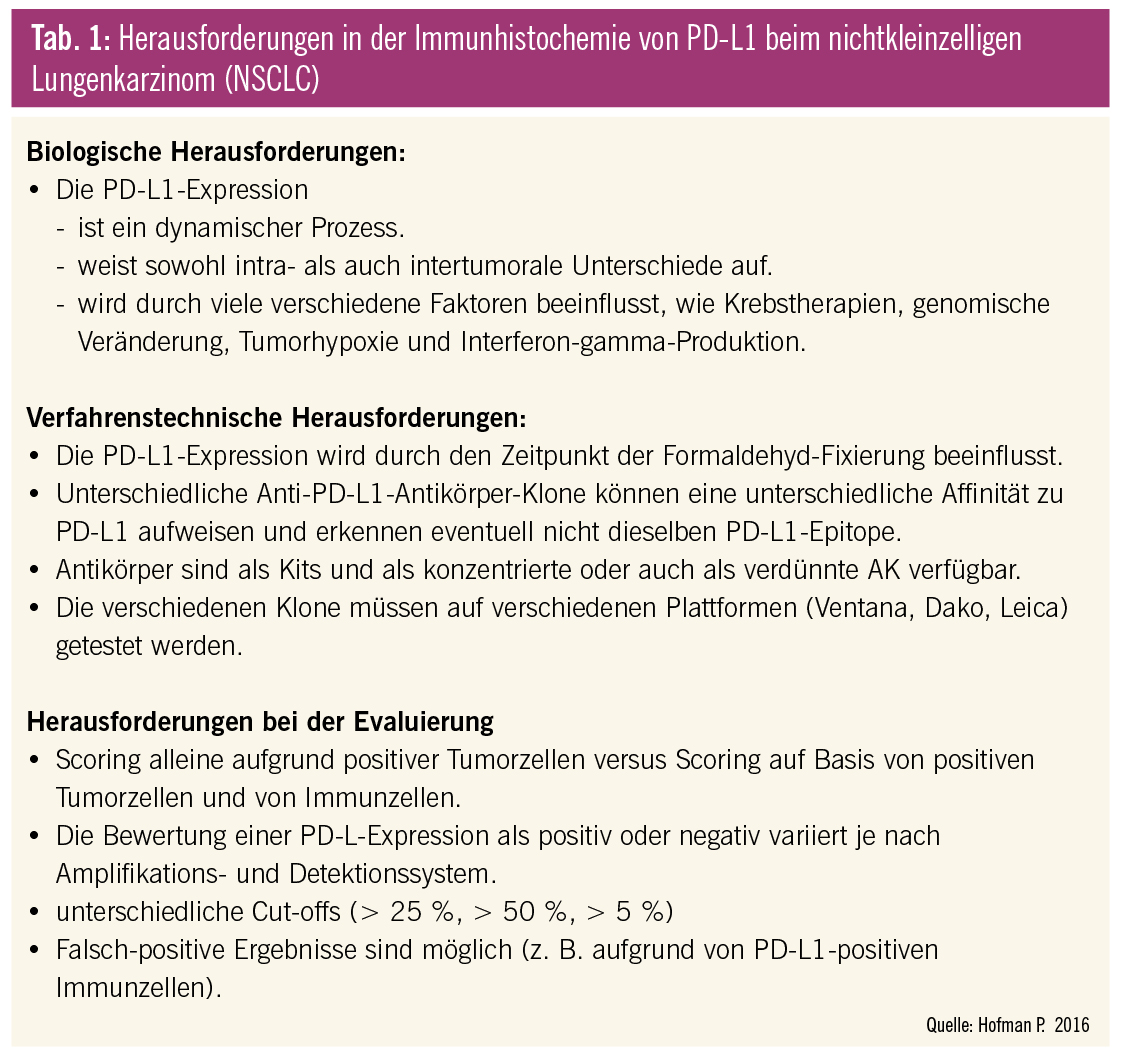
Aktuell sieht man sich zahlreichen Herausforderungen auf biologischer und verfahrenstechnischer Ebene und Problemen bei der Interpretation der ermittelten PD-L-Expression gegenüber (Tab. 1).
Wenn Biopsiestelle und Assay überdie Immuntherapie entscheidet
Die Biopsiestelle beeinflusst das Ergebnis wesentlich. Wie Hofman an einem Beispiel illustrierte, kann der Anteil PD-L1-positiver Tumorzellen in verschiedenen Biopsaten ein und desselben Tumors durchaus zwischen < 1 % und > 50 % liegen. Gezeigt wurde, dass der PD-L1-Status des Bronchialbiopsats sehr stark vom PD-L1-Status des Resektats desselben Tumors abweichen kann. Negativen Resultaten aus der Biopsie können positive Resultate aus dem Resektat gegenüberstehen.2 „Im ersten Fall würde der Patient fälschlicherweise keine Therapie mit Pembrolizumab erhalten“, erläuterte Hofman.
Hinzu kommt, dass je nach verwendetem Antikörper bzw. Assay die Anfärbung sehr variieren kann.3 Dies müsse bei der Auswahl des Cut-offs berücksichtigt werden, so Hofman. Er verwies darauf, dass auch das verwendete Testverfahren darüber entscheiden kann, ob ein Patient eine Immuntherapie erhält oder nicht. Ein Patient, bei dem bei Verwendung von 22C3 eine PD-L1-Expression < 50 % nachgewiesen wird, erhält keine Immuntherapie, durchaus aber bei Testung mit einem anderen Antikörper.
PD-L1-IHC-Diagnostik im Vergleich
Vergleiche der PD-L1-IHC-Diagnostik zeigen die Problematik der unterschiedlichen Testverfahren. Im Rahmen des Blueprint-Projekts von großen Pharmafirmen und Biotechnologieunternehmen brachten 22C3, 28-B und SP263 auf Tumorzellen dasselbe Ergebnis, während SP142 schlechter abschnitt. Bei der Immunzellfärbung war das Ergebnis aller vier Klone vergleichbar. Hofman verwies auf die Einschränkungen dieser Analyse: „Es wurden nur 39 Tumoren untersucht, die Korrelation mit dem therapeutischen Outcome fehlte, und die teilnehmenden Pathologen waren nicht trainiert worden.“
Eine große Untersuchung von AstraZeneca mit mehr als 500 Tumoren, die allerdings ohne SP142 durchgeführt wurde, bestätigt wie die German Ring Study 2016 die gute Korrelation der Färbe-Ergebnisse von 22C3, 28-8 und SP263.4, 5 Die German Ring Study ergab allerdings geringe Konkordanzraten beim IHC-Scoring.5 „Wir benötigen nun Studien, die die IHC-Ergebnisse mit dem klinischen Outcome einer Immuntherapie korrelieren, um zu sehen, welche Relevanz die Unterschiede haben“, sagte Hofman. In einer kleinen Untersuchung der Gruppe um Hofman brachte die Färbung der Tumor- und der Immunzellen mit SP142 und mit SP263 nicht dieselben prognostischen Ergebnisse.6
Erweitere Diagnostik für eine bessere Prädiktion
Hofman betonte die Notwendigkeit, die PD-L1-IHC und die CD8+-IHC zu kombinieren, um die prognostische Aussagekraft zu erhöhen.
Multiplex-Immunhistochemie: In Nizza arbeitet man an der Entwicklung von Multiplex-IHC-Assays, mit denen unter anderem die PD-L1/CD8+-Ratio bestimmt werden kann. Als nächster Schritt soll die Software zur Quantifizierung verbessert werden.
Multiparametrisches Profiling: Die PD-L1-Expression ist mit zahlreichen weiteren Faktoren assoziiert, die durch multiparametrisches Profiling erfasst werden sollen. Derzeit werden Parameter wie Raucherstatus, PD-L1-IHC, Onkogene, der histologische Subtyp und verschiedene Zelllinien integriert analysiert.
„Liquid Microenvironment“: Vergleichsweise neu ist auch das Konzept des „Liquid Microenvironment“. Es basiert auf der Erkenntnis, dass zirkulierende Tumorzellen mit Blutplättchen, myeloischen Zellen und mit Lymphozyten interagieren.
Derzeit wird die Korrelation zwischen der PD-L1-Expression auf zirkulierenden Tumorzellen und den Tumorzellen im Gewebe untersucht.
Offene Fragen
Hofman verwies auf zahlreiche offene Fragen rund um die PD-L1-IHC (Tab. 2) und präsentierte Lösungsansätze, um Fehler bei der Bestimmung zu minimieren (Tab. 3). Er hob abschließend hervor: „Wir brauchen internationale IHC-Guidelines für die Bestimmung und Evaluierung der PD-L1-Expression. Zur Qualitätsverbesserung könnte die Bestimmung der PD-L1-Expression in zertifizierten Pathologielaboren beitragen. Und wir müssen über die PD-L1-Expression hinaus weiter Faktoren in unsere Analyse einbeziehen, um die Prädiktion zu verbessern, so zumindest PD-L2, PD1 und CD8.“


6 Illie M et al., Mod Pathol 2016 Aug 26, DOI: 10.1038/modpathol.2016.149