Die Bedeutung von Kognition und Emotion für die Entstigmatisierung schizophrener Patienten
Kognitive Störungen sind bei der Schizophrenie ein kennzeichnendes Merkmal der Erkrankung und haben Einfluss auf den Krankheitsverlauf, auf die Adhärenz und die psychosozialen Funktionen. Hierbei handelt es sich vor allem um Störungen in den Bereichen der Aufmerksamkeit, des Arbeitsgedächtnisses, des verbalen Gedächtnisses, der Sprachflüssigkeit und der Exekutivfunktionen1, deren Bedeutung für die Rehabilitation und Reintegration der Patienten zunehmend erkannt wird.
Seit der Entwicklung der Neuroleptika lag der Schwerpunkt der Behandlung vor allem auf positiven und negativen Symptomen. Durch die Anwendung von klassischen Antipsychotika zeigten sich vor allem extrapyramidale Nebenwirkungen, die von vielen Patienten als sehr stigmatisierend erlebt wurden. Diese Behinderungen sind seit der Anwendung von atypischen Antipsychotika als rückläufig anzusehen. Heute stellen vor allem die Beeinträchtigungen der Patienten durch neurokognitive Einschränkungen eine Stigmatisierung dar, da diese Defizite vor allem im familiären, beruflichen und sozialen Umfeld zum Tragen kommen. Neue Forschungsergebnisse weisen zunehmend auf den Einfluss von kognitiven Störungen auf diese funktionalen Defizite hin.
Mit dem vermehrten Wissen über den Zusammenhang zwischen psychosozialen Funktionsstörungen und den dadurch verursachten psychosozialen Beeinträchtigungen der Erkrankung Schizophrenie und den damit verbundenen Einschränkungen im Alltagsleben2 hat die Frage der Stigmatisierung durch kognitive Dysfunktionen einen besonderen Stellenwert.
Neurokognition und Stigmatisierung
Nach E. Gofmann3 entsteht Stigmatisierung aus einer Zuschreibung von „virtueller“ sozialer Identität aufgrund von Abweichungen von erwartetem sozialem Verhalten oder Rollen. So können Beeinträchtigungen in kognitiven Fähigkeiten und emotionalem Erleben aufgrund von psychischen Erkrankungen ein Stigmatisierungsgrund sein. Die zugeschriebene Identität steht im Gegensatz zu der aktuellen Identität des Betroffenen und löst eine Beschädigung der sozialen Identität aus. Dadurch werden die Betroffenen von der sozialen Umwelt und dem eigenen Selbst isoliert.
Stigmatisierung ist also ein Vorgang, der nicht auf objektiven feststellbaren Eigenschaften basiert, sondern in einem Beziehungsverhältnis zwischen Patient und sozialer Umwelt entsteht. Aus Angaben über das Vorliegen einer psychischen Erkrankung wird auf das Vorliegen von bestimmten Eigenschaften geschlossen4. Diese sozialen Annahmen über psychische Erkrankungen werden im Rahmen der Sozialisation internalisiert. So können wahrgenommene Einschränkungen in kognitiven Funktionen zu einem Vorenthalten von sozialer Akzeptanz führen. Finzen5 betont: „Die sozialen Folgen der Stigmatisierung müssen als zweite Krankheit verstanden werden, die Folgen der Schuldzuweisung und die unmittelbaren Stigmatisierungsfolgen für die Angehörigen gleichsam als dritte.“
Der Umgang der Patienten mit ihrem stigmatisierten Status ist gekennzeichnet durch Vermeidungsverhalten, sozialen Rückzug und Beeinträchtigung des Selbstwertgefühls. Damit in Zusammenhang kommt es zu einer geringeren Lebensqualität und einer Reduktion sozialer Netzwerke. Eine Stigmatisierung psychisch kranker Menschen im Alltag hat soziale Folgen, trägt zu geringeren Chancen auf berufliche Anstellung bei und kann zu offener Diskriminierung durch Mitarbeiter von Behörden sowie sprachlicher Diskriminierung führen. Die Stigmaerfahrung kann zu einer gesteigerten Vulnerabilität führen und einen negativen Einfluss auf die Behandlung und den Krankheitsverlauf haben. Ursachen können eine geringere Bereitschaft zur Anerkennung der Diagnose, eine geringere Bereitschaft zur Behandlung und eine geringere Medikamentencompliance sein.
Überdauernde „trait marker“: Kognitive und emotionale Defizite sind als psychische Dysfunktionen bei Patienten mit Schizophrenie anzusehen, von denen bekannt ist, dass sie überdauernd vorhanden sind („trait marker“), auch zwischen den akuten Krankheitsphasen. Damit können sie als Eigenschaftsmerkmal in sozialen Situationen zu Diskriminierung und Stigmatisierung beitragen. Kognitive Störungen werden auch in besonderer Weise in sozialen Interaktionssituationen deutlich. Unter sozialer Kognition versteht man die Fähigkeit, mentale Zustände einer anderen Person wie Absichten, Wünsche oder Gefühlszustände wahrzunehmen. Ist diese basale soziale Kompetenz beeinträchtigt, werden Stigmatisierungen festgeschrieben.
Eine ausführliche Diagnose der kognitiven Störungen und eine individuelle auf die Beeinträchtigungen abgestimmte störungsorientierte Behandlung können auch zu einem Abbau der zusätzlichen psychischen Belastungen durch Stigmaerfahrungen beitragen.
So ist ein wesentliches Therapieziel in der Langzeitbehandlung von Patienten mit Schizophrenie neben einer zuverlässigen Rückfallprophylaxe auch die Erhaltung oder Wiedererlangung kognitiver Fähigkeiten6. Kognitive Störungen haben des Weiteren Relevanz für die Compliance, da sie die Therapiemotivation und das Engagement in einer therapeutischen Allianz reduzieren.
Diagnostik kognitiver Störungen
Zur Verbesserung der Diagnostik kognitiver Defizite und zur Entwicklung von neuen medikamentösen Therapieoptionen initiierte das US-amerikanische Nationale Institut für Seelische Gesundheit (NIMH) in einem internationalen Expertenkonsensus das MATRICS-Programm (Measurement and Treatment Research to Improve Cognition in Schizophrenia)7. Zeitgleich forderte die amerikanische Arzneimittelbehörde (Food and Drug Administration, FDA) für den Wirkungsnachweis einer Substanz nicht nur einen signifikanten Effekt auf kognitive Defizite, sondern auch eine Verbesserung der sozialen und beruflichen Funktionen.
Aktuelle neuropsychologische Testung kognitiver Funktionen
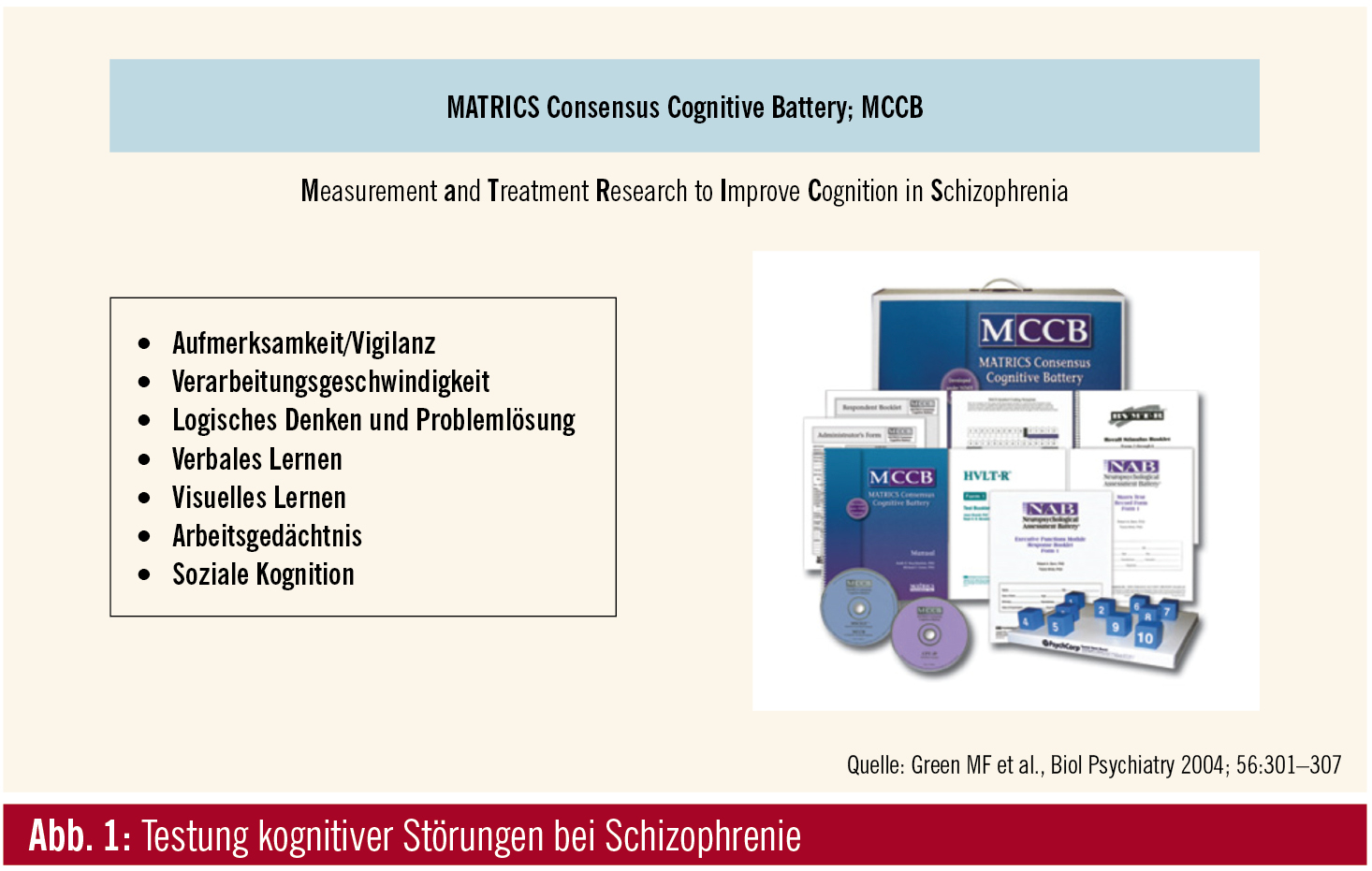
Die MATRICS-Consensus-Cognitive-Battery (MCCB) wurde im Rahmen des MATRICS-Projekts (Measurement and Treatment Research to Improve Cognition in Schizophrenia) des National Institute of Mental Health entwickelt. Diese Testbatterie ist ein Verfahren, das speziell für den Einsatz in klinischen Studien geeignet ist, da sie eine standardisierte Untersuchung neuer Medikamente zur Verbesserung der kognitiven Leistungsfähigkeit ermöglicht8 (Abb. 1).
Die MCCB dient einer relativ kurzen Überprüfung jener kognitiven Bereiche, die bei schizophrenen Personen häufig beeinträchtigt sind, und kann als Zielkriterium in klinischen Studien dienen, die sich mit der Überprüfung neuer Arzneimittel oder Aspekten von kognitiver Remediation befassen. Weiters stellt sie ein sensitives Instrument für die Erfassung von Veränderungen in der kognitiven Leistungsfähigkeit dar. Die MATRICS-Consensus-Cognitive-Testbatterie besteht aus 10 Untertests, die folgende 7 Bereiche der kognitiven Leistungsfähigkeit abdecken:
- Verarbeitungsgeschwindigkeit
- Aufmerksamkeit/Vigilanz
- Arbeitsgedächtnis
- verbales Lernen
- visuelles Lernen
- logisches Denken und Problemlösen
- soziale Kognitionen
Das „Screen for Cognitive Impairment in Psychiatry“ (SCIP)9 dient der Erfassung kognitiver Beeinträchtigungen, die in Zusammenhang mit psychotischen und affektiven Störungen auftreten. Ziel der Entwicklung des SCIP war es, ein kurzes, einfach vorzugebendes Instrument zu konstruieren, welches es ermöglicht, kognitive Defizite, die nicht ausschließlich im Rahmen einer demenziellen Erkrankung auftreten, zu erkennen. Da diese Beeinträchtigungen auch maßgeblichen Einfluss auf den Behandlungserfolg haben können, ist es von großem Vorteil, leichte Defizite bereits zu einem frühen Zeitpunkt in der Behandlung zu erkennen, sie im Rahmen einer umfassenden neuropsychologischen und physiologischen Untersuchung genauer abzuklären und in der vorgesehenen Behandlung zu berücksichtigen.
Mit dem SCIP können Funktionen des Arbeitsgedächtnisses, unmittelbares und verzögertes verbales Lernen, Wortflüssigkeit und psychomotorische Geschwindigkeit erfasst werden. Die Vorgabe ist unkompliziert. Es werden nur wenige Materialien (Testbogen, Stift und Stoppuhr) benötigt, was im stationären Umfeld und in der psychiatrischen Konsiliartätigkeit in Krankenhäusern auch eine Untersuchung am Bett des Patienten ermöglicht – sofern ausreichend Ruhe vorhanden ist. Nach einer kurzen Schulung kann das Verfahren von verschiedenen Berufsgruppen im Gesundheitswesen durchgeführt werden. Das „Screen for Cognitive Impairment in Psychiatry“ wurde ins Deutsche übersetzt und validiert.
Die „Brief Assessment of Cognition in Schizophrenia“ (BACS)10 stellt eine Testbatterie dar, die der Erfassung von kognitiven Leistungsfähigkeiten im Zusammenhang mit dem Störungsbild der Schizophrenie dient. Es werden folgende Bereiche erfasst:
- verbales Gedächtnis und verbales Lernen
- Arbeitsgedächtnis
- motorische Funktionen
- Aufmerksamkeit
- Informationsverarbeitungsgeschwindigkeit
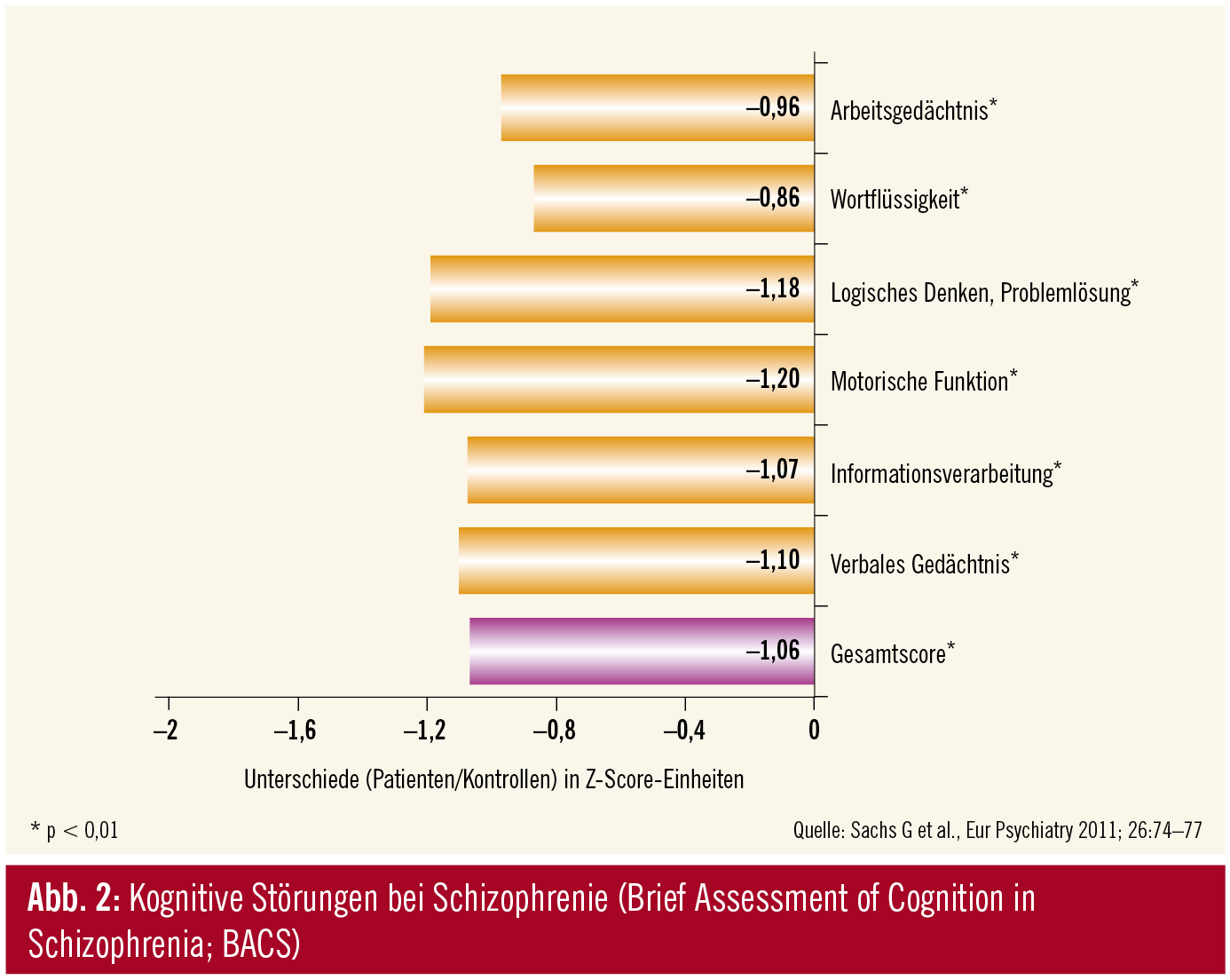
Die BACS wurde bisher sowohl in den USA als auch in Österreich, Japan und Frankreich an einer Stichprobe aus gesunden Kontrollpersonen und schizophrenen Patienten validiert. Die deutsche Validierung11 ergab, dass die BACS sehr gut zwischen Personen mit kognitiven Leistungsbeeinträchtigungen und solchen ohne Beeinträchtigung zu unterscheiden vermag (Abb. 2).
Medikamentöse Therapie kognitiver Störungen
Kognitive Störungen wurden häufig als Folge von Antipsychotikagabe angesehen, vor allem der Antipsychotika der 1. Generation. Durch die D2-Blockade im Striatum wurde eine negative Einflussnahme auf die Informationsverarbeitungsgeschwindigkeit und das prozedurale Lernen angenommen. Als weitere Einflussgrößen wurden extrapyramidale Nebenwirkungen, vor allem in den Bereichen, in denen motorischen Funktionen gefordert waren, und Anticholinergikagaben, die Gedächtnisfunktionen beeinträchtigen, angesehen. Die kognitiven Dysfunktionen und extrapyramidalen Nebenwirkungen sind Merkmale, die in sozialen Interaktionen zu Stigmatisierung im Sinne von negativen Zuschreibungen führen, dadurch besondere psychische Belastungen für die Patienten mit Schizophrenie auslösen und den Krankheitsverlauf beeinflussen können.
Effekte der Antipsychotika: Aufgrund des Stellenwertes der kognitiven Störungen für die psychosoziale Funktionsfähigkeit besteht ein großes Interesse, pharmakologische Behandlungen zur Therapie kognitiver Störungen zu finden. Die Anwendung atypischer Antipsychotika hat zu einer deutlichen Verbesserung der negativen und kognitiven Symptomatik sowie zur besseren Verträglichkeit, in erster Linie durch die Minderung der motorischen und affektiven Nebenwirkungen, geführt. Dadurch konnte auch ein wesentlicher Beitrag zur Entstigmatisierung geleistet werden. Kognitive Störungen scheinen ein „trait marker“ bei Patienten mit Schizophrenie zu sein. Einzelne Studien weisen auf einen möglichen positiven Effekt von atypischen Antipsychotika auf die Neurokognition und Affektregulierung hin.
Unter Berücksichtigung des Aspektes „Stigma“ zeigen die vorliegenden Vergleichsstudien, dass atypische Antipsychotika kognitive Defizite bei schizophrenen Störungen günstiger beeinflussen als klassische Antipsychotika. Einschränkend muss angeführt werden, dass in den meisten der Vergleichsstudien die Dosierungen der Vergleichssubstanz (meist Haloperidol) verhältnismäßig hoch gewählt wurde. Falls typische Antipsychotika niedriger dosiert wurden, gelangt ein Teil der Überlegenheit der atypischen Antipsychotika nicht mehr zur Darstellung.
Die Daten aus der EUFEST-Studie (European First Episode Schizophrenia Trial) konnten zeigen, dass sowohl atypische Antipsychotika (Amisulprid, Olanzapin, Quetiapin, Ziprasidon) als auch Haloperidol neurokognitive Defizite nach 6 Monaten signifikant besserten12. Die Effektstärken der Verbesserungen waren jedoch mäßig und es fanden sich keine signifikanten Unterschiede zwischen den einzelnen Behandlungsgruppen. In den Studien, in denen nur atypische Antipsychotika verglichen wurden, fanden sich insgesamt Verbesserungen in unterschiedlichen kognitiven Bereichen, jedoch keine signifikanten Unterschiede zwischen den einzelnen Substanzen.
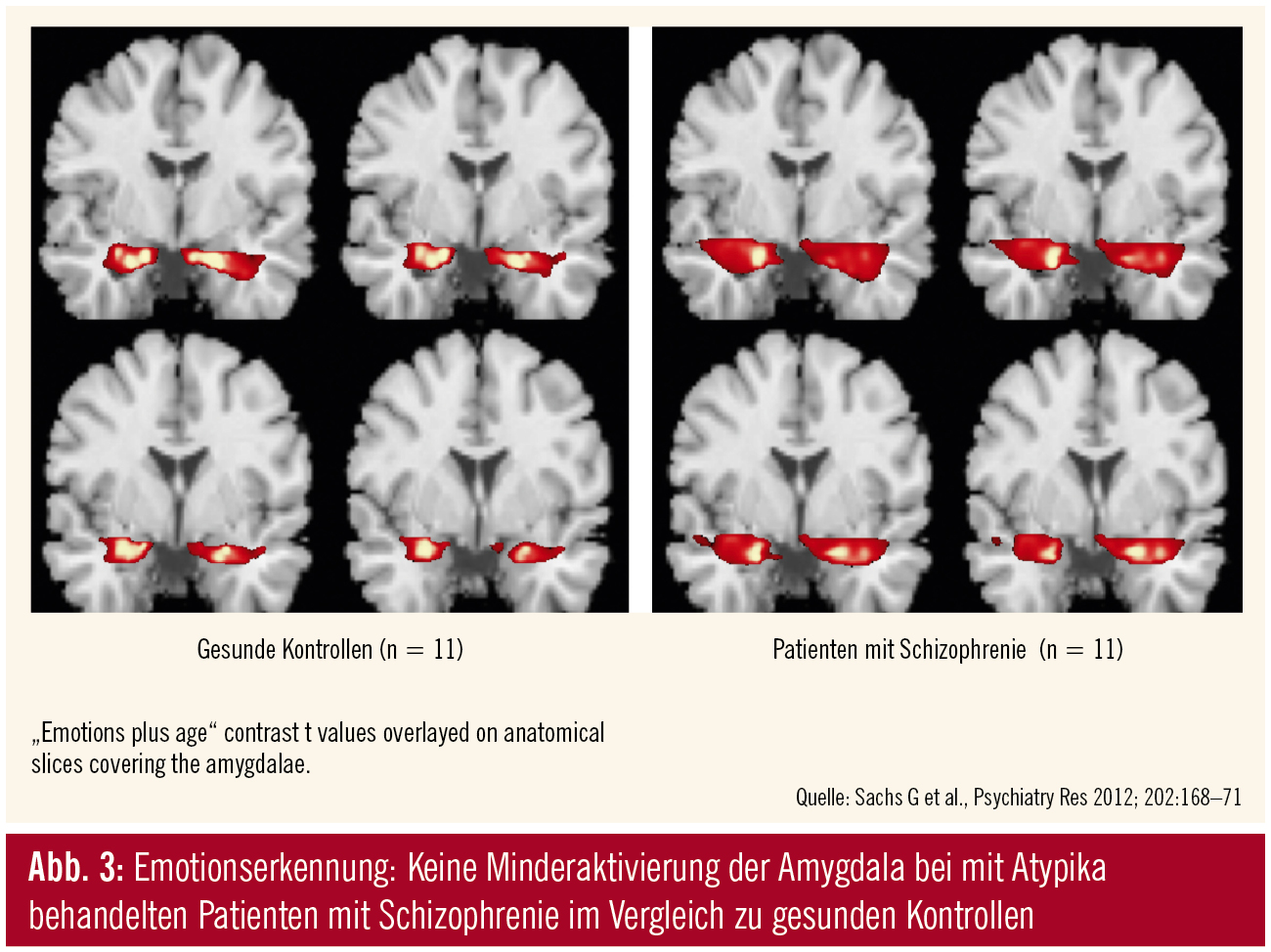
Emotionserkennung: Der Unterschied in der Wirkung der Antipsychotika der 1. und 2. Generation auf soziale Kognitionen hängt auch hier von der Dosierung ab. Die Fähigkeit, Emotionen im Gesicht von anderen zu erkennen, gilt als wesentlicher Aspekt von sozialen Kognitionen und zeigt sich bei Patienten mit Schizophrenie als deutlich beeinträchtigt1. Funktionell-hirnbildgebende Studien zeigen, dass Patienten mit Schizophrenie die Amygdala sowie den Gyrus fusiformis während des Erkennens von Emotionen im Gesicht weniger aktivieren als gesunde Kontrollpersonen13. Erste Hinweise auf einen möglichen positiven Effekt von atypischen Antipsychotika fanden sich in einer Studie von Sachs et al.14. Bei Patienten mit Schizophrenie, die stabil mindestens 6 Wochen auf atypische Antipsychotika eingestellt waren, konnten – im Vergleich zu gesunden Kontrollen – während des Erkennens von Emotionen im Gesicht keine Minderaktivierungen nachgewiesen werden (Abb. 3).
Zukünftige Studien sollten zeigen, inwiefern atypische Antipsychotika (Mit welchen spezifischen Rezeptorprofilen? In welcher Dosierung?) bei schizophrenen Patienten die Aktivierung von spezifischen, die Amygdalafunktion betreffenden Bahnen beeinflussen und dadurch eine adäquate Emotionsverarbeitung als wichtiges Element der postakuten Rehabilitation ermöglichen.
Kognitive „Enhancer“: Derzeit sind neue pharmakologische Substanzen zur Behandlung der kognitiven Defizite bei Schizophrenie, so genannte kognitive „Enhancer“ in Prüfung. Zur Entwicklung von neuen spezifischen neuropsychopharmakologischen Therapiestrategien zur weiteren Verbesserung der kognitiven Defizite organisierten sich im MATRICS-Programm Forschungszentren im NIHM-TURNS-Projekt (Treatment Units for Research on Neurocognition and Schizophrenia). Es wurde klinische Studien und Richtlinien für Studiendesigns sowie eine Testbatterie zur Erhebung der kognitiven Defizite entwickelt. Derzeit aussichtsreichste wichtige Zielstrukturen der Transmittersysteme, die nach heutigem Kenntnisstand für die Pathogenese kognitiver Störungen bei Schizophrenie eine Rolle spielen, sind15:
- der D1-Dopaminrezeptoren im präfrontalen Kortex
- Serotoninrezeptoren im präfrontalen und anterioren zingulären Kortex
- die exzitatorische glutamaterge Synapsen
- der nikotinische Azetylcholinrezeptoren im Hippokampus
- der muskarinische Azetylcholinrezeptoren
- GABA-erge (gamma-amino butyric acid) Systeme
Nichtmedikamentöse Therapieverfahren zur Behandlung von kognitiven Störungen
Einen wesentlichen Beitrag zur Verbesserung der kognitiven Störungen und damit zur Bewältigung der Behinderungen, die als stigmatisierend erlebt werden können, sind das kognitive Training und das Training zur Affektdekodierung (kognitive Remediation). Die kognitive Remediation zeigt beträchtliche Erfolge auf Gedächtnisleistung und exekutive Funktionen bei Schizophrenie. Spezifische rehabilitative Techniken wie „fehlerloses Lernen“ können die Schwierigkeiten der Patienten bei Aufgabenbearbeitungen kompensieren. Für die verbesserte Anpassung im Alltagsleben ist eine zusätzliche Beschäftigungstherapie erforderlich.
Computerisierte Remediationsprogramme: Nachdem frühe Versuche, computerisierte Aufgaben vor allem beim Aufmerksamkeitstraining einzusetzen, ermutigende Erfolge zeigten, wurde von Olbrich und Mitarbeitern das COGPACK16 spezifisch für die Bedürfnisse von Patienten mit Schizophrenie geschaffen (COGPACK®; Marker-Software-Version). Die Subprogramme umfassen Aufgaben in den Bereichen
- Aufmerksamkeit
- Konzentration
- verbale und räumliche Funktionen
- numerische Fähigkeiten
- Reaktionszeit
- Gedächtnis
Das Programm wurde Patienten als „Computerspiel“ vorgegeben und erzielte im Vergleich zu einer Gruppe mit der üblichen Behandlung ohne zusätzliche Intervention signifikante Besserungen im Bereich der Verarbeitungsgeschwindigkeit, der Wortflüssigkeit und des verbalen Gedächtnisses17. Kurtz et al.18 verglichen die Wirkung einer langfristigen, 12 Monate dauernden computerunterstützten Remediationsmaßnahme mit einem ebenso langen und intensiven Training im Umgang mit Computern und Programmen, jedoch ohne kognitive Trainingsaufgaben. Beide Gruppen zeigten deutliche Besserung in den meisten Bereichen, doch hatte die computerunterstützte Remediation eine noch stärkere Wirkung auf das Arbeitsgedächtnis.
Insgesamt kann geschlossen werden, dass Computertraining eine allgemein stimulierende, aber die Remediationsmaßnahme eine darüber hinausgehende spezifische Wirkung auf kognitive Funktionen hat. Eine Metaanalyse wurde von McGurk et al.19 an 26 randomisiert-kontrollierten Studien mit insgesamt 1.151 Patienten mit Schizophrenie durchgeführt. Die stärksten Effekte wurden im Bereich des verbalen Arbeitsgedächtnisses und der Verarbeitungsgeschwindigkeit berichtet, mit zunehmender Anzahl von Übungsstunden verbesserte sich auch das verbale Langzeitgedächtnis. Sachs20 schlug vor, dass Remediationsprogramme in Anpassung an das individuelle Defizitprofil der Patienten erstellt werden sollten, welches die Wirkung der Remediation verstärken könnte21. Eine weitere Metaanalyse von Wykes et al.22 fand geringfügige Effekte auf die gesamten kognitiven Funktionen, zusätzliche Verbesserungen fanden sich durch ergänzende rehabilitative Maßnahmen.
Soziales Kognitionstraining: Ausgehend von den grundlegenden Schwierigkeiten bei Patienten mit Schizophrenie, den emotionalen Ausdruck und die Absichten anderer Personen wahrzunehmen und zu interpretieren, und den daraus resultierenden Problemen, die diese Defizite in der zwischenmenschlichen Alltagsinteraktion mit sich bringen, wurde soziale Kognition zu einem zunehmend wichtigeren Ziel der Remediation. Es wurde eine Anzahl von Programmen entwickelt, die sich in ihrer Komplexität und Zielsetzung unterscheiden und sich teilweise oder ganz computerisierter Aufgaben bedienen. Unter den ersten Trainingszielen stand die Erkennung von Gesichtsausdrücken, ob glücklich, traurig oder zornig.
Ein ausgedehntes manualisiertes Programm des sozialen Kognitionstrainings, das Training der Affektdekodierung (TAD), wurde von Wölwer und Frommann23 entwickelt. Im Training der Affektdekodierung wird die Wahrnehmung der Grundemotionen trainiert sowie die Urteilsfähigkeit hinsichtlich der Intensität mimischer Emotion. TAD führte zu einer Verbesserung in der sozialen Kognition, aber nicht der anderen kognitiven Funktionen, während die kognitive Remediation alleine eine bessere Leistung im Bereich des verbalen Lernens, aber nicht der sozialen Kognition nach sich zog.
Sachs et al.24 untersuchten den Effekt des TAD im Hinblick auf soziale Funktionsfähigkeit und Alltagsfertigkeiten. In der Trainingsgruppe konnten Auswirkungen im Erkennen von Emotionen im Gesicht und in einigen Bereichen der kognitiven Funktionen nachgewiesen werden, die sich in der Gruppe ohne zusätzliches Training nicht fanden. Diese Verbesserungen zeigten sich vor allem im Erkennen von traurigen Gesichtern, weiters kam es auch zu einer Abnahme der Negativsymptomatik. Zusätzlich konnte erstmalig gezeigt werden, dass das TAD auch eine generelle Wirkung auf soziale Fähigkeiten hat. In der TAD-Trainingsgruppe besserte sich in den untersuchten Bereichen der Lebensqualität vor allem die soziale Beziehungsfähigkeit. Dieses Ergebnis weist auf eine Verbesserung der sozialen Interaktionsfähigkeiten hin, dadurch kann das TAD als Trainingsmethode angesehen werden, das zu einer Generalisierung der Effekte in Hinblick auf eine bessere Integration in die Gemeinschaft und in das Alltagsleben führen kann (Abb. 4).
 |
Gabriele Sachs und Hans-Peter Volz (Hg.) Neurokognition und Affektregulierung bei schizophrenen Psychosen. Neuropsychologie, Bildgebung, Testdiagnostik und Behandlung. Stuttgart, Schattauer 2013 |