Neurobiologie der Sucht und Brain-Imaging
Seit Jahrzehnten beschäftigt sich die Suchtforschung damit, die auslösenden und aufrechterhaltenden Faktoren von Suchterkrankungen zu beschreiben und zu analysieren, um das Verständnis dieser Erkrankungen zu fördern und Behandlungsmöglichkeiten zu validieren, zu verbessern und zu erweitern.
Belohnung und Dopamin: Zusammenhänge zum Suchtverhalten
Ein entscheidender Mechanismus im Zusammenhang mit der Suchtentstehung sowie -aufrechterhaltung ist die Verarbeitung von Belohnungen und belohnungsanzeigenden Reizen.
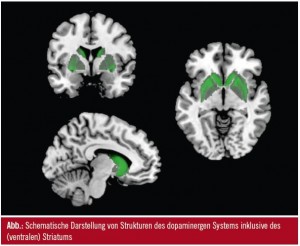
Auf neuronaler Ebene konnte durch Arbeiten am Tiermodell gezeigt werden, dass sowohl die Erwartung einer Belohnung als auch deren tatsächlicher Erhalt zu einer verstärkten Aktivität dopaminerger Mittelhirnneurone führt, welche zum ventralen Striatum (VS, der Kernregion des so genannten hirneigenen „Belohnungssystems“) und anderen mesolimbischen Strukturen hin projizieren1 (Abb.). Neben der Aktivierbarkeit des Dopaminsystems durch Belohnungen unterstreicht auch eine andere Entdeckung die entscheidende Rolle dieses Neurotransmitters im Suchtgeschehen: Auch jegliche Art von Droge, wie z. B. Alkohol, ruft einen direkten Anstieg in der dopaminergen Neurotransmission im VS hervor2. Tierstudien zeigten außerdem, dass vermutlich durch komplexe Konditionierungsprozesse auch suchtbezogene Stimuli – ohne Zugegensein der Droge an sich – die Ausschüttung von Dopamin im medialen präfrontalen Kortex (MPFC) sowie im VS hervorrufen und Annäherungsverhalten an die Droge sowie tatsächlichen Konsum auslösen können.
Bildgebende Verfahren: Beim Menschen können Belohnungsprozesse durch Stimulation mit einer Vielzahl an Reizen untersucht werden, welche von primären Verstärkern wie Nahrung oder Sexualität bis hin zu sekundären Verstärkern wie monetären Belohnungen reichen.
Eine moderne Methode, um die bei der Reizverarbeitung ausgelösten neurobiologischen Prozesse im Gehirn zu untersuchen, stellen dabei bildgebende Verfahren dar. Beispielsweise ermöglicht die funktionelle Magnetresonanztomographie – kurz fMRT – die Untersuchung der Hirnaktivität während der Verarbeitung von Belohnungsreizen, indem das Verhältnis von sauerstoffreichem zu sauerstoffarmem Blut gemessen wird. Der Sauerstoffgehalt gibt dabei indirekt Auskunft über die Aktivität der zugrunde liegenden Neuronen.
In der Suchtforschung wird diese nichtinvasive Art der Bildgebung häufig mit so genannten Reiz-Reaktions-Paradigmen („Cue Reactivity“-Paradigmen) kombiniert, um Prozesse im Gehirn bei der Verarbeitung von Suchtreizen zu untersuchen. Hier können suchtbezogene Bilder oder Wörter, aber auch Gerüche genutzt werden. Trotz der interindividuellen Varianz in der Reaktion auf suchtrelevante Reize sowie der Heterogenität der untersuchten Stichproben (abstinente Alkoholpatienten, Kokainabhängige etc.) gaben die meisten Studien übereinstimmend Hinweise auf bestimmte Hirnareale, die eine erhöhte Aktivierung aufwiesen.
Zu den relevanten Regionen gehört zum einen das anteriore Cingulum (ACC), welches zusammen mit dem benachbarten MPFC mit Aufmerksamkeits- und Gedächtnisprozessen sowie motivationaler Bewertung assoziiert ist. Zum anderen zählt hierzu das Striatum. Dieses lässt sich in einen ventralen (VS) und einen dorsalen Teil (DS) aufgliedern. Das VS erfasst dabei motivationale Aspekte von relevanten (salienten) Reizen, während das DS an der Konsolidierung von Reiz-Reaktions-Mustern und damit an der Bildung von Gewohnheiten beteiligt ist3. Interessanterweise zeigten Studien, dass eine erhöhte (alkohol-)reizinduzierte Aktivierung im ACC und MPFC mit einem erhöhten Rückfallrisiko assoziiert ist4, 5.
Dopaminerge Neurotransmission: Welche Rolle spielt in diesem Zusammenhang die dopaminerge Neurotransmission? Um den direkten Zusammenhang zwischen der durch drogenassoziierte Reize ausgelösten Gehirnaktivierung und dem Botenstoff Dopamin untersuchen zu können, kann mittels Positronenemissionstomographie (PET) in vivo die Neurotransmitterausschüttung sowie die Verfügbarkeit von Rezeptoren und Transportern gemessen werden.
Hier wurde in verschiedenen Studien nachgewiesen, dass bei entgifteten alkoholabhängigen Patienten eine reduzierte Verfügbarkeit und Sensitivität der zentralen Dopamin-D2-Rezeptoren vorliegt, welche eine kompensatorische Herabregulierung nach chronischem Alkoholkonsum darstellen könnte und mit einem erhöhten prospektiven Rückfallrisiko assoziiert ist6.
Weitere Studien zeigten, dass die reduzierte Dopamin-D2-Rezeptor-Verfügbarkeit im VS (inkl. des Nucleus accumbens) sowie eine erniedrigte Dopaminsynthese mit dem selbstberichteten Alkoholverlangen abhängiger Patienten korreliert war7, 8. Interessanterweise war diese Dysfunktion im dopaminergen System, im Speziellen im VS, mit einer erhöhten Hirnaktivierung während der Verarbeitung alkoholassoziierter Bildreize im ACC sowie MPFC assoziiert – Hirnregionen, deren verstärkte Aktivierung während der Präsentation von Suchtreizen wie oben beschrieben mit dem prospektiven Rückfallrisiko verbunden war7. Umgekehrt konnte gezeigt werden, dass die neuronale Reagibilität auf nichtsuchtbezogene, belohnungsanzeigende Reize – wie beispielsweise Geld – vermindert ist9.
Diese Beobachtung unterstützt die Hypothese, dass Alkohol und andere Drogen zu einer Art „Neuordnung“ der Prioritäten des Belohnungssystems führen können, so dass es zu stark auf Suchtreize reagiert, während es nur vermindert durch konventionelle Verstärker (inklusive primärer Verstärker wie Sex oder Nahrung) aktiviert wird. Die verminderte dopaminerge Transmission könnte in diesem Zusammenhang dazu motivieren, Alkohol zu konsumieren, um so das dysfunktionale Dopaminsystem „anzukurbeln“.
Sucht als Störung des Belohnungslernens
Neben dem starken Verlangen nach der Droge ist auch der Konsum trotz besseren Wissens eines der Kardinalsymptome einer Abhängigkeit. Betroffene geben häufig an, „nicht aufhören“ zu können, obwohl sie wissen, dass ein fortgesetzter Konsum weitreichende negative Konsequenzen haben wird.
In einer Primatenstudie von Schultz und Kollegen1 konnte gezeigt werden, dass Dopamin nicht nur entscheidend für die Verarbeitung von Belohnungen ist, sondern auch auf Lernprozesse wirkt. Die Forscher untersuchten mittels Einzelzellableitung die Aktivität dopaminerger Mittelhirnneurone von Affen, während diese eine Lernaufgabe durchführten. Hier zeigte sich, dass eine unangekündigte Belohnung (Saft) eine phasische Dopaminausschüttung nach sich zog. Nachdem diese Belohnung mit einem ankündigenden Hinweisreiz gekoppelt worden war und die Affen diesen Zusammenhang zuverlässig erfasst hatten, zeigte sich die Dopaminausschüttung nur noch während dieses belohnungsanzeigenden Reizes und nicht mehr beim tatsächlichen Erhalt der Belohnung.
„Vorhersagefehler“: Interessanterweise zeigte sich weiter, dass die dopaminerge Aktivität nicht nur für das Erlernen von Belohnungskontingenzen essenziell war, sondern auch für das Verlernen: Beim Ausbleiben der Belohnung trotz Hinweisreiz gab es einen signifikanten Abfall in der Dopaminausschüttung. Das Feuern dieser zum VS projizierenden Mittelhirnneurone bzw. dessen Aktivitätsabfall sind eng mit dem so genannten „Vorhersagefehler“ verknüpft, der die Differenz zwischen der erwarteten und der tatsächlichen Belohnung darstellt und Lernen aus Belohnung/Bestrafung möglich macht.
Da nun wie oben beschrieben die (Alkohol-)Abhängigkeit durch eine Dysfunktion eben dieses dopaminergen Systems gekennzeichnet ist, liegt die Annahme nahe, dass diese Dysfunktion auch mit einer Beeinträchtigung des für Lernprozesse notwendigen „Vorhersagefehlers“ einhergeht. In der Tat zeigten Park und Kollegen10, dass alkoholabhängige Patienten in einem einfachen Lernparadigma signifikant mehr Fehler machten und langsamer lernten.
Auf neurobiologischer Ebene zeigte sich bei den alkoholabhängigen Patienten eine fehlerhafte Konnektivität, d. h. funktionelle Kopplung, zwischen dem VS und dem dorsolateralen präfrontalen Kortex (DLPFC) – eine Hirnregion, die u. a. an der Handlungsplanung und -steuerung beteiligt ist. Diese Dysfunktion im belohnungsassoziierten Lernen könnte – neben der oben beschriebenen verminderten Reaktion auf nichtsuchtassoziierte Belohnungen – erklären, warum es Alkoholpatienten häufig so schwer fällt, ihre Aufmerksamkeit von drogenassoziierten Reizen zu lösen, nichtdrogenassoziierten Belohnungen dieselbe Bedeutsamkeit zuzuschreiben und alternative befriedigende Betätigungen zu finden.
Nichtstoffgebundene Süchte: Ganz anders oder doch sehr ähnlich?
Verhaltensweisen, die wiederholt und exzessiv betrieben werden, die Lebensführung der betroffenen Person beherrschen und zum Verfall der sozialen, beruflichen, materiellen und familiären Werte und Verpflichtungen führen, werden auch unter dem Begriff der nichtstoffgebundenen oder Verhaltenssüchte zusammengefasst.
Ein wichtiger Vertreter dieser Kategorie ist dabei das pathologische Glücksspiel. Im Klassifikationssystem ICD-10 wird pathologisches Glücksspiel im Kapitel „Persönlichkeits- und Verhaltensstörungen“ unter der Kategorie „Abnorme Gewohnheiten und Störungen der Impulskontrolle“11 eingeordnet. Betrachtet man jedoch die diagnostischen Kriterien im Detail, erklärt sich, warum pathologisches Glücksspiel im allgemeinen Verständnis den Verhaltenssüchten zugeordnet wird: Pathologisches Glücksspiel teilt sich mit den substanzgebundenen Süchten eine Reihe von Symptomen12 (Tab.).
Unter der Annahme, dass nichtstoffgebundenem Verhalten ähnliche Pathomechanismen zugrunde liegen wie stoffgebundenen Süchten, werden diese zu einem interessanten Forschungsfeld im Hinblick auf ätiologische Prinzipien der Sucht. Hier ließen sich neurobiologische Veränderungen untersuchen, ohne dass der exzessive und/oder langjährige Konsum einer Suchtsubstanz einen konfundierenden Einfluss auf die wissenschaftlichen Ergebnisse nimmt. So widmen sich auch zunehmend neurobiologische Studien den Unterschieden und Gemeinsamkeiten zwischen pathologischem Glücksspiel und substanzgebundenen Süchten: Während sich die Bemühungen zum besseren Verständnis des pathologischen Glücksspiels vor allem auf Mechanismen der exekutiven Kontrolle bzw. Impulskontrolle konzentrieren13, 14, wenden sich andere Studien mit Blick auf mögliche Suchtmechanismen den Grundlagen von Verlangen und Craving15, 16 und der Belohnungsverarbeitung zu17–20.
Glücksspielrelevante Reize und Belohnungssystem: So untersuchten Studien mittels Bildgebung beispielsweise die Reagibilität auf glücksspielrelevante Reize mit Hilfe bereits erwähnter „Cue Reactivity“-Paradigmen. Crockford und Kollegen15 verwendeten hierzu spielbezogene Videos im Vergleich zu Videos mit Naturszenen, die in einem subjektiv erhöhten Spielverlangen resultierten. Gleichzeitig beobachteten sie im fMRT, dass pathologische Glücksspieler eine verstärkte Aktivierung im rechten DLPFC, im rechten parahippokampalen Gyrus sowie im linken Okzipitalkortex zeigten. In ähnlicher Weise konnten auch van Holst und Kollegen21 vermehrte Aktivität im DLPFC, im ACC und im VS bei Betrachtung spielbezogener Bilder bei Personen mit pathologischem Glücksspiel zeigen.
Studien zur Reagibilität des Belohnungssystems berichten eine herabgesetzte Sensitivität bei Personen mit pathologischem Glücksspiel20, 22, die der oben beschriebenen Dysfunktion des Belohnungssystems bei substanzgebundenen Süchten ähnelt. Reuter und Kollegen20 untersuchten pathologische Spieler und gesunde Kontrollen mittels fMRT während eines Geldgewinnspiels. Sie beobachteten eine reduzierte Aktivität im VS sowie im ventromedialen Präfrontalkortex (VMPFC) bei den pathologischen Spielern, die darüber hinaus mit der Schwere der Symptomatik korreliert war. Ebenso zeigten Balodis und Kollegen19 eine reduzierte Aktivität im VS und VMPFC sowie in der Insula bei Verarbeitung von Verstärkern.
Dysfunktionale Verarbeitung von Verlusten: Zur näheren Erforschung von Faktoren, die zur Aufrechterhaltung des Spielverhaltens trotz negativer Konsequenzen führen, sind so genannte „Fast-Gewinne“ in den Fokus der Aufmerksamkeit gerückt. Verlustereignisse, die in der Wahrnehmung der Person einem möglichen Gewinn nahe waren, führen zu erhöhter Spieltendenz und einer Überschätzung der Gewinnwahrscheinlichkeit23. Studien konnten zeigen17, 18, dass bei gesunden Personen hierbei Regionen wie das Striatum und die Insula aktiviert werden, die auch in die Verarbeitung von Gewinnen involviert sind. Auch bei gewohnheitsmäßigen Spielern zeigte sich bei „Fast-Gewinnen“ eine vermehrte Aktivität des VS, die zudem mit dem Ausmaß des Spielverhaltens korrelierte. Auch scheint die dysfunktionale Verarbeitung von Verlusten einen relevanten Stellenwert in der Neurobiologie des pathologischen Glücksspiels einzunehmen22, was sich klinisch in der Jagd nach Verlusten vom Vortag widerspiegelt. Unklar ist derzeit, inwiefern bei den bisher untersuchten neurobiologischen Veränderungen von prädisponierenden oder krankheitsinhärenten Merkmalen pathologischen Glücksspiels auszugehen ist.
Danksagung: Diese Arbeit wurde unterstützt von der Deutschen Forschungsgemeinschaft(HE 2597/14-1) und vom Bundesministerium für Bildung und Forschung (NGFN Plus 01GS08159).
Resümee
Insgesamt ist von einer neuronalen Dysfunktion in der Belohnungserwartung und -verarbeitung bei abhängigen Menschen auszugehen, unabhängig davon, ob die Sucht an eine Substanz gebunden ist oder sich in einem Verhalten manifestiert. Solche neurobiologischen Befunde können dazu beitragen, das Stigma zu reduzieren, mit dem suchtkranke Menschen sich häufig konfrontiert sehen, und unterstreichen gleichzeitig, dass therapeutische Programme auf die individuellen Bedürfnisse und Schwierigkeiten der Betroffenen eingehen und diese adäquat adressieren sollten, wie etwa durch die Stärkung der Belohnungssensibilität mittels Genusstrainings.