„Die überaktive Blase bringt dich nicht um, aber sie nimmt dir das Leben“ (J. Brown)
Trotz des hohen Leidensdruckes erträgt jede zweite Betroffene ihr Leiden still und unbehandelt. Aus Hoffnungslosigkeit wollen Betroffene nicht einmal mit ihrem Arzt darüber sprechen. Daher ist es die Aufgabe des Arztes, sei es nun der Hausarzt oder ein Facharzt, nach Symptomen der ÜAB zu fragen und nicht vor den Folgen einer in manchen Fällen mühsamen Behandlung zurückzuschrecken. Man darf nicht, wie es leider manchmal vorkommt, über klare Zeichen wie Geruchsentwicklung oder Ähnliches hinwegsehen, nur um Ordinationszeit zu sparen. Es gibt wirksame Therapien, die zumindest die Symptome stark lindern können. Die Patientinnen werden es danken.
Was bedeutet „überaktive Blase“?
Seit 2005 wird allgemein (ICS, deutscher Arbeitskreis für urologische Funktionsdiagnostik etc.) die ÜAB als ein chronisch bestehender Symptomenkomplex aus Harndrang mit oder ohne Harnverlust, meistens verbunden mit erhöhter Miktionsfrequenz (mehr als 8-mal) und Nykturie (mindestens 2-mal) definiert. Eine Harninkontinenz (25–37 %) kann, muss aber nicht bestehen. Darüber hinaus spricht man von einer ÜAB trocken bzw. nass.
Dieses Beschwerdebild kann dabei nicht durch Stoffwechselstörungen oder lokale pathologische Veränderungen erklärt werden, eine sekundäre Drangsymptomatik muss ausgeschlossen werden. Als Beispiele seien genannt: Harnwegsinfekt, Blasentumor, Hormonmangel, Polyurie oder ein offener Blasenhals als insuffizienter Blasenverschluss.
Die Symptome der ÜAB überlappen sich aber auch öfter mit anderen funktionellen Beschwerden des unteren Harntraktes, wie der Belastungsinkontinenz. Hier gilt es dann abzuklären, welche Symptome zuerst auftraten, um so sekundär durch den erwähnten insuffizienten Blasenverschluss entstandene Drangbeschwerden auszuschließen.
Lebensqualität: Die ÜAB hat einen erheblichen Einfluss auf die Lebensqualität. In einer Studie an knapp 2.500 Patientinnen1 gaben etwa 50 % eine deutlich reduzierte Lebensqualität an. Auch bezüglich der Sexualität gaben 31 % der Frauen einen negativen Einfluss an. Zudem setzen weitergehende Folgen wie Stürze bei imperativem Harndrang oder Nykturie, Infektionen und die soziale Isolation den Patientinnen zu. Daher hat J. Brown die Problematik 2004 so formuliert: „Die überaktive Blase bringt dich nicht um, aber sie nimmt dir das Leben!“
Ursachen: Die Steuerung der Blasenfunktion (Harnspeicherung und Entleerung) erfolgt auf verschiedenen übergeordneten Ebenen im ZNS. Bei degenerativen zerebralen Prozessen jeglicher Genese kommt es zu einer verminderten zentralnervösen Hemmung und in weiterer Folge kann eine ÜAB induziert werden. Zur idiopathischen ÜAB gibt es sehr interessante rezente Studien. Funktionelle MRI- und PET-Scan-Untersuchungen bei gleichzeitiger Blasendruckmessung haben bei Patienten mit einer ÜAB eine Veränderung der Abläufe mit Aktivierung anderer Areale im präfrontalen Kortex (PFC) nachgewiesen2. Der mediale PFC, welcher normalerweise für die willentliche Kontrolle der Blase wichtig ist, wurde bei der symptomatischen Gruppe nicht aktiviert, es ergeben sich so genannte „urgency pattern“ oder „Drangmuster“.
Infektionen, Stoffwechselerkrankungen wie Diabetes mellitus oder toxische Einflüsse wie chronischer Alkoholismus können zu Nervenschädigungen bis hin zur Polyneuropathie (PNP) führen, welche sich auch auf die Blasenfunktion auswirken können (sowohl Blasenentleerungsstörungen wie auch ÜAB).
In letzter Zeit befassen sich immer mehr Arbeiten mit dem Urothel und seiner Rolle in der Ätiologie der ÜAB, und man scheint eher über die Afferenzen als über (wie bisher gedacht) die Efferenzen zu einer Lösung der Ätiologie-Frage zu kommen. Die gesamte Blasenwand mit Urothel, Interstitium und Detrusormuskulatur wird als Einheit gesehen3. Das zeigen auch prospektive, vergleichende uro‑dynamisch/ultrastrukturelle Studien, bei denen elektronenmikroskopische Erscheinungsbilder immer in mehreren Kompartments der Detrusorwand gefunden wurden4.
Im Rahmen der Altersblase dürfte es zu einer teilweisen cholinergen Detrusordenervation mit dadurch kompensatorisch gesteigerter muskarinischer Rezeptorsensibilität und den Symptomen einer ÜAB kommen. Auch wurde ein Ansteigen des Anteils atropinresistenter purinerger Rezeptoren auf bis zu 50 % nachgewiesen. Dies wäre eine Erklärung für die reduzierte Wirkung herkömmlicher Anticholinergika in höherem Alter5.
Prävalenz und ökonomische Aspekte: Insgesamt sind epidemiologische Daten zur ÜAB rar und die Methoden kaum standardisiert. Großteils wurden nur Telefonbefragungen oder Fragebögen verwendet. Zwei große Studien in Europa6 und den USA7 zeigen eine hohe Prävalenz in der erwachsenen Bevölkerung. In den USA konnte bei 16,5 % und in Europa (Deutschland, Frankreich, Großbritannien, Italien, Schweden und Spanien) bei über 40-Jährigen bei 17,4 % eine ÜAB nachgewiesen werden6.
Das Verhältnis zwischen Frauen und Männern beträgt 3 : 2, manche Studien zeigen keinen Unterschied. Die reinen Drangbeschwerden ohne Inkontinenz (ÜAB trocken) sind mit 13,6 % bei Männern im Vergleich zu 7,6 % bei Frauen sogar häufiger6. Eine zusätzliche Harninkontinenz besteht bei 25–37 %, wobei hier Frauen häufiger betroffen sind.
Die Häufigkeit der ÜAB nimmt mit dem Alter bei beiden Geschlechtern zu. Jüngere Frauen sind generell mehr betroffen, ab dem 60. Lebensjahr kehrt sich dieser Trend um. Die Folgen der ÜAB beeinträchtigen nicht nur die Lebensqualität, sondern führen auch durch die demografischen Veränderungen mit immer höherer Lebenserwartung zu weitreichenden medizinischen, sozioökonomischen und psychosozialen Auswirkungen. In einer sozioökonomischen Studie wurden die Gesundheitskosten nur für die Inkontinenzform der überaktiven Blase in den USA auf beachtliche 12,0 Mrd. US-Dollar geschätzt7.
Diagnostik und Therapieansätze: Natürlich müssen vor der Therapie Ursachen einer sekundären Drangsymptomatik ausgeschlossen werden. Harnanalyse, Restharnbestimmung, Miktionsprotokoll, eine Zystoskopie mit „Stresstest“ und vaginaler Inspektion mit Palpation zur Bestimmung der Beckenbodenfunktion sowie optional eine Flow-Messung, Sensibilitätskontrolle und Reflexabklärung sind zu empfehlen. Finden sich hier pathologische Befunde, wird man zuerst diese zu therapieren versuchen und erst bei anhaltenden Symptomen in Richtung ÜAB weiterbehandeln.
Eine Heilung bei der idiopathischen ÜAB ist eher selten. Das Ziel muss sein, die Symptome zu lindern und so die Lebensqualität der Betroffenen wieder auf ein möglichst hohes Niveau zu bringen.
Die anticholinerge medikamentöse Therapie ist neben der Verhaltenstherapie (Blasentraining, Toilettentraining) und der Elektrotherapie das wichtigste Standbein in der konservativen Behandlung.
Mirabegron, als ein β-3-Adrenorezep- toragonist, könnte in Zukunft eine Rolle in der Therapie spielen. Die Substanz steht nach erfolgreichen Phase-III-Studien vor der Zulassung.
Bei Hinweisen auf eine interstitielle Zystitis (IC) wird auch eine Blaseninstillationstherapie zur Wiederherstellung einer eventuell geschädigten Blasenschutzschicht (GAG-Layer) mit Hyaloronsäure (Cystistat®) oder Natrium-Chondroitinsulfat-Lösung (Gepan®) empfohlen. Ein tieferes Eindringen dieser oder anderer Substanzen in die Blasenwand gelingt mit EMDA (electromotoric drug administration) auf Basis der Iontophorese8. Näheres zu diesen Therapien im Beitrag „Pelvic Pain“, Botox, Neuromodulation und extravesikale Harnableitung werden im zweiten Teil von OA Johann Wachter abgehandelt.
Verhaltenstherapie, Elektrostimulation und Magnetfeldtherapie: Die guten Ergebnisse für Placebo im Vergleich mit der anticholinergen medikamentösen Therapie sind sicher auf die Zuwendung zum Patienten zurückzuführen. Diese Zuwendung ist ein Teil der Verhaltenstherapie. Diese setzt sich aus dem protokollgesteuerten Trinkregime, der Wahrnehmung der Blasenfüllung und vor allem den gezielten Kneifübungen mit dem Ziel eines Abklingens des Harndranges zusammen. Wichtig ist das Aufbauen eines Vertrauens in diese Unterdrückungsstrategie. Fallweise wird auch eine Miktion nach der Uhr eingesetzt.
Die Erfolgsraten des Kontinenztrainings9 betragen bezüglich der Reduktion der Inkontinenzepisoden 57 %, der Reduktion der Einnässmengen 54 % und der Verbesserung der Lebensqualität 55 %. Dies entspricht durchaus den Ergebnissen der anticholinergen medikamentösen Therapie. Leider ist die Verhaltenstherapie sehr personalintensiv und braucht eine hohe Motivation der damit Befassten. Am besten schneidet eine Kombination von Verhaltenstherapie und Medikamenten ab.
Die bei jüngeren Frauen recht erfolgreich eingesetzte Elektrostimulation über transvaginale oder Klitoris-Clips-Elektroden wird von älteren Patienten nur fallweise akzeptiert. Bei der extrakorporalen Magnetstimulation im Magnetstuhl gibt es keine Akzeptanzprobleme, die Behandlung ist aber sehr kostenaufwendig und selten verfügbar. Eine deutsche Studie zeigte eine Ansprechrate von 54 % bei der ÜAB10. Andere Studien aus Mainz zeigten eine deutliche Verbesserung der Lebensqualität. Insgesamt gibt es wenige wirklich aussagekräftige Studien bei Elektro- und Magnetfeldtherapie. Wie schon erwähnt, beeinflusst die persönliche Zuwendung des Behandlers das Ergebnis deutlich.
Entwicklungen bei den Anticholinergika: Atropin, das Gift der Tollkirsche, ist die Ursprungssubstanz der Anticholinergika. Dessen fatale Wirkung auf Herz, Kreislauf, Gehirn und Verdauungstrakt mit Tachykardie, Blutdrucksteigerung, Atemlähmung, Delir, Fieber und Mundtrockenheit zeigt schon das hohe Nebenwirkungspotenzial, das es bei der Entwicklung einsetzbarer Substanzen zu reduzieren galt.
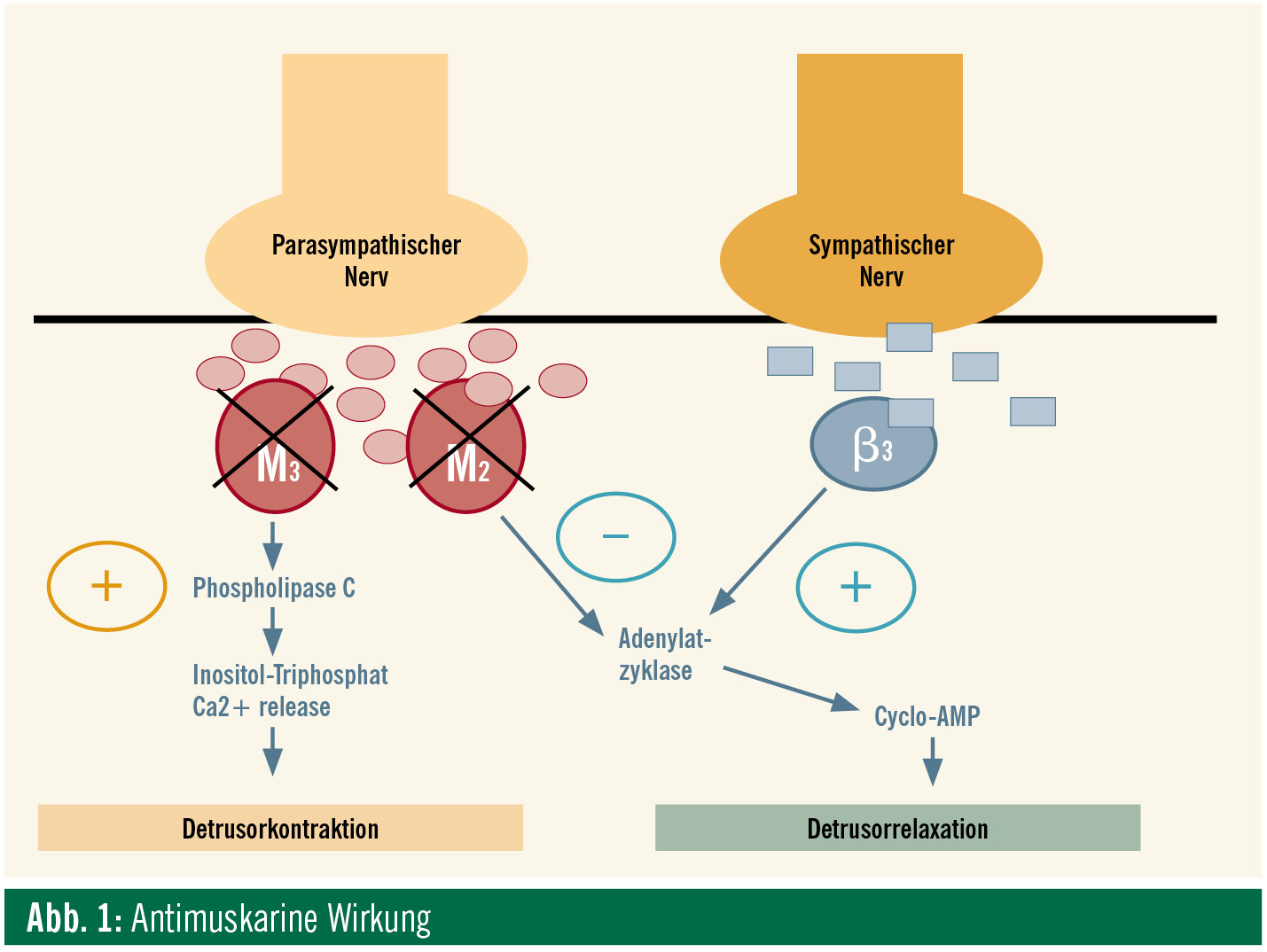
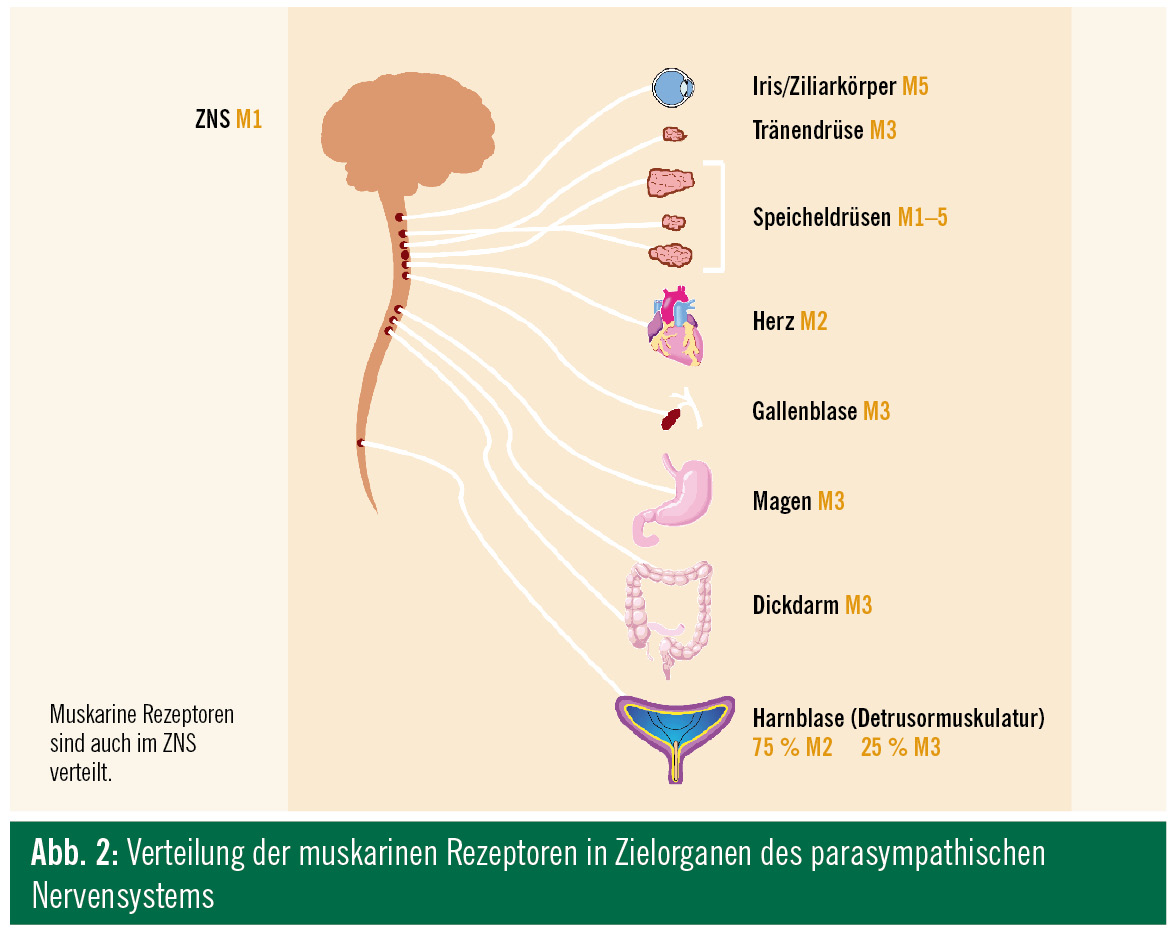
Aufgrund seiner Affinität zu den postsynaptischen Bindungsstellen konkurriert jeder anticholinerge Wirkstoff konzentrationsabhängig mit Acetylcholin. Dies geschieht erwünschterweise an der Blase (Abb. 1), aber auch an den anderen oben aufgezählten Organen (Abb. 2). Das ergibt eine Reihe von möglichen Nebenwirkungen, deren wichtigste die Mundtrockenheit, Obstipation, gastritische Beschwerden, Tachykardie sowie auch eine in letzter Zeit immer mehr in den Mittelpunkt gerückte Beeinträchtigung der kognitiven Fähigkeiten, gemessen an einer Verschlechterung der Gedächtnisleistung, sind.
Die an den entsprechenden Organen befindlichen so genannten Muskarin-Rezeptoren werden mittlerweile aufgrund molekularer Klonierungsuntersuchungen in die Subtypen M1 bis M5 unterteilt. Die Subtypen M2 und M3 sind für die Kontrolle der Blasenmotilität von besonderer Bedeutung. M1-Rezeptoren finden sich besonders im Gehirn. Bei der Entwicklung neuer Substanzen wurde und wird noch immer versucht, ein wirklich subtypenselektives Anticholinergikum mit weniger Nebenwirkungen zu finden.
Die ersten breit eingesetzten Anticholinergika waren Oxybutenin (Ditropan® und zahlreiche Generika), das nebenwirkungsärmere Tolterodin (Detrusitol®) sowie Trospiumchlorid (Spasmolyt®, Inkontan®). Propiverinhydrochlorid (30 mg als Mictonorm uno®) ist leider nicht in Österreich zugelassen, kann aber aus Deutschland bestellt und fallweise erstattet werden.
Neue M3-selektive Medikamente sind Solifenacin (Vesicare®) und Fesoterodin (Toviaz®). Solifenacin wird in Österreich erfolgreich eingesetzt. Es hat eine Halbwertszeit (HWZ) von 56 Stunden und dadurch garantiert die einmal tägliche Einnahme einen konstanten, wirksamen Substanzspiegel. Auch wurde bei dieser Substanz erstmals die „Alarmzeit“ (aus dem englischen „warning time“) in die Studien miteinbezogen, und es konnte eine signifikante Verlängerung nachgewiesen werden11. Toviaz® wird derzeit in Österreich nicht erstattet.
Neben der Entwicklung von neuen Medikamenten wird auch versucht, bekannte wirksame Substanzen durch eine neue Galenik bzw. Applikationsform besser verträglich zu machen. Relativ neu ist auch eine transdermale Formulierung von Oxybutenin (Kentera®). Durch die ständige langsame Aufnahme der Substanz durch die Haut vermeidet man die hohen Serumspiegel und erreicht eine niedrigere Nebenwirkungsrate. Leider traten in etwa 25 % Hautveränderungen an der Applikationsstelle auf, die den Einsatz etwas limitieren.
Bezüglich der zentralen Nebenwirkungen spielt die Liquorgängigkeit der verschiedenen Substanzen eine entscheidende Rolle. Die bis jetzt besprochenen Substanzen waren bis auf Trospiumchlorid alle tertiäre Ammoniumbasen, welche liquorgängig sind, also in das Gehirn gelangen können. In den letzten Jahren konnte eindeutig – besonders für Oxybutenin – der negative Effekt auf diese kognitiven Fähigkeiten nachgewiesen werden (nach Einnahme über 3 Wochen kam es im Gedächtnistest zu Zeichen einer Hirnalterung von 10 Jahren). Somit wird Oxybutenin ab dem 60. Lebensjahr und besonders bei Anzeichen einer Alzheimer-Erkrankung als Dauertherapie nicht mehr empfohlen, der fallweise situative Einsatz ist aber möglich. Tabelle 1 zeigt eine Auflistung der Anticholinergika in Bezug auf die Studienlage bezüglich ihrer ZNS-Nebenwirkungen. Ein Anticholinergikum ohne Auswirkungen auf die Hirnleistung ist Trospiumchlorid. Als eine stark hydrophile, quartäre Ammoniumverbindung kann diese Substanz die Blut-Hirn-Schranke praktisch nicht überschreiten und hat deswegen eine im Versuch vernachlässigbare Liquorgängigkeit. Die Bioverfügbarkeit dieser Substanz ist relativ gering, das wird über eine höhere Dosierung, wie bei der 60-mg-Retard-Formulierung (Urivesc®) ausgeglichen. Acetylcholin besitzt im Gehirn eine überragende Bedeutung für Aufmerksamkeitsprozesse und das Gedächtnis. An dieser Stelle muss man erwähnen, dass die heute bei älterem Menschen oft praktizierte Polypharmazie sehr oft anticholinerg wirkende Medikamente enthält (ältere Antidepressiva, Anti-Parkinson-Mittel, Antiasthmatika, Antihistaminika, Diuretika etc.) und es zu einem kumulativen, toxischen Effekt kommen kann, welcher der Demenz Vorschub leistet. Andererseits bekommen demente Patienten oft Cholinesterasehemmer, welche ihrerseits auf die Blase cholinerg wirken und damit die Drangsymptomatik verschlechtern können. Daran muss gedacht werden, bevor man eine aufgetretene Inkontinenz als Aggravierung der Demenz qualifiziert. Tabelle 2 fasst diese Interaktionen zusammen.
Therapierichtlinien der anticholinergen Therapie
Vorab sind natürlich Kontraindikationen und Nebenwirkungen zu bedenken (Tab. 3).
Allgemein gilt für den Arzt, auch wegen den Richtlinien der ökonomischen Verordnung in Österreich, mit den älteren Substanzen zu beginnen. Bei wem welche Präparate (auch bezüglich älteren oder neuen) wirken, kann nicht vorhergesehen werden. Ein Wechsel bringt oft unerwartete Erfolge12. Neben der Wirksamkeit spielt die Verträglichkeit die größte Rolle, und hier ist der Arzt gefordert, eine genaue Anamnese bezüglich Medikation, Begleiterkrankungen und kognitiven Fähigkeiten zu erheben. Wie oben erwähnt, spielt auch das Alter eine Rolle bei der Wahl des Anticholinergikums. Der Patient sollte schon vor der Therapie ein Miktionsprotokoll führen, dieses wird dann nach etwa 3 Wochen unter der Behandlung wiederholt. Erst ab diesem Zeitpunkt kann man eine wirkliche Aussage über die Wirksamkeit tätigen. Wegen der möglichen Nebenwirkungen sollte man immer mit einer möglichst niedrigen Dosis beginnen und diese erst langsam anheben. In der Folge ist es durchaus legitim, zur Maximaldosis zu gehen oder auch darüber hinaus. Diese dann Off-Label-Anwendung bringt oft noch ein verbessertes Ansprechen. Natürlich müssen eventuelle Nebenwirkungen genau monitiert werden.

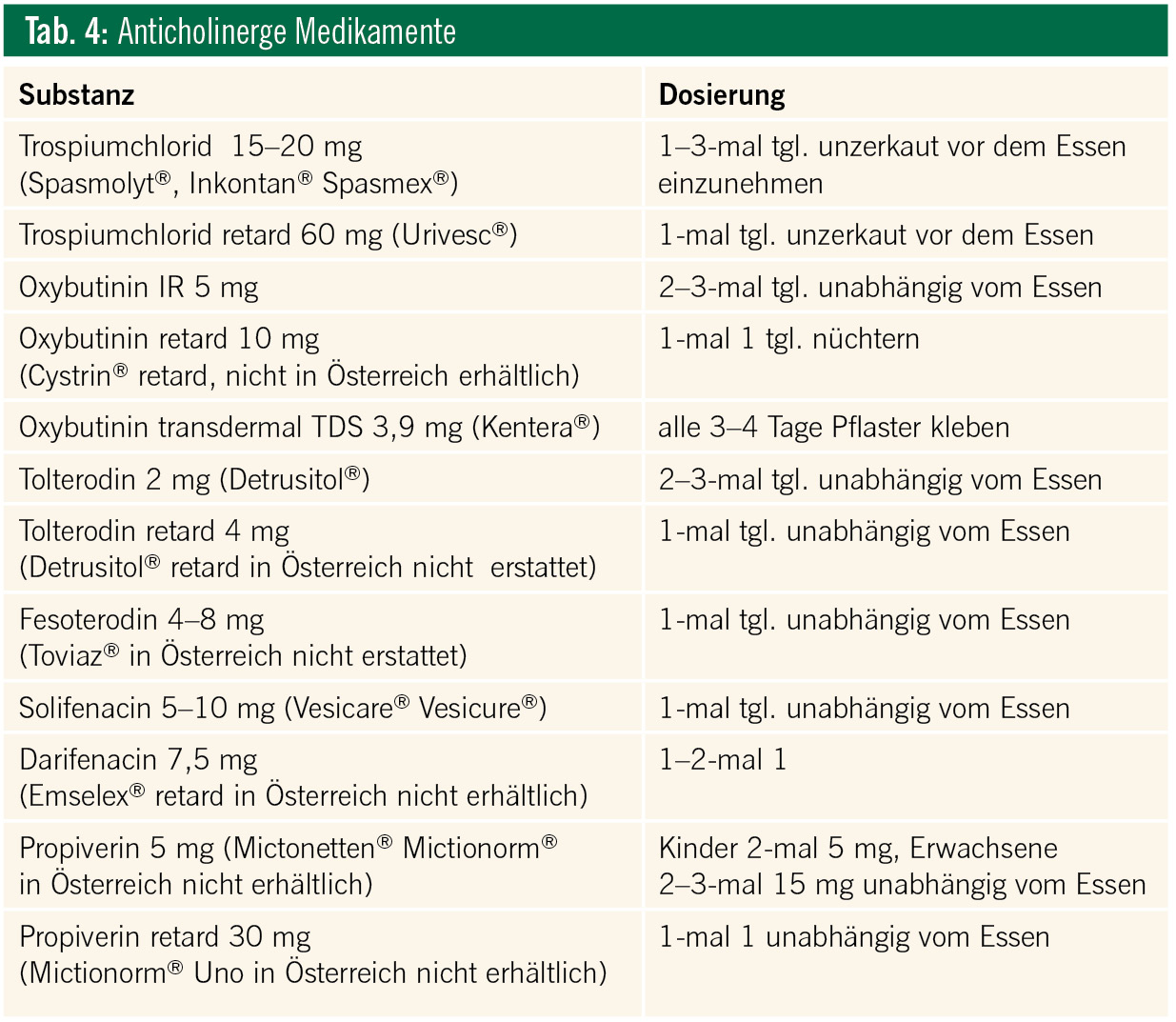
Laut unseren Verschreibungsregeln müssen zwei Substanzen aus der Grünen Box primär eingesetzt werden. Erst wenn keine ausreichende Verbesserung eintritt oder die Nebenwirkungen zu groß sind, darf mit den moderneren Präparaten begonnen werden. Vorteilhaft ist die zusätzliche Einnahme von Ballaststoffen mit der Nahrung oder über z. B. Laevolac®, da besonders ältere Patienten zur Obstipation neigen. Eine Übersicht über alle Anticholinergika inklusive Dosierung und Verschreibbarkeit (Farbe der Box) gibt Tabelle 4.
Insgesamt liegt die Ansprechrate der anticholinergen Therapie bei rund 75 %, wobei man aber nur in etwa 50 % mit einem wirklichen Beherrschen der Symptome rechnen kann. Die einzelnen Antimuskarinika unterscheiden sich hauptsächlich bezüglich der Nebenwirkungen. Fühlt sich der Patient unter einer anticholinergen Therapie gut, möchte aber nicht dauerhaft Medikamente nehmen, so sollte, wenn möglich, ausgeschlichen werden. Oft wird die Therapie auch nur in der kalten Jahreszeit, in der die Symptome öfter auftreten, eingesetzt. Andere Patienten verwenden Anticholinergika nur situativ, wie z. B. bei Busreisen, Wanderungen, Theaterbesuchen oder ähnlichen „heiklen“ Ereignissen.
Wir wissen, dass die Abbruchraten der anticholinergen Therapie nach 4 Monaten um 40 % liegen und weiter bis auf etwas 60–70 % nach einem Jahr ansteigen. Das liegt einerseits an der begrenzten klinischen Effizienz bei gleichzeitig hoher Erwartung von Patientenseite und andererseits an den doch beträchtlichen Nebenwirkungen. Eine Rolle spielt auch das erst langsame Abklingen des anticholinergen Effekts. Vielfach wissen wir nicht, wie es einem Großteil unserer Patienten mit ÜAB auf lange Sicht geht. Sie kommen oft erst nach ein paar Jahren – meistens mit anderen Beschwerden – wieder zu uns. In Richtung Ihrer Beschwerden mit der Blase befragt, haben sie sich gewöhnt, damit zu leben, oder die Beschwerden sind abgeklungen. Die wenigsten nehmen noch die anticholinerge Medikation. Genauere Studien darüber hat es kaum gegeben. Auf dem Global Forum of Incontinence in Prag 2010 hat Milsom eine sehr interessante schwedische Studie zu genau diesem Thema präsentiert. Bei dieser Longitudinalstudie stieg die Prävalenz der ÜAB bei den gleichen Befragten nach 14 Jahren von 16 auf 23 %. In dieser Studie war eine ÜAB trocken bei 50 % der untersuchten Frauen nicht mehr nachweisbar, hatte sich aber bei 23 % in eine ÜAB nass verschlechtert. Eine ÜAB nass war bei 26 % nicht mehr vorhanden und hatte sich bei 21 % in eine ÜAB trocken gewandelt. Von den primär beschwerdefreien Frauen hatten 8 % eine ÜAB trocken und 12 % eine ÜAB nass entwickelt. Man sieht also Entwicklungen in beide Richtungen. Realistische Therapieziele, Nebenwirkungen und die guten Ergebnisse der Verhaltenstherapie sollten bei der Verschreibung eines Anticholinergikums bedacht werden.
Take Home Message