Der nicht tastbare Hoden – Aktuelle diagnostische und therapeutische Strategien
Häufigkeit: Bei ca. 20% aller Knaben mit UDT kann der Hoden nicht getastet werden, wobei sich allerdings eine deutliche Abhängigkeit zur Erfahrung des Untersuchers zeigt. Etwa die Hälfte aller nicht tastbaren Hoden liegt intraabdominal oder gleitet je nach intraabdominalem Druck zwischen Bauchraum und proximalem Leistenkanal hin und her (“peeping testis”). Etwa 45% der NPT sind atroph, z. B. in Folge einer pränatalen Hodentorsion mit Nachweis eines Hodenrudiments (“vanishing testis”, “nubbin”), oder es liegt eine Agenesie vor, und etwa 5% der NPT sind der Palpation entgangen und liegen inguinal.
Diagnostik: Der wichtigste diagnostische Schritt ist die sorgfältige klinische Untersuchung in ruhiger warmer Umgebung. Eine deutliche Asymmetrie oder gar ein hypoplastisches Skrotum gelten als wichtiges Indiz für einen ein- oder beidseitigen Kryptorchismus (> Abb. 1). Nach der Inspektion des Genitalbereichs schließt sich die bimanuelle Palpation des Skrotums und der Inguinalregion mit warmen Händen an. Lässt sich weder skrotal noch inguinal ein Hoden tasten, sollte an die Möglichkeit eines ektopen Hodens gedacht werden und eine sorgfältige Palpation der suprapubischen, perinealen und penilen Region sowie der Oberschenkelinnenseite erfolgen. Bei unruhigen oder adipösen Kindern kann die Untersuchung – auch durch erfahrene Hände – sehr schwierig sein. Wiederholte Untersuchungen sind bei unklaren Befunden zu empfehlen.
Bleibt bei wachen Knaben der Hoden klinisch nicht tastbar, ermöglicht in ca. 20% der Fälle eine weitere Untersuchung in Narkose die Palpation des Hodens. Bleibt der Hoden auch in Allgemeinnarkose nicht tastbar, kann in derselben Anästhesie eine Operation – laparoskopisch oder offen operativ – angeschlossen werden. Der klinischen Untersuchung schließt sich die Sonografie (> 7,5 MHz) an. Der Stellenwert der Sonografie im Rahmen der Diagnostik eines Hodenhochstandes ist umstritten. Sie ist einfach durchführbar, nicht invasiv und kann insbesondere bei adipösen Kindern mit NPT Vorteile bieten. Die Sonografie dient darüber hinaus dem Ausschluss begleitender Anomalien wie Leistenhernien, Hydrozelen etc. Bei unilateralem NPT weist eine kontralaterale kompensatorische Hypertrophie, definiert als > 1,8 cm Längsdurchmesser des normal deszendierten Hodens, in 90% auf eine Monorchie z. B. bei Agenesie oder “vanishing testis” hin.
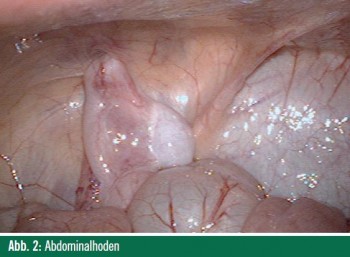
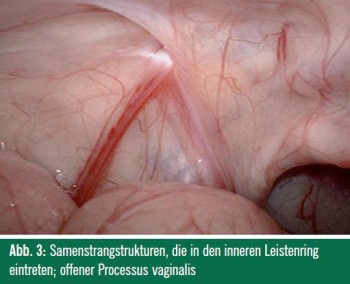
Sonografie und auch andere wegen der Notwendigkeit einer Sedierung oder Narkose im Kindesalter invasivere bildgebende Untersuchungsverfahren wie MRT und CT sind auf Grund ihrer unzureichenden Sensitivität ungeeignet zur Darstellung von Abdominalhoden. Der routinemäßige Einsatz bei Knaben mit NPT sollte daher unterbleiben. Die verlässlichsten Aussagen bezüglich der Hodenlage bei NPT bietet die diagnostische Laparoskopie. Lediglich nach multiplen abdominalen Voroperationen mag eine MRT zur Hodensuche eine Bedeutung haben, da intraabdominale Verwachsungen die laparoskopische Untersuchung erschweren und das Risiko des Eingriffs erhöhen können. Bei nicht voroperierten Kindern treten Komplikationen im Rahmen der diagnostischen Laparoskopie nur sehr selten auf (0,2%). Zu den typischen laparoskopischen Befunde gehören: Abdominalhoden (40%) (> Abb. 2), intraabdominal blind endende Samenstrangstrukturen (15%) bzw. Samenstrangstrukturen, die in den inneren Leistenring eintreten mit oder ohne offenen Processus vaginalis (45%) (> Abb. 3). In Fällen bilateraler NPT und beim geringsten Verdacht auf eine sexuelle Differenzierungsstörung wie z. B. bei begleitenden Fehlbildungen des äußeren Genitale, ist umgehend eine endokrinologische und genetische Abklärung und z. T. auch die interdisziplinäre Abklärung möglicher Syndrome zu empfehlen. Der HCG-Test bei bilateralen NPT wird zunehmend durch die einmalige Bestimmung von Inhibin B ersetzt.
Therapie: Grundsätzlich kann die Therapie des Hodenhochstandes sowohl medikamentös als auch chirurgisch erfolgen. Da die Deszensusrate nach alleiniger Hormontherapie selbst bei nicht deszendierten palpablen Hoden mit maximal 20% enttäuschend ist, sich aber im Vergleich zur alleinigen chirurgischen Therapie positive Effekte in Bezug auf die Fertilitätsparameter zeigen, erfolgt heute in den meisten Fällen eine Kombinationstherapie. Je höher das Risiko einer Fertilitätsbeeinträchtigung ist, desto dringender wird eine neoadjuvante oder adjuvante Hormontherapie empfohlen. Die Deszensusrate nach Hormontherapie bei NPT ist vernachlässigbar gering, aber immerhin 15% initial NPT waren nach neoadjuvanter Hormontherapie palpabel, so dass möglicherweise eine Operation erleichtert wird.
Die chirurgische Standardtherapie bei nicht deszendierten palpablen Hoden besteht in der inguinalen Freilegung, Funikulolyse und Orchidopexie nach Shoemaker. Bei der chirurgischen Therapie nicht palpabler Hoden unterscheidet man prinzipiell offen operative und laparoskopische Verfahren.
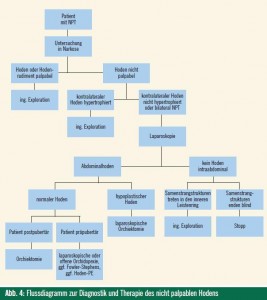
Bei NPT sollte prinzipiell eine Kontrolluntersuchung in Narkose erfolgen. Ist in Narkose ein Hoden oder ein Hodenrudiment palpabel, erfolgt primär die inguinale Freilegung. Ebenso erfolgt eine primäre inguinale Freilegung bei Hypertrophie des kontralateralen Hodens, da mit hoher Wahrscheinlichkeit mit einem “vanishing testis” zu rechnen ist (s. o.).
Bei fehlender kontralateraler Hypertrophie ist die primäre diagnostische Laparoskopie ebenso indiziert wie bei beidseitigem Kryptorchismus. Das weitere Vorgehen ist vom intraoperativen Befund und vom Alter des Kindes abhängig.
Hochinguinal oder abdominal gelegene erhaltungswürdige Hoden mit langem Ductus deferens und kurzen Samenstranggefäßen können durch eine ein- oder zweizeitige Operationstechnik nach Fowler-Stephens nach skrotal verlagert werden. Die mikrovaskuläre Autotransplantation bleibt speziellen Zentren vorbehalten. Nach Abschluss der Pubertät sollten ein kryptorcher Hoden und insbesondere ein Abdominalhoden u. a. auf Grund des erhöhten Risikos einer Hodentumorentstehung orchiektomiert werden. Ab einem Alter von 10 Jahren wird routinemäßig eine Hodenbiopsie zum Ausschluss einer TIN empfohlen. Auch die Entfernung eines “nubbins” wird derzeit empfohlen, da in bis zu 5-15% noch vitales Hodengewebe und damit potenziell entartungsfähige Zellen nachweisbar sind. Das Risiko einer malignen Entartung ist allerdings bei Hodenrudimenten im Vergleich zu Abdominalhoden sehr gering.
Take Home Message
|
Literatur bei der Verfasserin
Weiterführende Literatur:
– Esposito C et al., Nat Clin Pract Urol 2008 May; 5(5):252-60. Review
– AWMF-Leitlinien-Register Nr. 006/022; Leitlinie Hodenhochstand – Maldescensus testis