Nierenzellkarzinom – Konzept der aktiven Überwachung und chirurgische Interventionsmöglichkeiten
Die steigende Inzidenz an kleinen Nierentumoren (Durchmesser 2–4 cm) um das 10-Fache innerhalb der letzten 15 Jahre ist nicht zuletzt auf die Entwicklung im Bereich der bildgebenden Diagnostik zurückzuführen. Bei der Computertomografie ist mittlerweile eine 100%-ige Sensitivität gegeben. Angesichts der Tatsache, dass 70–80 % der diagnostizierten Tumoren Zufallsbefunde sind und die höchste Inzidenz bei komorbiden Patienten älter 70 Jahre verzeichnet wird, stellt sich die Frage, ob eine operative Vorgehensweise immer die sinnvollste Entscheidung darstellt. Aus einer von Klatte et al. durchgeführten Studie1 geht zwar hervor, dass auch bei kleinen Nierentumoren in zirka 7 % eine Metastasierung vorliegt, Daten aus Studien zur aktiven Überwachung (AS) haben jedoch gezeigt, dass bei einem gewissen Patientengut (z.B. hohes Alter) unter bestimmten Voraussetzungen (Tumor < 4 cm, Vorliegen von Komorbiditäten) auf eine vordergründige (nierenerhaltende) Operation verzichtet werden kann. Unter den kleinen Nierentumoren finden sich generell ca. 20 % gutartige und 80 % Nierenzellkarzinome, wobei Letztere fallweise mit einem potenziell aggressiven Verlauf einhergehen.
Aktive Überwachung: Einfluss von Tumorgröße und -volumen: In mehreren Studien wurde das Prinzip der AS unter verschiedenen Aspekten untersucht, allerdings wurden so gut wie keine Anhaltspunkte identifiziert, die eine Prognose ermöglichen würden.
Was die Aggressivität betrifft, wird in der Literatur vorwiegend eine Tumorgröße von 3 cm als kritischer Grenzwert berichtet, ab welcher von einer zunehmenden Aggressivität des Tumors ausgegangen werden muss. Von Relevanz ist jedoch auch die TNM-Klassifikation, die eine Unterscheidung bei einer Größe von 4 cm zwischen Stadium T1a und T1b vornimmt. Bei Untersuchungen zum Tumorwachstum konnten im Rahmen klinischer Studien signifikante Unterschiede zwischen Tumoren ≤ 4cm und > 4 cm Größe nachgewiesen werden: Beispielsweise wurde in einer Metaanalyse aus dem Jahr 2006 in einer Studie zur AS von Volpe et al.2 auch bei gutartigen Tumoren mit einer initialen medianen Größe von 2,4 cm ein Wachstum von 0,3 cm pro Jahr festgestellt. Bei einem medianen Follow-up von drei Jahren fand sich keine Korrelation des Wachstums mit primärer Tumorgröße, Fuhrman-Grad oder Benignität/Malignität (Onkozytom vs. Nierenzellkarzinom). In einer norwegischen Studie von Beisland et al.3 erwies sich das Wachstum in Relation zur initialen Größe zwar nicht als signifikant, das Tumorvolumen bei Tumoren ≤ 4 cm vs. > 4 cm hingegen zeigte sehr wohl eine Korrelation mit der initialen Größe. Diese Ergebnisse lassen darauf schließen, dass neben der Tumorgröße das Tumorvolumen wesentlich berücksichtigt werden muss, wenn eine AS in Erwägung gezogen wird.
Vorhersage des Tumorwachstums mittels Bildgebung? Bei einer Entscheidung zu einer AS via serielle (halbjährliche) CT-Untersuchungen muss bei Kontrolle der Tumorgröße ein Schwankungsbereich von 0,2–0,3 cm, bei Beobachtung der Volumenzunahme ein Schwankungsbereich von 2,0–2,5 cm3 berücksichtigt werden. Von besonderer Relevanz ist die exponenzielle Zunahme des Tumorvolumens in Abhängigkeit vom Tumor-Durchmesser. Ein Messfehler im Spiral-CT von +/– 0,5 cm sowie eine radiologisch bedingte Variabilität sind nicht vermeidbar. In einer 2007 von Kunkle et al.4 publizierten Studie zum Tumorwachstum unter AS hat sich gezeigt, dass ca. ein Drittel der Patienten (25–33 %) ein so genanntes „Zero Growth“, also kein Wachstum, aufweisen. Diese Zahlen spiegeln sich in der gesamten Literatur zur AS wider. Das Wachstum erlaubt dabei keinen Rückschluss auf den Tumortyp, denn Nierenzellkarzinome weisen eine ähnliche prozentuelle Größenzunahme auf wie gutartige Tumoren. Insgesamt wurde jedoch in vielen Studien ein durchgängig geringes Risiko für eine Progression bei kleinen Nierentumoren festgestellt. Eine Vorhersage des Tumorwachstums mittels Bildgebung ist allerdings aufgrund der vorliegenden Daten nicht möglich.
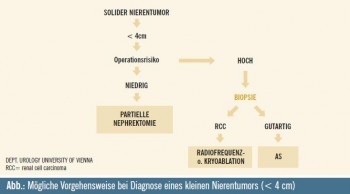
Radikale Nephrektomie vs. organerhaltende Operation vs. AS: Obwohl langfristig gesehen keine signifikanten Unterschiede im progressionsfreien Überleben nachweisbar sind, die für eine radikale Nephrektomie sprechen würden, wird die organerhaltende Operation laut Statis tik definitiv noch zu selten praktiziert. In der EORTC-Studie 309045 wurde die Nichtunterlegenheit einer nierenerhaltenden Operation gegenüber der radikalen Nephrektomie belegt: Nach einem medianen Follow-up von 9,3 Jahren kam es basierend auf 541 eingeschlossenen Patienten bei nur neun im radikalen und vier im konservativen Arm zu einer Progression. Zudem spricht für die Nierenteilresektion die Tatsache, dass eine radikale Nephrektomie mit einem größeren Risiko für eine chronische Niereninsuffizienz assoziiert ist. Basierend auf den EAU-Guidelines (European Association of Urology) 2010 (6.2.3)6 sollte daher die partielle Nephrektomie und, bei entsprechender Expertise des behandelnden Chirurgen, eine laparoskopische Tumorresektion SOC-gemäß (Standard of Care) durchgeführt werden. Die Entscheidung für eine AS wird im Allgemeinen individuell gestellt und hängt im Wesentlichen auch vom Operationsrisiko des jeweiligen Patienten ab – ein Beispiel für das Prozedere bei Vorliegen eines soliden Tumors < 4 cm ist in der Abbildung dargestellt. Die Tatsache, dass nachweislich eine Tendenz zur Übertherapie bei alten Menschen vorliegt, lassen die AS trotz der eingeschränkten Datenlage als attraktive Alternative zu operativen Maßnahmen erscheinen.
1 Klatte T et al., J Urol. 2008; 179(5):1719–1726
2 Volpe A et al., Cancer 2004; 100:738–745
3 Beisland C et al., Eur Urol 2009; 55:1419–1529
4 Kunkle DA et al., J Urol 2007; 177:849
5 http://www.news-medical.net/news/20100419/EORTC-30904-study- Conservative-surgery-not-inferior-to-radical-renal-surgery.aspx
6 http://www.uroweb.org/?id=217&tyid=1
INTERVIEW:
SPECTRUM UROLOGIE: Welche wesentlichen Neuerungen haben sich in den vergangenen Jahren auf dem Gebiet der chirurgischen Therapie des Nierenzellkarzinoms vollzogen? OA Dr. Mesut Remzi:
Beim lokalisierten Nierenzellkarzinom sollte, sofern dies technisch realisierbar ist, immer nierenerhaltend operiert werden. Wenn auch diesbezüglich ein geringer Evidenzlevel vorliegt, so existieren zahlreiche Studien, in denen für die Nierenerhaltung gezeigt wurde, dass das tumorspezifische Überleben nach 5 Jahren bei bis zu 100 % liegt. Allerdings muss erwähnt werden, dass die Nierenerhaltung – und hier wiederum die laparoskopische Vorgehensweise – einen im Vergleich zur radikalen Nephrektomie wesentlich komplizierteren Eingriff darstellt. Bei der kompletten Nierenentfernung gilt der laparoskopische Zugang mittlerweile als Standard und hat als Erstlinientherapie in die EAU Guidelines 2010 (6.2.1)1 Einzug gefunden.
Welche Techniken bieten sich bei nierenerhaltener Vorgangsweise?
Es gibt hier verschiedene Techniken, von denen sicherlich die Laparoskopie die wichtigste Methode darstellt, wobei ihre Umsetzung in den klinischen Alltag noch nicht breitflächig vollzogen ist. Die Expertise des Chirurgen spielt hierfür eine entscheidende Rolle, da aufgrund einer im Vergleich zur offenen Operation wesentlich längeren Ischämiezeit die Gefahr einer dauerhaften Nierenfunktionsschädigung gegeben ist. Als Alternativmethoden zur Laparoskopie sind die Kryoablation sowie die Radiofrequenzablation (RFA) zu erwähnen. Beide Methoden führen onkologisch zu schlechteren Endresultaten als die laparoskopische Nierenerhaltung. Die RFA ist mit technischen Problemen assoziiert und hinsichtlich ihrer Ergebnisse der Kryoablation unterlegen. In einer von uns durchgeführten Studie konnte gezeigt werden, dass die Kryoablation aufgrund ihrer geringen Komplikationsrate für ältere, komorbide Patienten wesentliche Vorteile gegenüber einer partiellen Nephrektomie bietet. Die Arbeit wird demnächst im Journal of Endourology erscheinen.2
Inwieweit hat sich das Konzept der aktiven Überwachung bei kleinen Nierentumoren durchgesetzt?
Unter Berücksichtigung der Tatsache, dass 20 % der kleinen Nierentumoren gutartig sind, stellt sich die Frage, ob bei jedem Patienten jeder Tumor behandelt werden muss. Das Konzept der aktiven Überwachung ist eine relativ „junge“ Vorgehensweise im Bereich der urologischen Onkologie, und die Entscheidung dafür ist vorwiegend auf Erfahrungswerte und Vorschläge in der Literatur gestützt, da keine etablierten Guidelines für das Prinzip der aktiven Überwachung vorliegen. Die wichtigsten Kriterien für die Entscheidung zu einer aktiven Überwachung sind sicherlich durch das Alter und die Komorbiditäten eines Patienten gegeben: bei Vorliegen eines hohen Alters in Kombination mit signifikanten Komorbiditäten ist meines Erachtens die Indikation für eine aktive Überwachung in Erwägung zu ziehen. Das Prozedere bei der Wahl einer – bzw. dem Verzicht auf eine – Therapie ist definitiv eine individuelle.
1 http://www.uroweb.org/?id=217&tyid=1
2 Klatte T et al., Perioperative, oncological and functional outcomes of laparoscopic renal cryoablation and open partial nephrectomy: a matched pair analysis. In press