Uneinheitliches Management des fortgeschrittenen Prostatakarzinoms in Österreich
Methodik: Es wurde ein 10-seitiger Fragebogen etabliert, der verschiedene Aspekte des Managements von Patienten mit einem fortgeschrittenem Prostatakarzinom (PCa) umfasste. Zusätzlich wurden insgesamt 4 Fallbeispiele präsentiert und in 3 Fragen die EAU-Leitlinientreue erfragt. Diese Fragebogen wurden an 150 Urologen in Österreich versandt.
Die Rücklaufquote betrug 97 %, somit konnten insgesamt 143 Fragebögen zur Auswertung gebracht werden. Der berufliche Hintergrund der teilnehmenden Urologen setzte sich wie folgt zusammen: 82 % waren Urologen mit §2-Kassenordinationen, 6 % hatten nur die so genannten „kleinen“ Kassen, und die verbleibenden 12 % waren Spitalsfachärzte mit Wahlarztordinationen. Dementsprechend groß war die klinische Erfahrung der teilnehmenden Urologen. Die Berufserfahrung betrug weniger als 10 Jahre bei 10 %, 11–20 Jahre bei 45 %, 21–30 Jahre bei 25 %; eine Berufserfahrung von mehr als 30 Jahren wurde von 18 % angegeben; über 60 % der Urologen gaben an, mehr als 15 PCa-Patienten pro Monat zu betreuen.
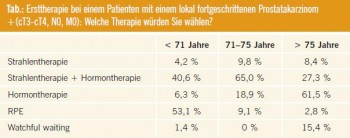
Behandlungsstrategien beim lokal fortgeschrittenen PCa: Die Tabelle fasst die Angaben zu den Behandlungsstrategien beim lokal fortgeschrittenen PCa zusammen. Bei Patienten jünger als 71a hält sich die Therapieempfehlung radikale Prostatektomie und kombinierte Strahlen-Hormontherapie weitgehend die Waage. Eine reine Strahlentherapie, eine primäre Hormontherapie bzw. ein Watchful Waiting wird kaum durchgeführt. Mit zunehmendem Alter wird die radikale Prostatektomie kaum noch empfohlen, dafür nimmt der Stellenwert der Strahlen-/Hormontherapie sowie der reinen Hormontherapie zu. In der älteren Patientengruppe wird ein Watchful Waiting zunehmend eingesetzt (15 %). Diese Abbildung unterstreicht die Divergenz in den Behandlungsstrategien, was primär durch den Mangel an kontrollierten Studien bedingt ist.
Die einzige randomisierte Studie zur RPE konnte nach 8–10 Jahren keinen signifikanten Überlebensvorteil der Operation gegenüber Watchful Waiting bei den über 65-Jährigen nachweisen, insofern muss die Indikation zur RPE bei den über 70-Jährigen heute kritisch gestellt werden1.
Die alleinige Strahlentherapie gilt beim lokal fortgeschrittenen PCa als obsolet: in mehreren kontrollierten Studien konnte der positive Effekt einer (neo-)adjuvanten Hormontherapie nachgewiesen werden. Wir erfragten auch die Dauer der Hormontherapie im Rahmen einer Strahlentherapie: 90 % der Urologen gaben an, diese für 6 Monate bis 3 Jahre zu geben; dies entspricht den gängigen Empfehlungen.
Interessant ist die Beobachtung, dass nach wie vor wenige Urologen eine Watchful-Waiting-Strategie beim lokal fortgeschrittenen PCa einsetzen. Diese Fragestellung wurde nämlich in einer großen, randomisierten Studie untersucht (EORTC 30891)2. Eingeschlossen wurden fast 1.000 Patienten im Tumorstadium (T0-4 N0-2 M0), die keiner kurativen Therapie zugeführt werden konnten. Sie erhielten entweder eine sofortige Hormontherapie oder erst bei symptomatischem Krankheitsprogress. Der sofortige Androgenentzug resultierte in einem moderaten, aber statistisch signifikanten Anstieg des Gesamtüberlebens2. Es zeigte sich aber kein signifikanter Unterschied in der krankheitsspezifischen Mortalität und im symptomfreien Überleben im Vergleich zum verzögerten Therapiebeginn; 50 % der Patienten im verzögerten Therapiearm benötigten nie eine Hormontherapie2. In einer Subgruppenanalyse konnte man nachweisen, dass Patienten über 70 Jahre mit einem PSA von < 50 ng/ml und einer PSA-DT > 12 Monaten von einer sofortigen Androgenentzugstherapie eher nicht profitieren.
Fallbeispiel 1
Behandlungsstrategien des PSA-Rezidivs nach RPE
Die möglichen Behandlungsstrategien wurden anhand des folgenden Falles untersucht: Patient 57 Jahre, RPE vor 20 Monaten (pT3aR0, pN0, Gleason Score 8), PSA 3 Monate nach RPE nicht nachweisbar; 12 Monate nach der OP 0,8 ng/ml, 15 Monate nach OP 1,2 ng/ml, 18 Monate nach OP 2,2 ng/ml. Der Patient ist asymptomatisch, DRU negativ, Scan negativ, CT: o. B.
Die Therapievorschläge der Urologen waren wie folgt (Mehrfachantworten möglich): Antiandrogen-Monotherapie: 17,9 %
externe Irradiatio plus LHRH für 6 Monate: 24,5 %
externe Irradiatio als Monotherapie: 18,4 %
kontinuierliche LHRH-Therapie: 21,8 %
maximale Androgenblockade 7,1 %
intermittierende Hormontherapie: 4,6 %
Watchful Waiting: 3,6 %
Orchiektomie: 2 %
Es fällt eine deutliche Divergenz der Therapievorschläge auf, die auch dadurch bedingt ist, dass es kaum möglich ist, zwischen einem lokalen und/oder systemischen Rezidiv zu diskriminieren. Die Wertigkeit einer externen Irradiatio bei dem o. a. Fall ist umstritten. Eine langfristige PSA-Kontrolle wird nur bei Patienten mit einem PSA-Wert von unter 0,5 ng/ml zum Zeitpunkt der Bestrahlung relativ verlässlich erreicht. Diesbezüglich sei auf die exzellente Arbeit von Stephenson et al. hingewiesen, der für diese Fragestellung ein Nomogramm entwickelt hat3. Für eine intermittierende LHRH-Therapie entschieden sich nur 4,6 % der Fachärzte, dies entspricht durchaus den EAULeitlinien, die diesen Approach (noch) als experimentell ansieht. Erste Daten aus randomisierten Studien zeigen aber, dass das progressionsfreie sowie das Gesamtüberleben unter einer kontinuierlichen und intermittierenden Hormontherapie identisch sind; zur Gruppe mit einem PSA-Rezidiv gibt es aber noch keine validen Langzeitdaten4. Die verbesserte Lebensqualität und der in der Regel lange Verlauf sprechen jedoch für einen intermittierenden Approach4.
Fallbeispiel 2
Primär metastasiertes PCa
Patient: 76 Jahre, minimale Miktionsbeschwerden (IPSS 6), Restharn 30 ml, DRU: mäßig vergrößerte, derbe Prostata, PSA: 198 ng/ml, Biopsie: 8/8 Stanzen positiv, US/Niere: bds. o. B. Scan: 4 suspekte Herde im Achsenskelett.
Wie schon bei Fall 1 davor, besteht auch hier eine deutliche Varianz der Therapieoptionen: 43,9 % der Urologen entschieden sich für eine kontinuierliche LHRHTherapie (inkl. Flare-up-Therapie), 22,4 % für eine maximale Androgenblockade und 21,4 % für eine bilaterale Orchiektomie. Es war für uns überraschend, dass so viele eine maximale Androgenblockade (MAB) favorisieren. Unter einer MAB verbessert sich das 5-Jahres-Überleben um ca. 2–5 %5. In den EAU-Leitlinien wird hinterfragt, ob dieser marginale Überlebensvorteil klinisch relevant ist. Zur intermittierenden Hormontherapie bei M+-Patienten wurde von da Silva die erste randomisierte Studie vorgestellt6. Es zeigte sich, dass das Gesamtüberleben im kontinuierlichen und intermittierenden Studienarm identisch war6. Bezüglich des gegenwärtigen Standes der intermittierenden Hormontherapie sei auf einen kürzlich erschienen Review hingewiesen4.
Übereinstimmung mit den EAU-Leitlinien
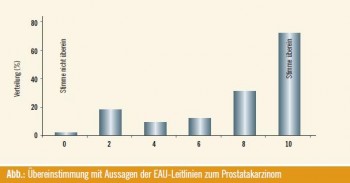
Im Rahmen der Untersuchung wurden die Urologen mit 5 Aussagen der EAULeitlinie7 zum Management des fortgeschrittenen PCa konfrontiert und befragt, inwieweit Sie mit diesen übereinstimmen. Die größte Übereinstimmung fand sich für die Aussagen „Die Kombination von externer Strahlentherapie mit einer Hormontherapie ist besser geeignet als eine reine Strahlentherapie.“ und „Ein Androgenentzug ist eine Therapieoption, die sich bei Patienten mit biochemischem Rezidiv mit Fernmetastasierung empfiehlt.“ Die geringste Übereinstimmung fand sich für die Aussage: „Die neoadjuvante Hormonbehandlung vor RPE ist keine Therapieoption für Patienten mit lokal fortgeschrittenem PCa.“ Dies zeigt, dass die neoadjuvante Hormontherapie vor RPE zeitweise eingesetzt wird, was in Diskrepanz zur EAU-Leitlinie steht; diese stellt klar fest, dass dieser Approach keinen relevanten Vorteil zeigt (Abb.).
Schlussfolgerung
Die vorliegende Untersuchung, an der etwa die Hälfte aller §2-Urologen in Österreich teilgenommen hat, zeigt die bestehenden Behandlungsstrategien beim fortgeschrittenen PCa auf. Diese Umfrage belegt eine zum Teil deutliche Divergenz der Therapieoptionen, was auch den Mangel kontrollierter Studien und die damit nur vagen Leitlinienempfehlungen widerspiegelt. Natürlich spiegelt diese Varianz auch die verschiedenen Patientenwünsche wider. Um die Behandlung des fortgeschrittenen PCa zu harmonisieren, sind weitere kontrollierte Studien dringend erforderlich. Basierend auf diesen Studien müssen dann fundierte Leitlinienempfehlungen ausgearbeitet werden.
1 Bill-Axelson et al., N Engl J Med 2005; 352:1977–1984
2 Studer et al,. J Clin Oncol, 2006; 24:1868–1876
3 Stephenson et al., J Clin Oncol, 2007; 25:2035–2041
4 Boccon-Gibod et al., BJU Int 2007; 100:738–743
5 Calais da Silva et al., Eur Urol 2009; 55:1269–1277
6 Prostate Cancer Trialists’ Collaborative Group, The Lancet 2000; 355:1491–1498
7 www.eau.org