Langzeitmanagement der Plaque-Psoriasis – Wirksamkeit und Sicherheit von Biologika
Biologika werden seit über 10 Jahren in der Behandlung der Psoriasis vulgaris mit Erfolg eingesetzt. Selbst schwerste Formen dieser Erkrankung wurden behandelbar gemacht. In Zusammenschau von Aufklärung, richtiger Indikationsstellung, optimaler Therapieplanung, regelrechtem Monitoring und Beobachtung möglicher unerwünschter Wirkungen haben diese Therapeutika ein gutes Sicherheitsprofil und stellen eine wichtige Medikamentengruppe in der Behandlung der Psoriasis dar.
Die Erkrankung: Psoriasis ist eine T-Zell-mediierte, entzündliche, chronische Systemerkrankung, die sich in erster Linie an der Haut manifestiert. Sie beginnt häufig im frühen Erwachsenenalter und persistiert dann meist. Weltweit sind 2–3 % der Bevölkerung von dieser Erkrankung betroffen. Die häufigste klinische Form ist die chronische Plaque-Psoriasis mit scharf begrenzten silbrig-weißen, schuppenden, erythematösen Plaques in typischer Verteilung. Bei mehr als 90 % der Patienten verläuft die Erkrankung chronisch.1 20–30 % der Psoriasispatienten entwickeln eine seronegative Polyarthritis.2 In Abhängigkeit von Dauer und Schwere der Erkrankung besteht auch ein erhöhtes Risiko für Adipositas, das metabolische Syndrom sowie kardiovaskuläre und psychische Erkrankungen.3, 4
Therapieziel: Da die Ätiologie der Erkrankung letztlich ungeklärt ist, gibt es keine kurative Therapie. Das Therapieziel ist daher, eine lang anhaltende Erscheinungsfreiheit zu erzielen. Daten aus klinischen Studien zeigen einen Zusammenhang zwischen einer effizienten Therapie der Psoriasis und einem verminderten Risiko für kardiovaskuläre Erkrankungen.5 Trotz der Vielzahl an Therapieoptionen ist die Qualität der Versorgung chronischer Psoriasispatienten mit Systemtherapeutika einschließlich Biologika in vielen Ländern Europas unzureichend.6
Problem Langzeitmanagement: Die Chronizität der Erkrankung erfordert eine kontinuierliche Therapie. Durch die Schwere der Erkrankung benötigen viele Patienten mit Psoriasis eine systemische medikamentöse Therapie (Acitretin, Methotrexat, Ciclosporin oder Fumarsäure) bzw. eine Phototherapie (PUVA, Schmalband-UV-B). Die Langzeitbehandlung mit diesen konventionellen Therapien ist in Hinblick auf Kontraindikationen, unerwünschten Nebenwirkungen, Reboundeffekt, Langzeittoxizität und aufwendiger Verlaufskontrollen limitiert. Die Strategie der Entwicklung der Biologika wurde auf die Langzeittherapie der Psoriasis ausgelegt.
Biologika
Biologika sind gentechnologisch erzeugte Proteine. Sie stammen von lebenden Organismen und gehören zur Gruppe der „disease modifying antirheumatic drugs“ (biologic DMARD). Die Hauptindikation der Biologika auf dem Gebiet der Dermatologie stellt die schwere Plaque-Psoriasis dar. Die derzeit für die Behandlung der Psoriasis zugelassenen Biologika sind monoklonale Antikörper oder Fusionsproteine, deren Wirkung sich gegen wichtige proinflammatorische Mediatoren in der Entzündungsreaktion der Psoriasis richtet. Zu diesen gehören die Tumornekrosefaktor-α-Blocker (TNF-α-Blocker) Etanercept (Enbrel®, Zulassung 2004), Infliximab (Remicade®, Zulassung 2005) und Adalimumab (Humira®, Zulassung 2007) sowie der anti-IL12/IL23 Antikörper Ustekinumab (Stelara®, Zulassung 2009).
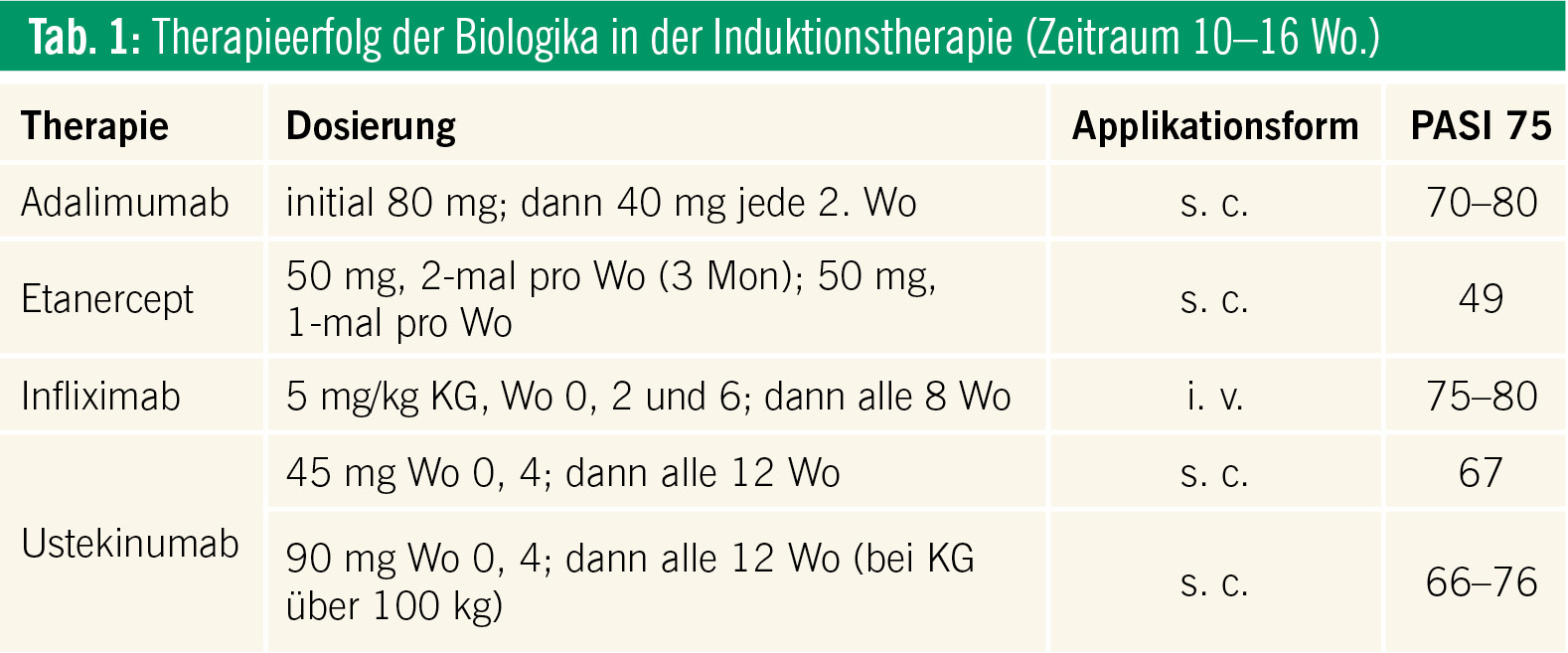
Wirkmechanismen: Der chimäre monoklonale Antikörper Infliximab und der humane monoklonale Antikörper Adalimumab neutralisieren freies und membrangebundenes TNF-α. Zusätzlich führen sie zur Lyse von Zellen, die auf ihrer Oberfläche rezeptorgebundenen TNF-α exprimieren. Das Fusionsprotein Etanercept blockiert die Rezeptorbindung von freiem TNF-α und von Lymphotoxin-α. Der humane monoklonale Antikörper Ustekinumab bindet an die p40-Untereinheit der IL-12- und IL-23-Rezeptoren und blockiert so die IL-12- und IL-23-abhängige Aktivierung und Ausdifferenzierung von Th-1-Zellen (IL-12) und Th-17-T-Zellen (IL-23), die bei der Psoriasis von zentraler pathogenetischer Bedeutung sind. Umfangreiche prospektive, placebokontrollierte, multizentrische Studien auf hohem Evidenzniveau konnten zeigen, dass Biologika in einem kurzen Behandlungszeitraum als Monotherapie eine deutliche Verbesserung des „Psoriasis Area and Severity Index“ (PASI) brachten (Tab. 1).
Langzeitdaten über den Einsatz von Biologika sind spärlich. In einer Erweiterung der Phase-III-Studie REVEAL wurden die Langzeitwirkung und Langzeitsicherheit von Adalimumab untersucht. Diese Studie zeigte, dass die initiale Ansprechrate unter kontinuierlicher Therapie mit Adalimumab über 3 Jahre erhalten blieb.7
In einer kürzlich veröffentlichten Metaanalyse von 20 randomisierten, kontrollierten Studien erwies sich Infliximab als das Biologikum mit der höchsten Wirksamkeit und dem raschesten Ansprechen.8
Die Langzeitwirksamkeit von Etanercept wurde in einer Phase-III-Extensionsstudie über 96 Wochen untersucht. Unter einer Therapie mit 50 mg Etanercept s. c. zweimal wöchentlich erreichten bis zur Woche 96 rund 51 % der Patienten eine 75%ige Reduktion des PASI.9
Die Langzeitdaten aus der PHOENIX-Studie zeigten nach drei Jahren eine kontinuierliche Wirksamkeit von Ustekinumab mit PASI-75-Ansprechraten zwischen 62,7 % (45 mg) und 72,2 % (90 mg)10.
Steuerbare Therapieplanung: Im Falle von Infliximab haben Studiendaten gezeigt, dass die kontinuierliche Therapie in Hinblick auf Wirksamkeit und Sicherheit einer Intervallbehandlung überlegen ist.11 Zusätzlich besteht bei Therapieunterbrechungen bei den monoklonalen Anti-TNF-α-Antikörpern die Gefahr des Wirkverlusts durch neutralisierende Anti-Drug-Antikörper.
Im Gegensatz dazu entsprechen die TNF-α-Bindungsdomänen des humanen TNF-α-Rezeptorfusionsproteins Etanercept weitgehend denen der natürlicherweise im Körper vorkommenden TNF-α-Rezeptoren. Etanercept kann durch sein unterschiedliches immunogenes Profil sowohl in kontinuierlicher als auch in intermittierender Anwendung zum Therapieerfolg führen.12, 13
Kommt es unter der Therapie mit einem bestimmten TNF-α-Blocker zum Wirkverlust, so haben sich in der Praxis unterschiedliche Strategien bewährt. Bevor ein Wechsel auf ein anderes Präparat erfolgt, besteht die Möglichkeit, vorübergehend die Dosis zu steigern bzw. die Dosisintervalle zu verkürzen. Durch die Kombination eines TNF-α-Blockers mit Methotrexat (MTX) in niedriger Dosierung, wie sie in der Behandlung der rheumatoiden Arthritis eingesetzt wird, kann der Antikörperbildung entgegengewirkt werden.14 Weiters kann bei bestimmten Indikationen die Kombination mit MTX oder Acitretin die therapeutische Wirksamkeit steigern.15
Sicherheit: Biologika sind zur Therapie der mittelschweren bis schweren Plaque-Psoriasis dann indiziert, wenn der Patient auf eine andere, konventionelle systemische Therapie nicht angesprochen hat, bzw. wenn eine Kontraindikation oder Unverträglichkeit gegenüber diesen Substanzen besteht.
Obwohl eine Reihe von Studien gezeigt hat, dass Biologika in der kurzzeitigen und mittelfristigen Anwendung nachweisbar sicher sind, müssen Einschränkungen beachtet werden (Tab. 2).
Sicherheitsbedenken: TNF-α hat eine zentrale Position in der angeborenen und erworbenen Immunität. Dies erhöht das Risiko für Tuberkulose und andere schwer verlaufende bakterielle, virale, mykotische und opportunistische Infektionen im Einsatzbereich von TNF-α-Antagonisten. Aus diesem Grund müssen aktive Infektionen vor und während der Behandlung ausgeschlossen bzw. monitiert werden. Im Falle der latenten Tuberkulose gilt, dass eine Therapie mit TNF-α-Blockern erst nach
Behandlung der Infektion beginnen soll. Europäische Register zeigen übereinstimmend, dass eine Behandlung mit den am längsten erprobten Biologika, den TNF-α-Blockern, das Risiko von malignen Erkrankungen nicht erhöht. Allerdings gibt es immer wieder widersprüchliche Daten im Hinblick auf ein erhöhtes Malignomrisiko unter TNF-α-Blockern. Die Beurteilung des Malignomrisikos durch eine Therapie mit Biologika kann somit heute nicht mit letzter Sicherheit erfolgen. In Post-Marketing-Berichten wurde das Auftreten von bisher insgesamt 48 Fällen von Malignomen bei Kindern und Jugendlichen, die TNF-α-Blocker in unterschiedlichen Indikationen erhalten hatten, beobachtet. Die Beurteilung solcher Daten ist schwierig und hängt von vielen Faktoren wie Vortherapien, Grunderkrankung usw. ab. Obwohl kein sicherer Zusammenhang zwischen dem Auftreten dieser Malignome und der Therapie mit TNF-α-Blockern gezeigt werden konnte, wurde von der US Food and Drug Administration (FDA) ein entsprechender Warnhinweis veranlasst.16
Metaanalysen verglichen die Wirksamkeit und Verträglichkeit von TNF-α-Blockern mit konventionellen systemischen Therapien bezüglich unerwünschter Wirkungen. Die Rate an unerwünschten Wirkungen war der Nebenwirkungsrate konventioneller systemischer Therapien ähnlich.17
Nach dem derzeitigen Wissen stellen Biologika bei richtiger Anwendung eine geeignete Behandlungsoption für die mittel- und langfristige Behandlung der stigmatisierenden Erkrankung Psoriasis dar. Dennoch müssen bestehende Sicherheitsbedenken in der Langzeitbehandlung mittels weiterer Studien verfolgt werden.