Aspekte des Langzeitmanagements und der Lebensqualität bei Patienten mit Psoriasis
Psoriasis vulgaris ist eine immunmediierte, entzündliche Erkrankung, die sich in erster Linie an der Haut manifestiert. Die Prävalenz liegt zwischen 1 und 3%. In Deutschland wurde in einer epidemiologischen Studie für das Jahr 2005 eine Prävalenz von 2,5% ermittelt, wobei allerdings nur Patienten, die aufgrund der Psoriasis in ärztlicher Behandlung waren, erfasst wurden.1 Die Psoriasis verläuft meist chronisch-rezidivierend. 60-70% der Betroffenen erkranken vor dem 30. Lebensjahr.
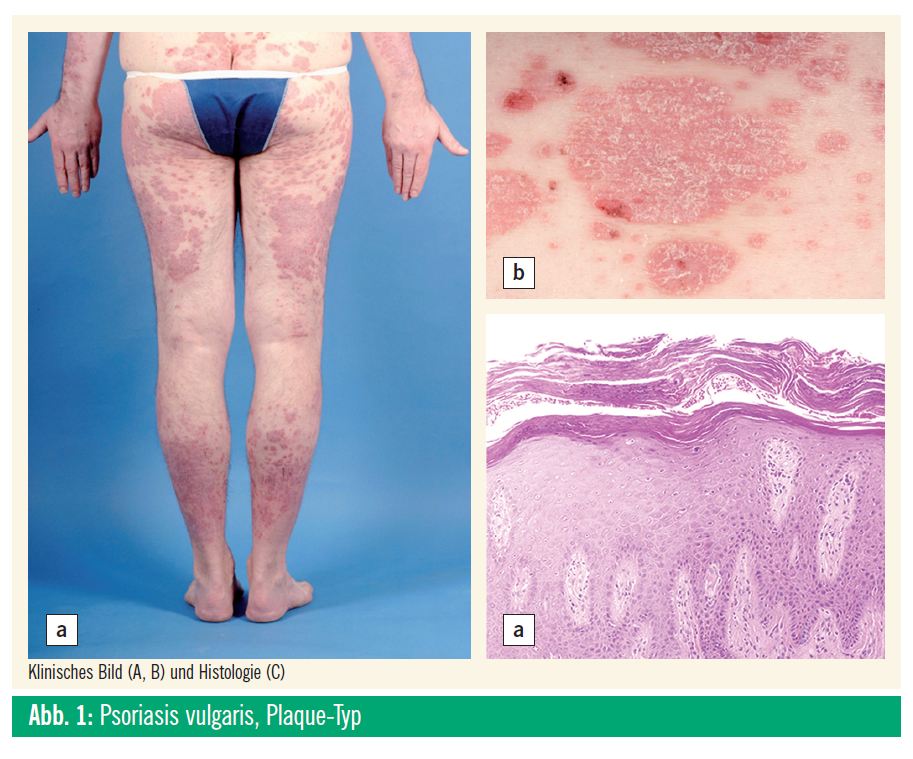
Die klinischen Manifestationsformen der Psoriasis vulgaris sind vielfältig. Am häufigsten tritt sie unter dem Bild der Plaque-Psoriasis mit schuppenden, erythematösen Plaques an den Prädilektionsstellen Knie, Ellbogen und Sakralregion auf. Das klinische Bild sowie Ausdehnung, Dauer und Verlauf können jedoch sehr unterschiedlich sein und reichen von der chronisch-stationären Plaque-Psoriasis über die Psoriasis inversa bis hin zur palmoplantaren Psoriasis und Verlaufsformen mit Gelenk- und Nagelbeteiligung (Abb. 1).
Herausforderung Langzeitmanagement
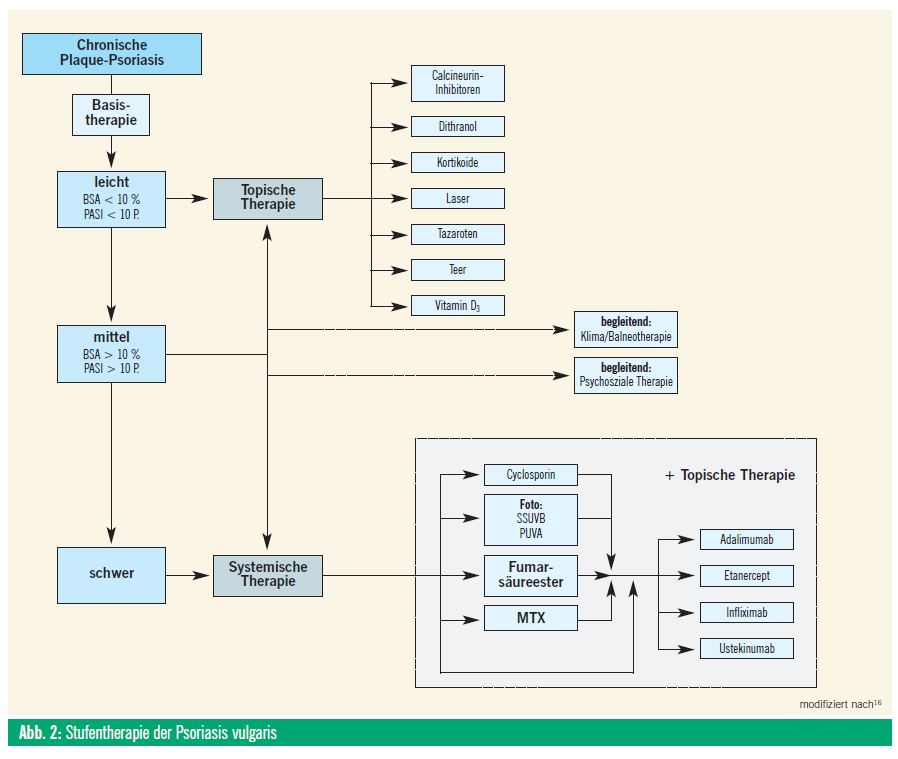
Kontrollierte Daten zur Langzeittherapie der Psoriasis sind leider spärlich. Nationale und internationale Behandlungsrichtlinien empfehlen ein “stufenweises” Vorgehen, abhängig vom Schweregrad der Erkrankung (Abb. 2). Beurteilt wird der Schweregrad nach Ausdehnung und Stärke des Hautbefalls. Zunehmend wird auch die Beeinträchtigung der Lebensqualität in diese Beurteilung miteinbezogen.2
Topische Therapien
Bei leichten Erkrankungsformen kommen topische Therapien mit Klasse-III- und -IV-Steroiden, Vitamin-D-Präparaten, Dithranol und Tazaroten zum Einsatz. Ein Kombinationspräparat aus Calcipotriol und Betamethason war in mehreren klinischen Studien der Therapie mit Monopräparaten überlegen und in einer Langzeitstudie über 52 Wochen sicher und gut verträglich.3
Lichttherapien
Lichttherapien mit UV-B und Photochemotherapien (PUVA-Therapie) waren über lange Zeit die erste Therapiewahl bei mittelschweren und schweren Formen der Psoriasis vulgaris, da sie bei kurzfristiger Anwendung sicher und sehr effektiv sind.
Langzeitrisiko? Argumente gegen eine langfristige Behandlung sind ein hoher Zeitaufwand mit drei bis vier Bestrahlungen pro Woche, vorzeitige Hautalterung und im Falle der oralen PUVA-Therapie ein dosisabhängiges karzinogenes Risiko. Während sich in einer großen Patientenkohorte nach mehr als 100 UV-B-Bestrahlungen innerhalb einer Nachbeobachtungszeit von 5,5 Jahren kein Hinweis auf ein erhöhtes Auftreten von Plattenepithelkarzinomen der Haut zeigte, ist dieses Risiko bei oraler PUVA-Therapie in Abhängigkeit von der Kumulativdosis erhöht. Vortherapien mit PUVA erhöhen das Risiko zur Entwicklung von Plattenepithelkarzinomen vor allem bei jenen Patienten, die Ciclosporin erhalten; diese Therapie ist daher obsolet. Die Daten zum Melanomrisiko durch Langzeit-PUVA-Behandlungen sind kontroversiell und zeigen mit Ausnahme einer Studie keinen Zusammenhang zwischen PUVA-Therapie und einer erhöhten Inzidenz von Melanomen.4 Laut europäischen Richtlinien werden Phototherapien, präferenziell UV-B-Therapien, zur Induktionstherapie der mittelschweren und schweren Psoriasis empfohlen, während sie für die Langzeitbehandlung als ungeeignet eingestuft werden.5
Konventionelle Systemtherapien
Ciclosporin: Von den so genannten “konventionellen” Systemtherapien zur Behandlung der mittelschweren und schweren Psoriasis ist Ciclosporin zur Langzeitbehandlung aufgrund seines Nebenwirkungsprofils nur eingeschränkt geeignet. Die systemische Therapie mit Ciclosporin ist rasch und gut wirksam. Allerdings korreliert die Behandlungs dauer mit dem Auftreten einer meist irreversiblen Nephropathie. Eine arterielle Hypertonie ist eine weitere, häufige Nebenwirkung, die der Nephropathie oft vorangeht. Bei Langzeitbehandlung mit Ciclosporin sollen daher eine Dosis von maximal 3 mg/kg KG und eine Behandlungsdauer von zwei Jahren nicht überschritten werden.5
Fumarsäureester sind in der Langzeitanwendung gut wirksam und sicher. In einer klinischen Studie wurden hierzu Sicherheitsdaten über einen Zeitraum von bis zu 14 Jahren erhoben.6 Nebenwirkungen, vor allem gastrointestinale Beschwerden und Flush-Symptomatik, sind häufig und führen mitunter zum Therapieabbruch.
Methotrexat wird seit Jahrzehnten in der Systemtherapie der Psoriasis und Psoriasis- Arthritis eingesetzt. Kontrollierte Studiendaten zur Langzeitbehandlung fehlen allerdings. Der häufigste limitierende Faktor in der Langzeitanwendung ist die hepatotoxische Wirkung von Methotrexat. Daher sind die Überwachung der Kumulativdosis sowie engmaschige Kontrollen der Leberfunktion durch serologische Tests und bildgebende Verfahren erforderlich. Die Durchführung einer Leberbiopsie vor bzw. während einer Therapie mit Methotrexat sollte nur nach strenger Indikationsstellung erfolgen.7
Biologika
Die Einführung der Biologika in der Psoriasis-Therapie hat sowohl das Therapiespektrum als auch das Verständnis für die Erkrankung erweitert und verändert. Erstmals wurden große, kontrollierte, prospektive klinische Studien zur Wirksamkeit und Verträglichkeit dieser neuen Substanzen durchgeführt. Biologika, die EU-weit in der Indikation Psoriasis zum Einsatz kommen, umfassen die Tumornekrosefaktor-alpha (TNF-α)-blockierenden Medikamente Infliximab, Adalimumab und Etanercept sowie den Anti-IL- 12/IL-23-Antikörper Ustekinumab. So erfolgreich und gut dokumentiert die Wirkung und die Sicherheitsaspekte der Biologika im kurz- und mittelfristigen Einsatz sind, bleibt dennoch die Frage nach Sicherheit und Wirksamkeit im Langzeitmanagement offen. Die Zulassungszeiträume in der Indikation Psoriasis liegen zwischen sieben Jahren (Etanercept; EMEA-Zulassung 2004) und zwei Jahren (Ustekinumab; EMEA-Zulassung 2009). Für diese Zeiträume scheinen die klinischen Daten viel versprechend.8
Neben einem erhöhten Infektionsrisiko standen vor allem Bedenken hinsichtlich eines erhöhten Malignomrisikos im Vordergrund. Nach derzeitigem Wissensstand und Auswertung großer Biologika-Register scheint dieses Risiko allerdings nicht gegeben zu sein. Interessanterweise hat sich gezeigt, dass die Psoriasis selbst, ähnlich wie die rheumatoide Arthritis, mit einem erhöhten Lymphomrisiko einhergeht.
Offene Fragen: Ob Vortherapien wie PUVA oder Ciclosporin ein mögliches erhöhtes karzinogenes Risiko in der Langzeitbehandlung mit Biologika bewirken, ist zur Zeit ungeklärt. Ebenso offen ist die Frage, ob und wie sich eine jahrzehntelange, mitunter lebenslange kontinuierliche Biologika-Therapie, wie sie mit Infliximab, Adalimumab und Ustekinumab vorgesehen ist, auf die genannten Sicherheitsbedenken.
Erhaltungstherapie: Ein weiterer Aspekt ist die Frage nach der Compliance zur Weiterführung einer Therapie bei Patienten, die klinisch erscheinungsfrei sind. Etanercept, das in der Indikation Psoriasis zur Intervallbehandlung zugelassen ist, trägt dieser Überlegung Rechnung.
Studiendaten zeigen, dass bei Patienten mit initial gutem Ansprechen nach Therapiepausen bei neuerlicher Gabe eine vergleichbar gute Wirksamkeit zu erwarten ist. In einer rezenten Studie war Adalimumab bei Patienten nach einer 19-wöchigen Therapieunterbrechung in ähnlichem Maße wirksam wie bei kontinuierlicher Therapie über drei Jahre. In dieser Studie war ein PASI-50 oder weniger mit einem verminderten Ansprechen nach Therapiepause assoziiert. Allerdings war das klinische Ansprechen unabhängig vom Auftreten von Antikörpern gegen Adalimumab.9
Wirkverlust verhindern: Das Phänomen des Wirkverlusts wird in der klinischen Praxis bei allen Präparaten bei einem geringen Teil der Patienten beobachtet. In einer Studie bei Patienten mit Morbus Crohn unter Infliximab-Therapie konnte gezeigt werden, dass die Kombination mit niedrig dosiertem Methotrexat die Entstehung von Anti-Infliximab-Antikörpern vermindert und dass dies mit einem verbesserten klinischen Ansprechen verbunden ist.10 Bislang fehlen prospektive klinische Studien, die der Frage nachgehen, ob bei Psoriasis eine begleitende immunsuppressive Therapie langfristig einen möglichen Wirkverlust verhindert oder ob in jedem Fall bei Wirkverlust ein Therapiewechsel notwendig ist.
Ökonomische Überlegungen
Neben Fragen zur Wirksamkeit und Sicherheit sind es vor allem ökonomische Überlegungen, die das Langzeitmanagement der Psoriasis beeinflussen. Kosten für Kuraufenthalte am Toten Meer werden von den Krankenkassen üblicherweise nicht mehr übernommen. Auch bei den von den Fachgesellschaften und Expertengruppen zusammengestellten Therapierichtlinien spielen neben therapeutische und Sicherheitsaspekte auch ökonomische Überlegungen eine Rolle. Ein Blick auf die direkten Kosten der unterschiedlichen Therapien macht dieses Vorgehen verständlich (s. Tab.). Allerdings schließt dieser Blickwinkel einen wichtigen Aspekt aus, der vor allem im Langzeitmanagement der Erkrankung zum Tragen kommt, und zwar eine über die unmittelbaren Therapiekosten hinausreichende Kosten-Nutzen-Kalkulation einer Behandlung.
| Tab.: Direkte Kosten der Psoriasis-Therapie mit Biologika | ||
|---|---|---|
| Therapie | Dosierung | Preis in US$12,15 |
| Adalimumab | initial 80 mg; dann 40 mg jede 2. Wo | 692,47 |
| Etanercept | 50 mg, 2x pro Wo für 12 Wo; 50 mg/Wo od. 25 mg 2x pro Wo für 12 Wo |
407,18 (50 mg) |
| Infliximab | 5 mg/kg KG Wo 0, 2 und 6; dann alle 8 Wo | 2.324 (60-80 kg KG) 2.905 (80-100kg KG) 4.891,49 (45 mg) |
| Ustekinumab | 45 mg (90 mg) Wo 0, 4; dann alle 12 Wo | 4.891,49 (45 mg) 9.782,97 (90 mg)* |
| * bei Körpergewicht (KG) über 100 kg | ||
QALY und Lebensqualität
Die “Quality-adjusted life year” (QALY) misst die Beeinträchtigung des Patienten durch die Erkrankung, und zwar sowohl qualitativ als auch quantitativ, berechnet den Nutzen, den ein Patient durch ein bestimmtes Medikament in Bezug auf diese Parameter erfahren würde, und wie teuer diese Verbesserung des QALY ausfällt. Es werden daher nicht nur direkt medikamentenbezogene Kosten, sondern auch indirekte Kosten wie Arztbesuche, Krankenstände, zusätzliche Behandlungen usw. in die Berechnung miteinbezogen. So hat eine Studie zur UV-B-Therapie der Psoriasis ergeben, dass die Heimbehandlung, obwohl in den direkten Kosten etwas teurer, der Behandlung beim Arzt überlegen ist, da sie mit einer höheren Lebensqualität und verbesserten Akzeptanz verbunden ist.11 Vergleicht man die QUALY-Berechnungen für die unterschiedlichen Biologika, weisen diese eine weitgehend vergleichbare Kosteneffizienz auf.12-15
Die QALY-Evaluierung zeigt, dass die Fragestellung der Wirtschaftlichkeit und Finanzierbarkeit der Langzeitbehandlung eng mit jener der Lebensqualität verbunden ist. Eine insuffiziente Therapie bedeutet einerseits eine massive Einschränkung der Lebensqualität jedes einzelnen betroffenen Patienten, in dessen Folge Depressionen, Nikotinabusus und übermäßiger Alkoholkonsum auftreten können, andererseits entsteht gerade durch die erwähnten Begleiterscheinungen ein nicht zu unterschätzender volkswirtschaftlicher Schaden.
Wie wichtig ein langfristig gutes Therapiemanagement ist, zeigt eine Studie, die sich mit dem psychosozialen Aspekt der Erkrankung auseinandersetzt. Die Reaktion auf emotionale Gesichtsausdrücke wurde untersucht.
Psoriasis-Patienten zeigten selektiv auf den Ausdruck von Ekel eine reduzierte Wahrnehmung. Dieses Verhaltensmuster war mit einer reduzierten Aktivität in der zerebralen Inselregion assoziiert.
Ergebnisse wie diese belegen, wie tief greifend eine chronische, stigmatisierende Erkrankung das Verhalten der Betroffenen beeinflusst, und sind auch richtungsweisend für das Langzeitmanagement der Psoriasis, das neben Fragen der Wirksamkeit, Sicherheit und Kosten einer Behandlung auch die Lebensqualität der Betroffenen umfassen muss.
1 Schäfer I, Rustenbach SJ, et al., Epidemiology of Psoriasis in Germany – Analysis of Secondary Health Insurance Data. Gesundheitswesen 2010 Jun 11 (Epub ahead of print)
2 Finlay AY. Current severe psoriasis and the rule of tens. Br J Dermatol 2005; 152(5): 861-7
3 Van de Kerkhof PC, Barker J, et al., Psoriasis: Consensus on topical therapies, J Eur Acad Dermatol Venereol 2007; 22: 859-870
4 Menter A, Korman NJ, et al., Guidelines of care for the management of psoriasis and psoriatic arthritis: Section 5. Guidelines of care for the treatment of psoriasis with phototherapy and photochemotherapy. J Am Acad Dermatol 2010; 62(1): 114-35
5 Pathirana D, Ormerod AD, et al., European S3-Guidelines on the systemic treatment of psoriasis vulgaris. JEADV 2009: 23: Suppl. 2
6 Hoefnagel JJ, Thio HB, et al., Long-term safety aspects of systemic therapy with fumaric acid esters in severe psoriasis. Br J Dermatol 2003; 149: 363-369
7 Barker J, Horn EJ, et al., Assessment and management of Methotrexate hepatotoxicity in psoriasis patients: Report from a consensus conference to evaluate current practice and identify key questions toward optimizing Methotrexate use in the clinic. JEADV 2011; 25 (Epub ahead of print)
8 Van Lümig P, Driessen R, et al., Safety of treatment with biologics for psoriasis in daily practice: 5-year data. J Eur Acad Dermatol Venereol 2011 Mar 24 (Epub ahead of print)
9 Gordon K, et al., Efficacy and safety in patients with psoriasis treated continuously with Adalimumab for approximately 3 years. EADV 2010, Goteborg, Sweden, P592
10 Vermeire S, Noman M, Van Assche G, et al., Effectiveness of concomitant immunosuppressive therapy in suppressing the formation of antibodies to Infliximab in Crohn’s disease. Gut 2007; 56(9): 1226-31
11 Koek MBG, Sigurdsson V, et al., Cost effectiveness of home ultraviolet B phototherapy for psoriasis: Economic evaluation of a randomised controlled trial (PLUTO study) BMJ 2010; 340: c1490
12 Anis AH, Bansback N, et al., Economic evaluation of biologic therapies for the treatment of moderate to severe psoriasis in the United States. Journal of Dermatological Treatment 2011; 22: 65-74
13 Knight C, Mauskopf J, et al., Cost-effectiveness of treatment with Etanercept for psoriasis in Sweden. Eur J Health Econ. 2011 Mar 6 (Epub ahead of print)
14 Rodgers M, Epstein D, et al., Etanercept, Infliximab and Adalimumab for the treatment of psoriatic arthritis: A systematic review and economic evaluation. Health Technol Assess 2011 Feb; 15(10): i-xxi, 1-329
15 Martin S, Feldman SR, et al., Cost per responder analysis of Ustekinumab and Etanercept for moderate to severe plaque psoriasis. J Dermatolog Treat 2011 Jan 22 (Epub ahead of print)
16 Nast A, Augustin M, et al., S3-Leitlinie zur Therapie der Psoriasis vulgaris – Update: Übersicht der Therapieoptionen und Efalizumab. JDDG 2010; 8: 65-66