Vesikulobullöse und pustulöse Dermatosen im Kindesalter
Die Haut ist unser mechanistisches, physikalisches und antibakterielles Schutzschild, das den Menschen u. a. auch vor Flüssigkeitsverlust und Austrocknung bewahrt. Die Haut von Säuglingen und Kleinkindern weist eine höhere Verletzbarkeit, Sonnenempfindlichkeit und Empfindlichkeit gegenüber Irritation im Vergleich zu Jugendlichen und insbesondere zu Erwachsenen auf. Kinder präsentieren sich daher häufig mit Bläschen, Pusteln, Blasen. Diese können eine primäre blasenbildende Hauterkrankung, aber auch Zeichen systemischer Erkrankungen sein und oft differenzialdiagnostische Herausforderungen darstellen.
Differenzialdiagnostische Überlegungen
Bei Begutachtung dieser Erkrankungen sind folgende Überlegungen, Merkmale und Entscheidungen relevant, nachdem man das Kind komplett ausgezogen und es von Kopf bis Fuß angeschaut hat: Manifestationsalter, Höhenlage der Blasen in der Haut (subkorneal, intraepidermal oder dermoepidermal), schlaffe oder pralle Blasen, direkte oder indirekte Nikolski-Zeichen auslösbar oder nicht, Lokalisation der ersten Blase, Verteilung, Größe und Konfiguration der Blasen (vereinzelt, generalisiert, gruppiert, entlang von Dermatomen). Sind Schleimhäute, Haare, Hautanhangsgebilde betroffen? Bestehen Juckreiz, Fieber, andere Systemzeichen? Gibt es eine Infektanamnese beim Kind, in der Familie, im Freundeskreis? Sind Impfungen vorausgegangen? Liegen eine Familienanamnese bezüglich blasenbildender Dermatosen sowie Konsanguinität vor? Essenziell ist auch die Unterscheidung zwischen einer harmlosen Erkrankung oder einem akut lebensbedrohlichen Zustand, weiters die Frage: erworben oder angeboren? Kann ich selber abklären und behandeln, oder muss das Kind hospitalisiert bzw. an ein spezialisiertes Zentrum zugewiesen werden?
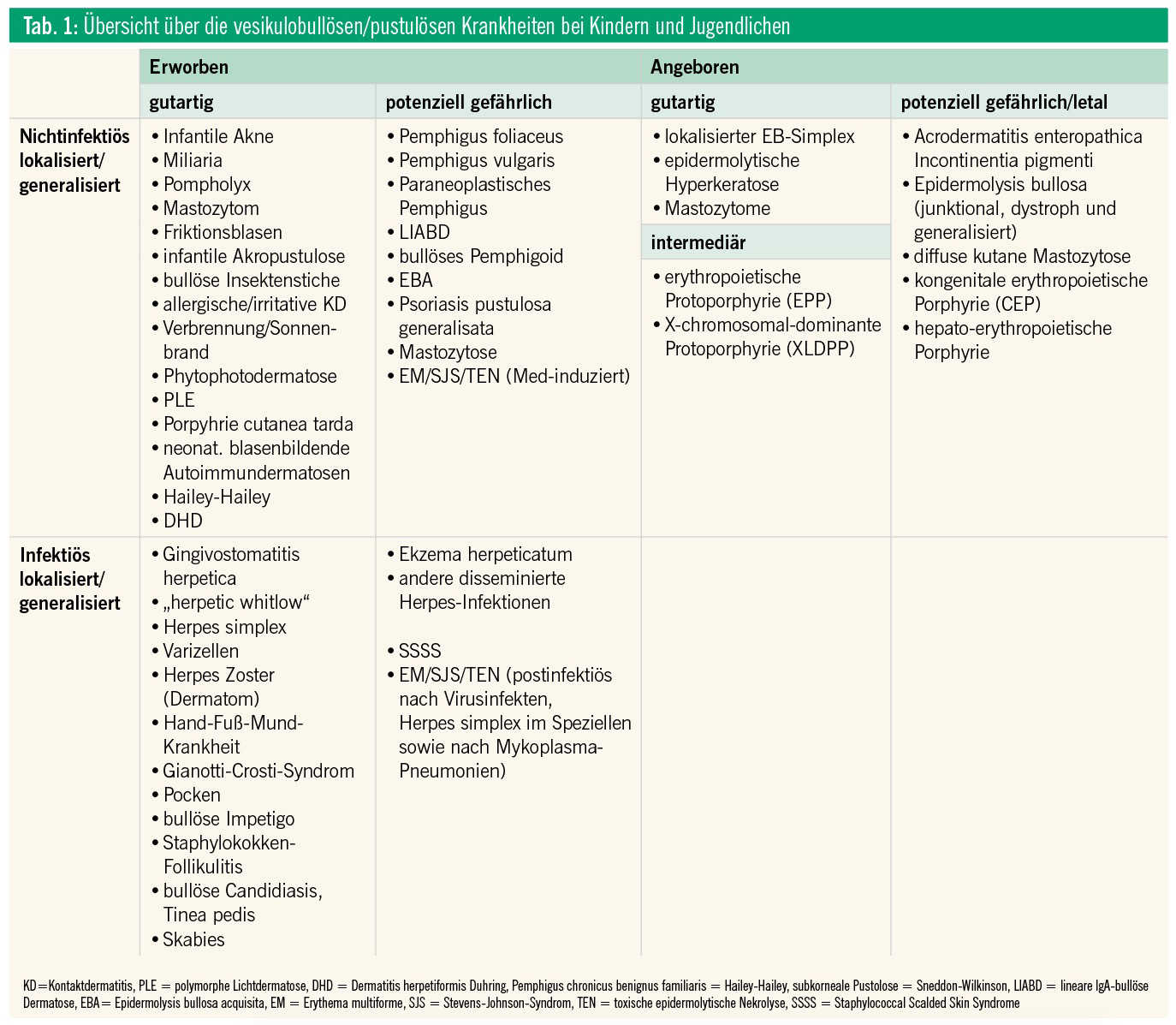
Tabelle 1 gibt eine Übersicht über die wichtigsten Differenzialdiagnosen der Blasen-und pustelbildenden Erkrankungen im Kindesalter, eingeteilt nach Kausalität und Dignität.
Diagnostik
Diagnostische Maßnahmen ergeben sich aus den erwogenen Differenzialdiagnosen. Diese sind bei infektiösen Erkrankungen bakterielle Abstriche und Kulturantibiogramm, KOH und Pilzkulturen, Skabies- Diagnostik, Tzanck-Test, PCR aus Abstrichen, bakterielle Kulturen aus peripherem Blut, Virus-Serologie, Lues-Serologie und Endotoxin-Bestimmungen.
Bei unklaren Dermatosen und Verdacht auf autoimmunbullöse Krankheiten und Genodermatosen stellt die Stanzbiopsie trotz Invasivität die Methode der Wahl dar, und zwar in jedem Alter. Diese wird in den allermeisten Fällen für eine Histologie (H&E-Färbung, bei Bedarf PAS und andere Färbungen), direkte Immunfluoreszenz, bei Bedarf Salt-Split-Technik zur Lokalisation der Blasenbildung in der Basalmembranzone, Immunfluoreszenz-Antigen-Mapping und Elektronenmikroskopie bei Verdacht auf Epidermolysis bullosa sowie Immunhistochemie eingesetzt. Zur Diagnostik von Genodermatosen und Beratung zur weiteren Familienplanung werden genetische Testungen aus EDTA-Blut durchgeführt. Hierbei kann nach einem bekannten Gendefekt bei bestimmten vererbbaren Erkrankungen gesucht werden. Bei negativem Test bzw. nicht bekannter Mutation werden Next-Generation-Sequencing-Techniken zur Entdeckung neuer Gene beim Patienten und bei den Eltern eingesetzt.
Blasenbildende Dermatosen in Bildern
Die Bildtafel zeigt eine Auswahl klinischer Bilder der häufigsten blasen-/pustelbildenden Dermatosen bei Säuglingen und Kindern:
Infantile Akne, infantile Akropustulose, Miliaria (rubra, cristallina – je nach epidermaler Höhe), vereinzelte Mastozytome (Bild 1–5) – diese können bei Säuglingen und Kleinkindern aufgrund der noch schwachen dermoepidermalen Verankerung bei Mastzelldegranulation (Darier-Test) mit Blasenbildung reagieren; Pompholyx, allergische/ irritative Kontaktdermatitis mit scharf begrenzten Erosionen, Windelsoor (Bild 6 und 7) – einzelne juckende oberflächliche Pusteln auf erythematösem Grund, die leicht platzen und randständige Schuppung bilden, stellen die häufigsten blasenbildenden Dermatosen dar, gefolgt von bullöser Impetigo contagiosa (Bild 8–12) – erythematöse, anfangs wie Insektenstiche imponierende, erosive, krustöse sowie bullöse Läsionen, die sich als bakterielle Schmierinfektion durch Kratzen auf gesunde Haut übertragen lassen, meist durch Staphylococcus aureus (großblasige Impetigo), gefolgt von Streptokokken (kleinblasig).
Sie alle sind selbstlimitiert bzw. heilen unter entsprechender Therapie (lokal, systemische Antibiose oder antimykotische Therapie) rasch ab. Ein bakterielles, akut lebensbedrohliches und daher gefürchtetes Krankheitsbild ist das Staphylococcal Scalded Skin Syndrome (SSSS, Dermatitis exfoliativa), ausgelöst durch die epidermolytischen Toxine A und B von toxin-bildenden Staphylokokkenstämmen. Die Haut ist schmerzhaft und diffus rot, die Hornschicht schwimmt bereits beim geringsten Ankommen ab (direktes Nikolski-Zeichen positiv) und hinterlässt ein verbrühtes Aussehen – Auftreten meist nach Angina oder Otitis. Eine rasche Behandlung mit i. v. Penicillinen rettet Leben.
Die Bilder 13–15 illustrieren typische Veränderungen an Kinderfingern, darunter eine durch chronisches Lutschen auftretende Impetigo am Daumen (Bild 13) sowie eine typische Herpes-simplex-Infektion am Finger (Bild 14), man sieht auf erythematösem geschwollenem Grund zahlreiche einzelne Bläschen mit klarem oder trübem Blaseninhalt, bei bakterieller Superinfektion entsteht daraus das pustulöse „herpetic whitlow“ (herpetischer Finger) (Bild 15). Tritt Herpes simplex auf atopischer Haut auf, kann es zu disseminiertem Herpes kommen. Bild 16 zeigt ein superinfiziertes Ekzema herpeticatum bei einem Kind mit atopischer Dermatitis, das antivirale und antibiotische i. v. Therapie erfordert. Die Bilder 17–23 zeigen, wie unterschiedlich sich bakterielle Superinfektionen manifestieren können: Die schlaffe Blase auf gesunder Haut am Ellbogen lässt als Primärläsion eine Impetigo vermuten (Bild 17), bei genauer Betrachtung des gesamten Integuments sieht man große herabhängende eitrige Blasen mit dazwischen verteilten kleinen Papeln, Pusteln, ausgestanzt wirkenden Ulzera und Nekrosen. Die Diagnose lautet Varizellen mit S. aureus-Superinfektion bei einem atopischen Kind (Bild 18). Auch Herpes Zoster ist bei Kleinkindern und Jugendlichen ein häufiges Phänomen (Bild 19 und 20), wie auch die Hand-Fuß-Mund- Krankheit, die sich neben Fieber mit palmoplantaren Bläschen sowie Bläschen im Mund und Rachen manifestiert (Bild 21–23). Sie ist eine Tröpfcheninfektion, die durch Coxsackie-A-Viren oder Enterovirus 71 ausgelöst wird. Die wichtigste Differenzialdiagnose der palmoplantaren Bläschen und Pusteln bei Säuglingen und Kleinkindern ist nach wie vor die Skabies (Bild 24).
Disseminierte stecknadelkopfgroße Pusteln auf erythematöser Haut oder gruppierte subkorneale Pusteln auf erythematösen Plaques sind auch bei Kindern verdächtig für Psoriasis pustulosa (Bild 25 und 26). Die generalisierte akute Form kann lebensbedrohlich sein und eine stationäre Aufnahme bis zur Therapieeinstellung erforderlich machen. In hartnäckigen Fällen müssen neben Lokaltherapien auch bei Kleinkindern Methotrexat oder Cyclosporin A, bei Jugendlichen auch Acitretin und NB-UVB oder PUVA in Erwägung gezogen werden.
Ein eigenes Kapitel stellen die äußerst seltenen, oft letalen oder schwerwiegenden hereditären bullösen Erkrankungen dar (Bild 27–30), die in dermatologischen Abteilungen bzw. eigenen Zentren diagnostiziert und behandelt werden. Auf sie kann hier nicht im Detail eingegangen werden. Wichtig ist, bei Geburt mit fehlender Haut, Nageldystrophie oder blutigen rezidivierenden Blasen daran zu denken und das Kind entsprechend zuzuweisen.
Eine weitere seltene hereditäre Erkrankung, die mit Blasen einhergeht, ist die X-linked Incontinentia pigmenti (Bloch- Sulzberger-Syndrom; Bild 31). Sie ist bei männlichen Föten meist letal, bei Mädchen unterschiedlich ausgeprägt und weist 4 Phasen der Hautmanifestation auf: papulös, bullös, verrukös, hyper- und/oder hypopigmentierte Phasen, die sowohl aufeinander folgen als auch simultan vorliegen können. Wichtig und problematisch sind zerebrale, okuläre, muskuloskeletale und immunologische Manifestationen, sodass diese Neugeborenen einer multidisziplinären Durchuntersuchung unterzogen werden müssen.
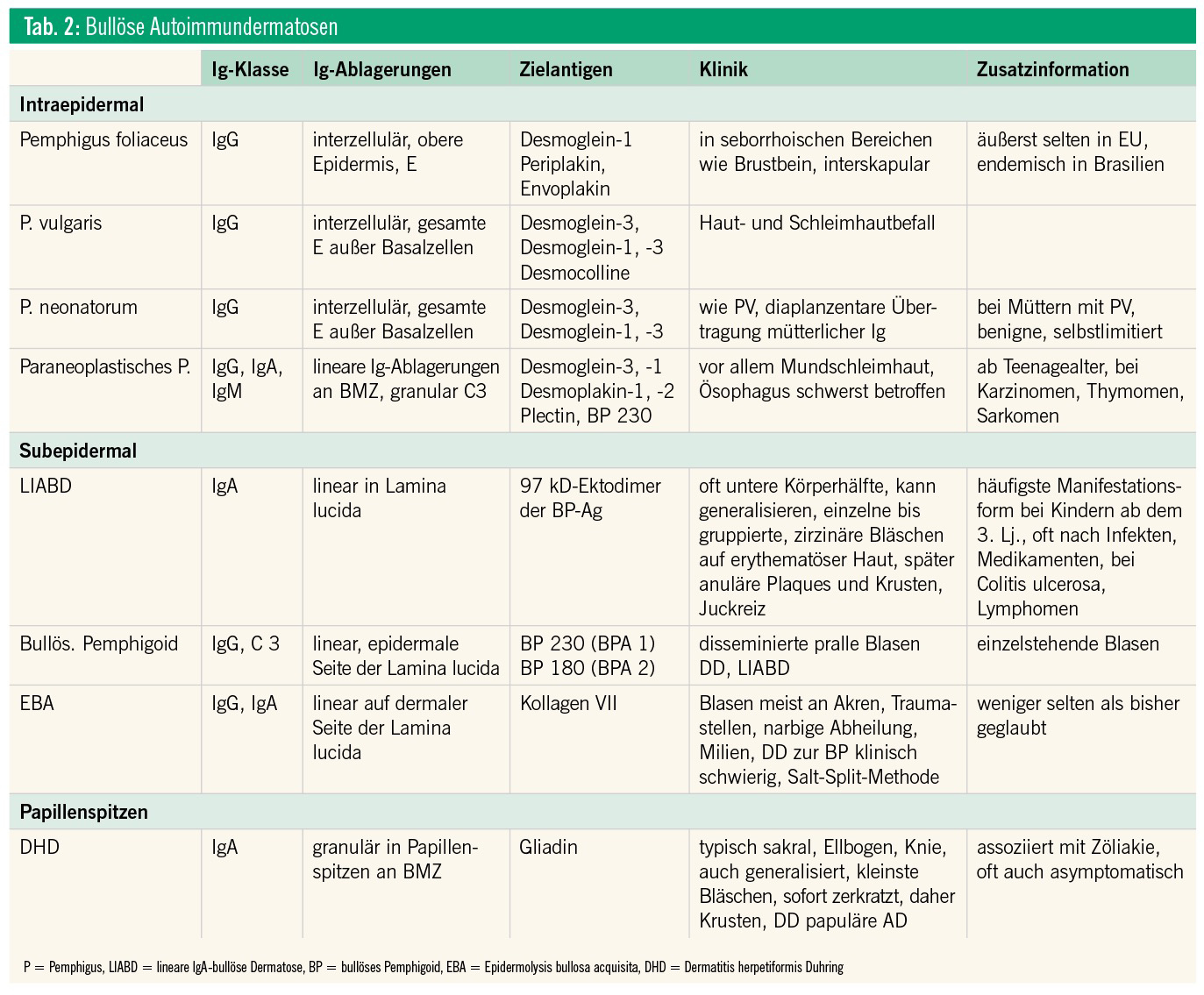
Bullöse Autoimmundermatosen sind im Kindesalter und bei Jugendlichen in der Regel selten, stellen jedoch die wichtigsten Differenzialdiagnosen der infektiösen blasenbildenden Krankheiten dar. Die Blasen befinden sich je nach Erkrankung intraepidermal (schlaffe Blasen, Nikolski-I-positiv) oder im Bereich der Basalmembranzone (pralle Blasen, Nikolski-II-positiv; indirekte Form). Die spezifischen Merkmale der einzelnen Krankheitsbilder sind in Tabelle 2 zusammengefasst, dazugehörige klinische Bilder finden sich in der Abbildung (Bild 32–40).
Aufgrund der Klinik sowie der histologischen, Immunfluoreszenz-und immunserologischen Befunde kann die Diagnose rasch gestellt und die adäquate Therapie eingeleitet werden. Therapie der Wahl bei Dermatitis herpetiformis Duhring (DHD) und der linearen IgA-bullösen Dermatose (LIABD) ist das Sulfonamidderivat Dapson – soweit der Betroffene keinen Glukose-6-Phosphat-Dehyrogenase-(G6PD-)Mangel aufweist, bei LIABD zusätzlich systemisches Kortison. Der Ausschluss einer G6PD-Defizienz vor Therapiebeginn ist zwingend, da es bei entsprechendem Mangel unter Dapson zu lebensbedrohlicher Hämolyse und Methämoglobinbildung kommen kann. Nach Besserung wird bei LIABD das Kortison ausgeschlichen und Dapson über 1–2 Jahre weiter verabreicht, bei DHD ist Dapson eine lebenslange Therapie. Zum Therapie-Monitoring bei LIABD eignet sich die Bestimmung der IgA-Titer im Serum (indirekte Immunfluoreszenz).
Bei allen anderen bullösen Autoimmundermatosen (Pemphigus vulgaris [PV], bullöses Pemphigoid [BP] und Epidermolysis bullosa acquisiata [EBA]) bestand die klassische Therapie bis vor kurzem aus einer Kombination von hochdosiertem systemischem Kortison und Immunsuppressiva wie Azathioprin oder MTX – trotz möglicher Nebenwirkungen wie Infektionen, Sepsis, Entwicklungsstörungen, Kachexie etc. Seit 2017 ist bei PV die Therapie der ersten Wahl Rituximab (Anti-CD-20-Antikörper) mit oder ohne initiale, kurzzeitige systemische Kortisongabe. Das Biologikum eignet sich vom Prinzip für alle anderen bullösen Autoimmunkrankheiten mit Antikörperbildung. Allerdings gibt es bei BP, assoziiert mit Eosinophilie und erhöhter IL-4/IL- 5-Produktion, sehr positive Berichte zum Einsatz von Omalizumab (Anti-IgE-Antikörper) und Dupilumab (Anti-IL-4-Antikörper), welche ein günstigeres Nutzen-Risiko-Verhältnis aufweisen. Das Erstgenannte ist zugelassen für Asthma bei Kindern ab 6 Jahren, Zweiteres bei atopischer Dermatitis ab 12 Jahren, wobei Studien bei jüngeren Kindern laufen.
Bilder nur in der Print-Ausgabe verfügbar. Wir bitten um Verständnis.