Ambulant erworbene Pneumonie – ein Update
Theoretisch gibt es eine Unzahl von Mikroorganismen, die Infektionen der tiefen Atemwege, darunter die Pneumonie, verursachen können. Praktisch entscheidet die Umgebung, in der sich der Patient befindet, welche Erreger tatsächlich wahrscheinlich sind.
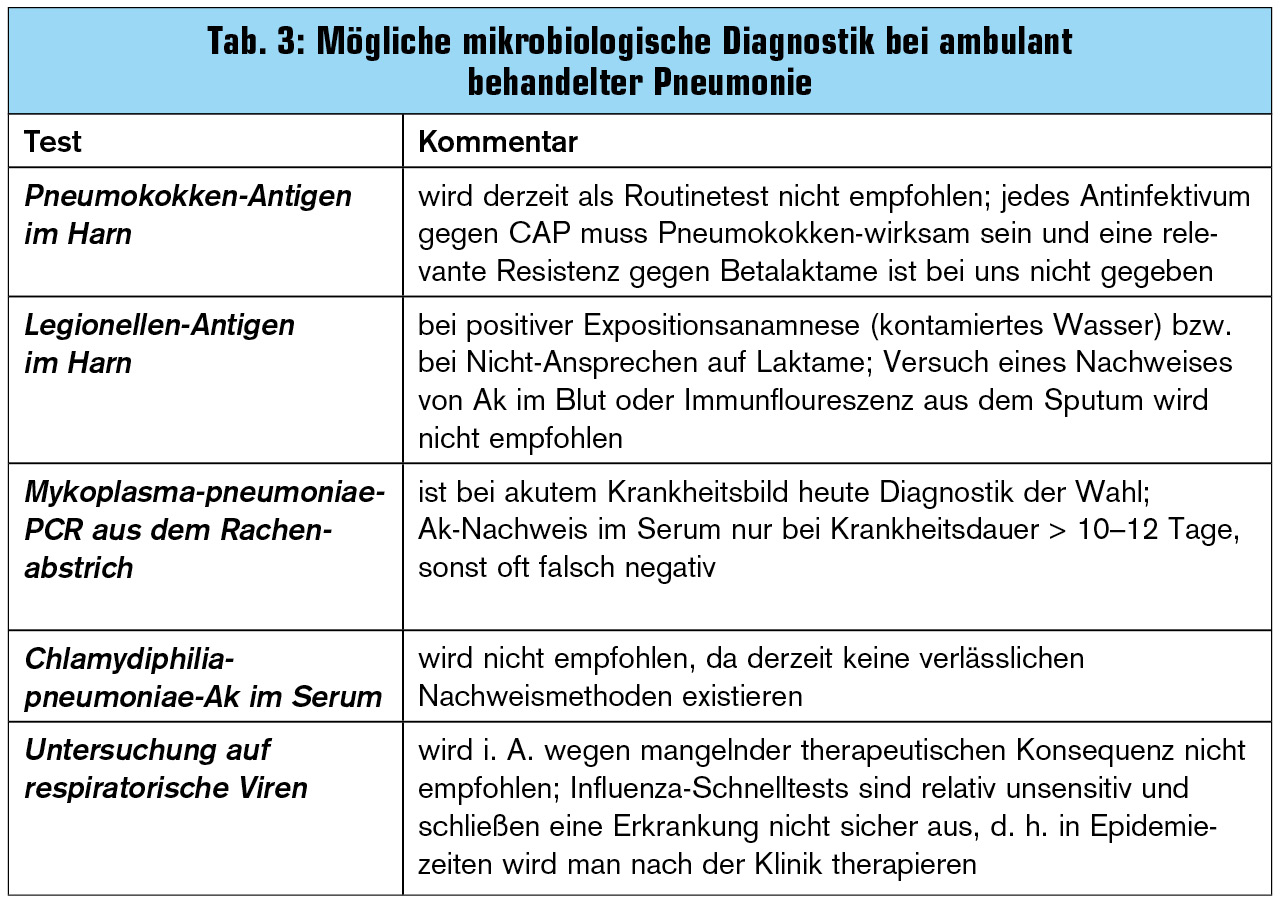
Erregerkalkül: Aus diesem Konzept heraus haben sich verschiedene Pneumoniedefinitionen entwickelt: beginnt die Erkrankung während eines Spitalsaufenthaltes („hospital-acquired“) oder an der Intensivstation („respirator-associated“) oder ist sie außerhalb des Spital erworben – mit („healthcare-associated“) oder ohne regelmäßigen Kontakt zu Gesundheitseinrichtungen („community-acquired“, CAP). Da ein direkter Erregernachweis bei Pneumonie in bis zu 40 % der Fälle auch in Spital und unter Studienbedingungen nicht gelingt und beim Hausarzt auch gar nicht versucht werden sollte, helfen diese Begriffe, die möglichen Erreger zu kalkulieren und die Therapie zu gestalten (Tab. 1 und 2). Darüber hinausgehende diagnostische Überlegungen wie Tierkontakte (Psittakose, Q-Fieber), Reiseanamnese oder Kontakt mit kontaminiertem Wasser (Legionellosen) spielen erfahrungsgemäß beim nur leicht Erkrankten keine Rolle.
Resistenzkalkül: Neben der Frage, welche Erreger in Frage kommen, ist natürlich von Interesse, ob die einzelnen Erreger auch gegen die üblichen Antiinfektiva resistent geworden sein könnten. Von einer erhöhten Wahrscheinlichkeit einer Resistenz ist dann auszugehen, wenn der Patient in den letzten 3 Monaten mit Antiinfektiva therapiert wurde, in einer Langzeitpflegeeinrichtung untergebracht ist oder aufgrund chronischer Morbidität wiederholt in Spitäler aufgenommen war. Generell ist aber im deutschsprachigen Raum die Resistenzsituation bei Pneumokokken, die ja die wichtigsten bakteriellen Pneumonieerreger gegen Betalaktamen sind sehr gut (2–6 % der Stämme intermediär empfindlich oder resistent, Resistenzen gegen Makrolide sind möglich (11–18 % resistent) und gegen Tetrazykline vergleichsweise niedrig (7–11 % resistent) (Daten aus CAPNETZ, 2009).
Zweckmäßige Diagnostik: Neben einer gründlichen klinischen Untersuchung und dem Lungenröntgen in 2 Ebenen gibt es wenig Evidenz für die Zweckmäßigkeit weiterer, vor allem mikrobiologischer Diagnostik wie Abnahme von Sputum- oder Blutkulturen beim Hausarzt: Die Notwendigkeit einer Untersuchung auf Biomarker wie C-reaktives Protein oder Procalcitonin (PCT), letzteres allein schon aus Kostengründen, ist umstritten. Ein negatives CRP bei einem schon > 24 Stunden kranken Menschen macht die Diagnose einer bakteriellen Pneumonie sehr unwahrscheinlich; auch für den Einsatz von PCT, um rascher die antiinfektive Therapie beenden zu können, gibt es Literatur. Provokant formuliert: Wer setzt bei einem akut kranken, hoch fiebernden Patienten mit klassischem Infiltrat tatsächlich das Antibiotikum ab, weil das CRP/PCT negativ ist? Die Bestimmung von Blutbild und Nierenfunktionsparameter werden von den Guidelines empfohlen, letztere ja auch, weil erhöhte UUN/BUN-Werte auf einen komplizierteren Verlauf deuten.
Überlegungen zur Spitalseinweisung: Nach der Diagnose gilt es das Risiko von Komplikationen und damit die Notwendigkeit einer eventuellen Spitalseinweisung abzuschätzen. Bei Patienten unter 65 Jahren sind COPD, Diabetes mellitus, vorbestehende Herzerkrankungen, die Gabe systemisch wirksamer Kortikoide, fortgeschrittene Nieren-/Leberinsuffizienz, Malignome und Immunsuppression, Spitalsaufnahmen im letzten Jahr und rezente Antiinfektivagabe klassische Risikofaktoren für Komplikationen oder Therapieversagen zu werten. Neben diesen Parametern, die im Einzelfall oft schwer zu gewichten sind, haben sich in den letzten Jahren für die Patienten > 65 Jahren Risikoscores etabliert, deren einfachster, weil rein klinisch zu überprüfen, der CRB-65-Score ist: Circulation mit diastolischem RR ≤ 60 mmHg respektive systolischem RR < 100 mmHg, Respiration mit Atemfrequenz ≥ 30/min; Bewusstsein d. h. akut und neu aufgetretene ZNS-Funktionsstörung/-einschränkung und dazu ein Alter ≥ 65, letzteres zählt aber allein genommen nicht als Grund für die Spitalseinweisung. Bei einem CRB-65 von 0 ist von einem sehr geringen Komplikationsrisiko auszugehen (Sterblichkeit 19 mg/dl), wobei 0–1 Punkte für eine ambulante Therapie sprechen, bei 2 Punkten ist von einer kurzzeitigen stationären Beobachtung, z. B. an einer Notfallaufnahmestation, und bei 3–5 Punkten von einer schweren Pneumonie auszugehen. In diese Überlegungen fließt natürlich ein, dass der Erkrankte eine ausreichend häusliche Betreuung hat und unabhängig von der Ausgangssituation legt ein Nichtansprechen auf 2–3 Tage Antibiotikagabe die Spitalseinweisung nahe.
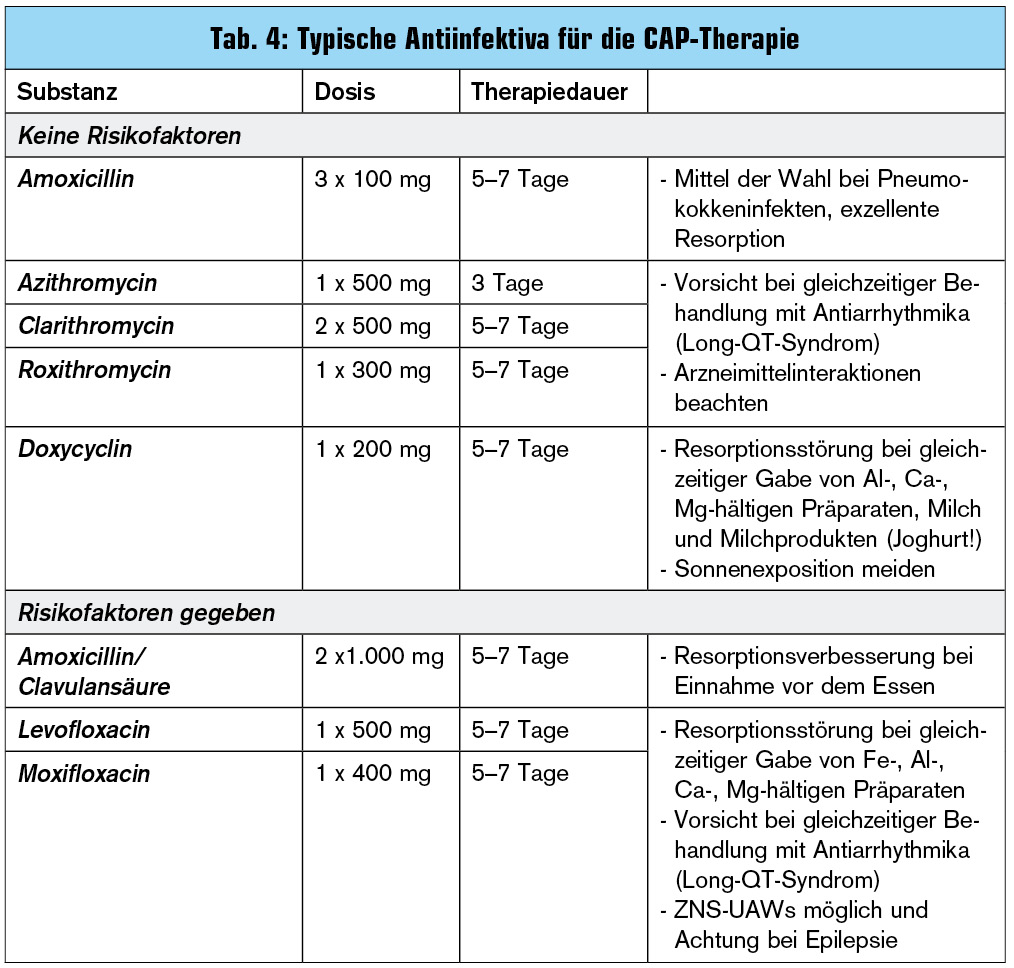
Für die Behandlung der CAP steht eine Reihe von im Allgemeinen gut verträglichen und oral verabreichbaren Antiinfektiva zur Verfügung, deren Einsatz sich am Vorliegen von Resistenzrisiken (Langzeitpflege, Spitalsaufenthalte etc.) richtet (Tab. 4). Zugelassen für die Therapie von Infekten der tiefen Atemwege sind auch Oralcephalosporine wie Cefuroxim und Cefpodoxim, sollten aber in Hinblick auf deren schlechte Resorption und die aktuelle Problematik mit zunehmend resistenten Enterobakterien (ESBL-Bildner) mit Zurückhaltung verordnet werden.
Für Patienten, die mit CAP eine Notfallaufnahmestation aufsuchen, gibt es einige Publikationen, die das Ergebnis des Managements der Erkrankung von der Zeit zwischen Vorstellung des Patienten und erster Antibiotikagabe (maximal 4–8 Stunden) abhängig sehen. In einigen Ländern wurde diese Zeitspanne als Qualitätsindikator akzeptiert und mit der Refundierung der Behandlungskosten assoziiert. Für den niedergelassenen Bereich scheint dieser Aspekt keine Rolle zu spielen: abgesehen der Tatsache, dass niemand die Zeitspanne zwischen Arztbesuch und Beschaffung der Medikamente in der Apotheke beeinflussen kann, korreliert auch die Dauer bis zur klinischen Stabilisierung nicht mit diesem Parameter. Derartige Überlegungen sollten daher im niedergelassenen Bereich keine Rolle spielen, noch dazu, da bekannt ist, dass die Angst, eine Pneumonie zu „übersehen“, die Neigung zu unnötiger Antibiotikagabe signifikant erhöhen kann.
Für die Behandlung von Patienten, denen eine orale Therapie ad hoc nicht zumutbar ist, stehen eine Reihe von 1-mal-täglich zu verabreichenden Antiinfektiva zur Verfügung, auch wenn diese gegenwärtig nicht zur Standardtherapie im niedergelassenen Bereich gehören – dies letztlich aber nur aus Gründen der Refundierung: Ceftriaxon 1 x 1–2 g, Ertapenem (Invanz®) 1 x 1 g, Levofloxacin (Tavanic®) 1 x 500 mg, Moxifloxacin (Avelox®) 1 x 400 mg, Doxycyclin (Vibravenös®) 1 x 200 mg, Azithromycin (Zithromax®) 1 x 500 mg.
Erfahrungsgemäß erreichen drei Viertel der CAP-Patienten mit dem 3 Therapietag eine Situation der klinischen Stabilität, sind fieberfrei und die Klinik hat sich signifikant gebessert; die antibiotische Therapie kann dann 48–72 Stunden nach Abfiebern, man sagt frühestens nach 5 Tagen, beendet werden. Eine Therapiedauer über 7 Tage ist nicht nötig, die oft geübte Praxis, jedes verordnete Antibiotikum über mindestens 10 Tage zu „vollenden“, sollte aufgegeben werden. Ein Nichtansprechen legt die Spitalseinweisung nahe.
Eine radiologische Nachkontrolle 2 Wochen nach Ende der Antibiotikatherapie wird in den Guidelines empfohlen, um bei Patienten > 60 Jahre und/oder Rauchern eine nicht-infektiöse Ursache für die Infektion, z. B. Bronchuskarzinom, auszuschließen. Empfehlenswert ist es, Patienten nach Mittellappenpneumonie dem Lungenfacharzt vorzustellen.
In Hinblick auf die Prävention fordern alle Fachgesellschaften in ihren Guidelines das Angebot einer Impfung gegen Pneumokokken bei allen Patienten > 65 Jahre und die jährliche Auffrischung der Influenzaimpfung bei allen > 50 Jahre sowie Familienmitgliedern oder Kontaktpersonen (auch Mitarbeiter des Gesundheitswesens) von Patienten bei denen ein erhebliches Risiko von Influenzakomplikationen besteht, bzw. allen Patienten unabhängig vom Alter mit chronischen Herz-Kreislauf- oder Lungenerkrankungen.