APOSEC – Neuer Therapieansatz in der Behandlung des Herzinfarkts
K. Hoetzenecker1, A. Assinger2, M. Gyöngyösi3, I. Volf2, H. J. Ankersmit1
1 Klinische Abteilung für Thoraxchirurgie, Christian-Doppler-Labor für Diagnose und Regeneration von Herz- und Thoraxerkrankungen, Medizinische Universität Wien
2 Institut für Physiologie, Medizinische Universität Wien
3 Klinische Abteilung für Kardiologie, Medizinische Universität Wien
Hintergrund
Weltweit sterben jährlich ca. 7,2 Millionen Menschen an den Folgen eines akuten Herzinfarkts und die ischämischen Herzerkrankungen werden global als die häufigste Todesursache in einer aktuellen Erhebung der WHO angeführt. In den letzten Jahren ist es gelungen, durch eine Verbesserung des Versorgungsnetzes und eine sofortige Wiedereröffnung der okkludierten Koronararterie die frühe Sterblichkeit des Herzinfarkts zu verringern. Trotz dieser schnellen Wiederherstellung des koronaren Blutflusses kommt es in bis zu 50 % aller Patienten zu einer persistierenden Minderversorgung des Herzmuskels mit Sauerstoff und zu einem „Nachbrennen“ des myokardialen Schadens. Der Grund dafür ist die so genannte mikrovaskuläre Obstruktion (MVO). Die genauen Ursachen der MVO sind noch nicht vollständig geklärt, wichtige Faktoren in der Entstehung der MVO sind Thrombozyten, Abwehrzellen und eine Engstellung der kleinen Blutgefäße.
Die Forschungsgruppe rund um Assoc. Prof. Univ.-Doz. Dr. Hendrik Jan Ankersmit konnte in früheren Studien zeigen, dass die Verabreichung von APOSEC den Schaden nach einem Herzinfarkt in einem Großtiermodell signifikant verringert.1–3
APOSEC ist ein Präparat, das aus dem Kulturüberstand von apoptotischen peripheren mononukleären Zellen gewonnen wird. Ziel der vorliegenden Studie war es, den Effekt von APOSEC auf die Entwicklung der MVO zu untersuchen.4
Methodik
Schweinen wurde ein in der Leiste eingebrachter Führungsdraht bis in die linke Koronararterie vorgeschoben und die LAD („left anterior descending artery“) wurde mit einem Ballon für 90 Minuten verschlossen. Eine Gruppe der Versuchstiere wurde mit dem Präparat APOSEC intravenös behandelt, den anderen Tieren wurde nicht-konditioniertes Medium als Placebokontrolle verabreicht. Die für die MVO relevanten Datensätze wurden mittels Herzkatheter-, Herzultraschall-, Magnetresonanztomografie- (MRT), EKG- und Holter-EKG-Untersuchungen und regelmäßiger Blutabnahmen ermittelt. In einer zweiten Versuchsreihe wurde der Einfluss von APOSEC auf Thrombozyten und die Vasomotorik mittels Licht-Transmissions-Aggregometrie, Durchflusszytometrie, Immunhistochemie, Western-Blot-Analysen, ELISA und Myografieexperimenten an Koronararterienringen untersucht.
Ergebnisse
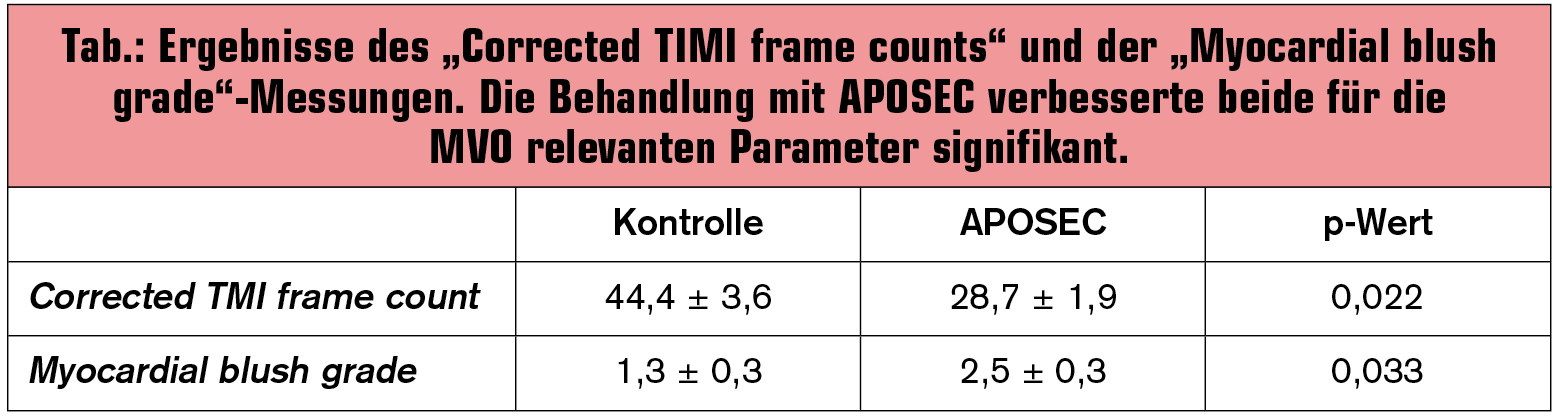
Die Verabreichung von APOSEC während eines akuten Herzinfarkts führte zu einer signifikanten Reduktion der Größe von MVO-Arealen (APOSEC: 0,3 ± 0,1 cm3; Kontrollen: 0,8 ± 0,1 cm3; p = 0,04). Diese Daten konnten durch Herzkathetermessungen bestätigt werden (Tab. 1).
Einen indirekten Hinweis auf die durch APOSEC verbesserte Durchblutung in der Mikrovaskulatur ergaben die Auswertungen der EKG- und Holter-EKG-Aufzeichnungen. In der Therapiegruppe hatten mehr Tiere eine Normalisierung der ST-Strecken-Veränderung und es kam insgesamt zu weniger arrhythmischen Episoden als in der Kontrollgruppe.
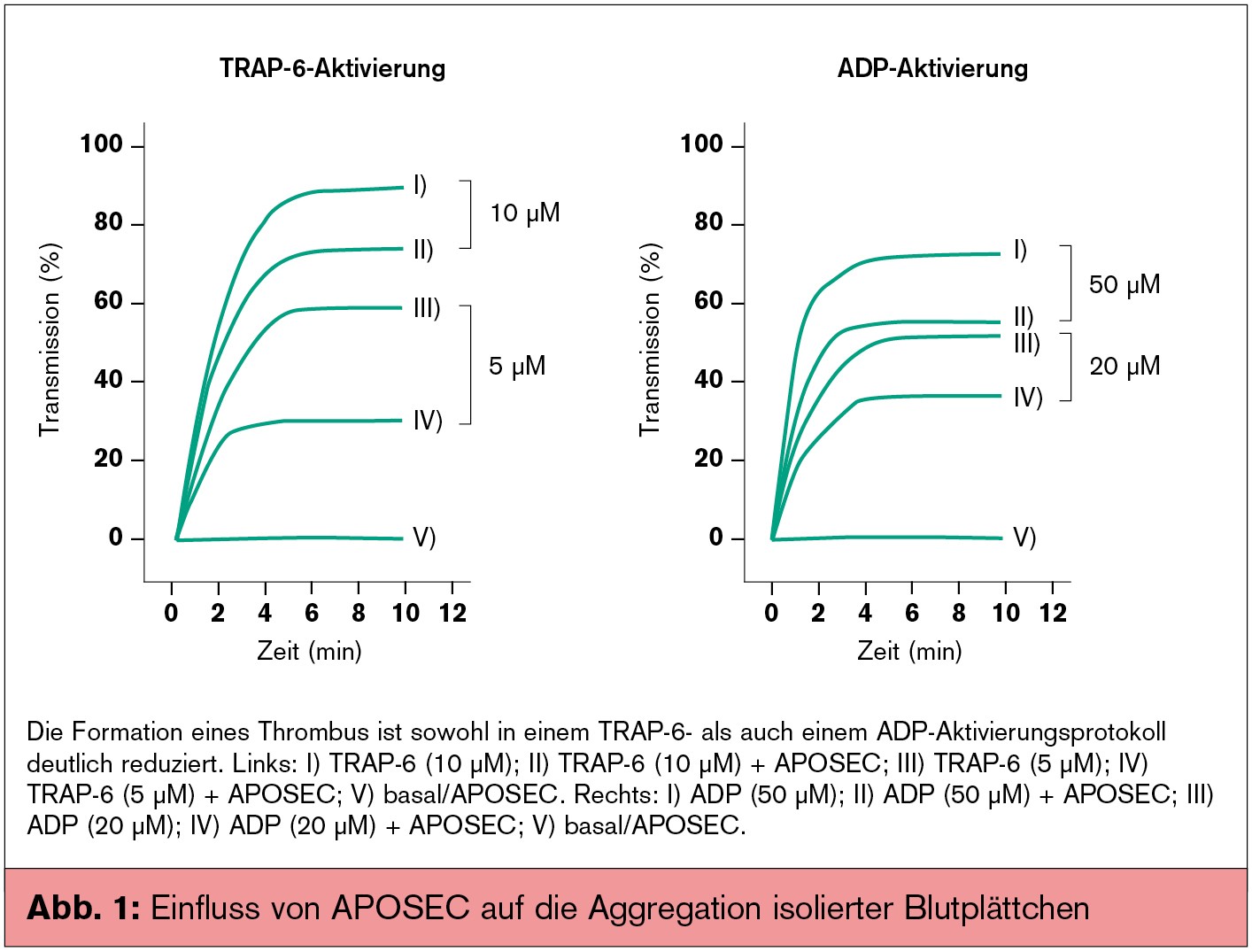
In weiterführenden In-vitro-Experimenten wurde der Einfluss von APOSEC auf die Aktivierbarkeit und Aggregation von Blutplättchen untersucht. Hier konnte gezeigt werden, dass eine Präinkubation von Thrombozyten mit APOSEC die Expression von Aktivierungsmarkern und folglich die Formation eines Thrombus reduziert (Abb. 1).
Als Mechanismus der plättchenhemmenden Eigenschaft von APOSEC konnte ein Einfluss auf die VASP-(Vasodilator-stimuliertes Phosphoprotein)-Signaltransduktion gezeigt werden.
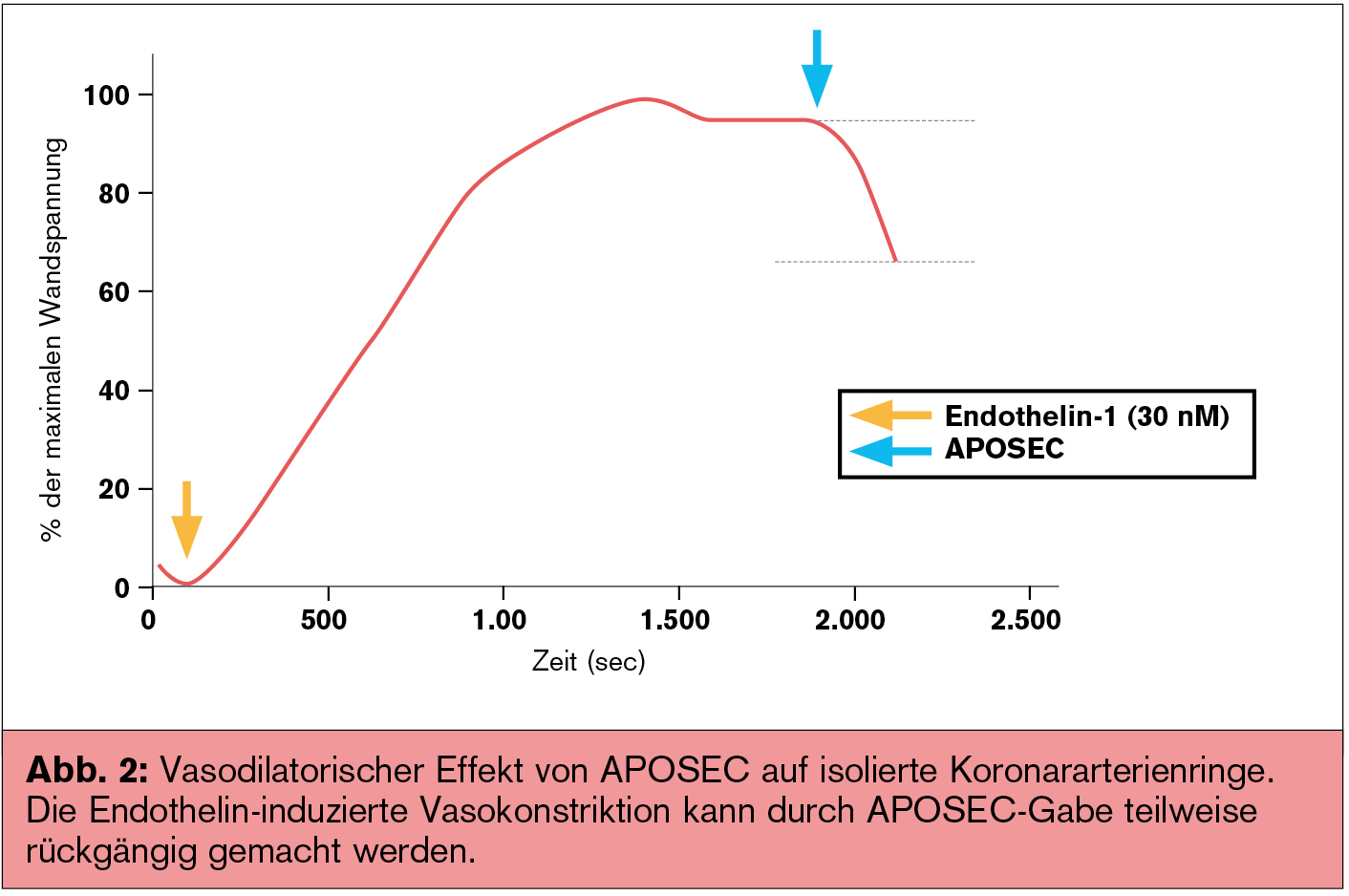
Da der vasomotorische Status der kleinen Blutgefäße ein wichtiger Kofaktor in der Entstehung der MVO ist, wurde ein möglicher Effekt von APOSEC auf die Vasomotorik untersucht. In Myografieexperimenten an isolierten Koronararterienringen konnte eine vasodilatorische Wirkung von APOSEC gezeigt werden (Abb. 2).
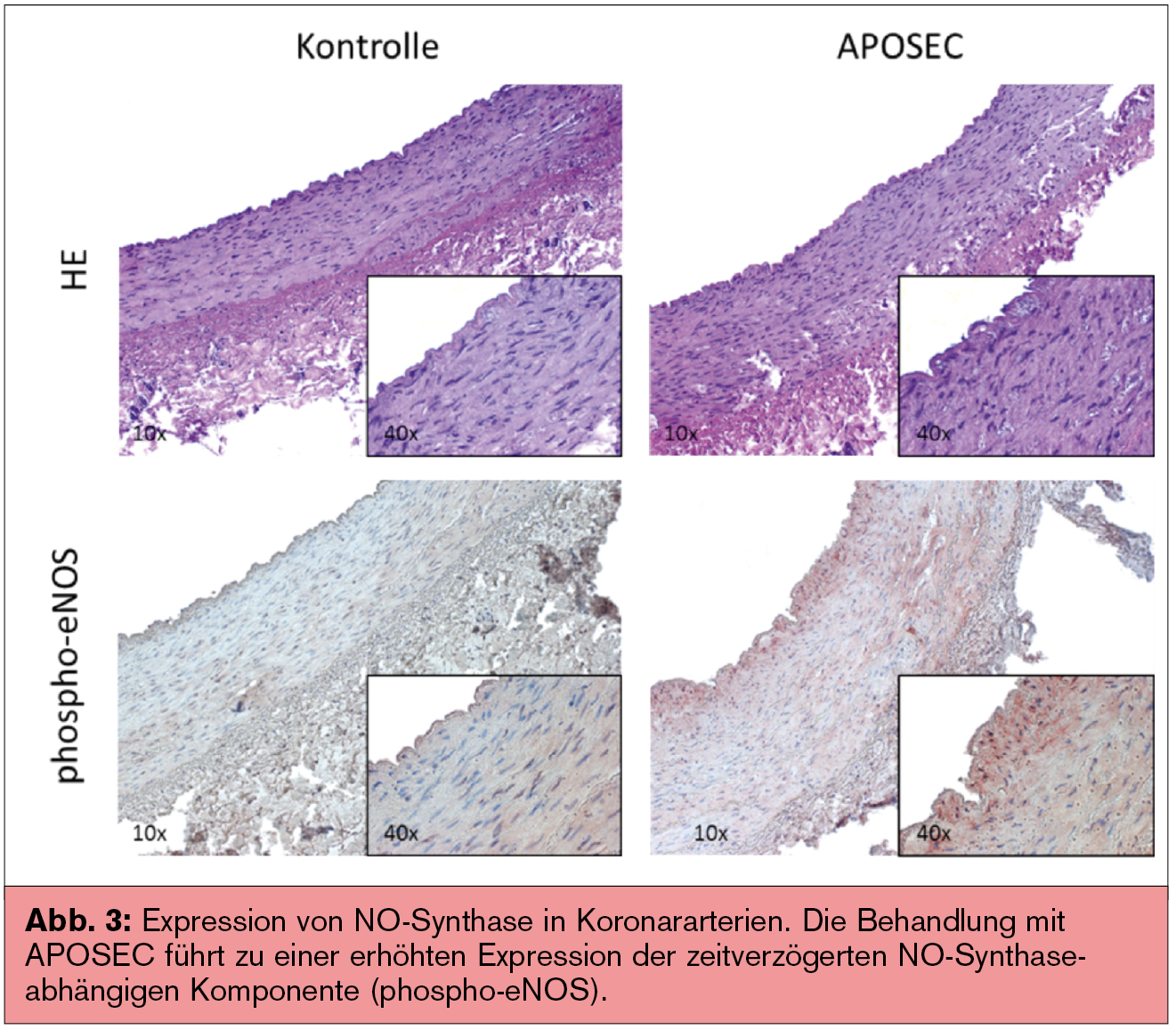
Diese gefäßdilatierende Wirkung von APOSEC konnte in eine unmittelbare NO-Synthase- unabhängige und eine zeitverzögerte NO-Synthase-abhängige (iNOS, phospho-eNOS) Komponente unterteilt werden (Abb. 3).
Ausblick
Die Therapie der MVO ist heute zu einem wichtigen Forschungsschwerpunkt der Kardiologie geworden. Mit einer adäquaten Behandlung der mikrovaskulären Obstruktion könnte die Prognose des Herzinfarkts weiter verbessert und die Langzeitmorbidität und -mortalität reduziert werden.
Die Entwicklung von APOSEC basiert auf Erkenntnissen der Stammzell-Forschung. Hier konnte in den letzten Jahren gezeigt werden, dass die Wirkung der Stammzelltherapie zu einem überwiegenden Teil den sezernierten, parakrinen Faktoren der Stammzellen zuzuschreiben ist.5 Seither konnten mehrere Gruppen alleinig durch die Verabreichung von Überstand aus kultivierten Stammzellen den ischämischen Schaden nach einem Herzinfarkt reduzieren. Der größte limitierende Faktor der Stammzelltherapie ist aber, dass die Gewinnung von Stammzellen technisch aufwändig und teuer ist.
Die Verwendung von Kulturüberstand alternativer Zellen mit den gleichen Wirkungen könnte dieses Problem lösen. In vorangegangenen Studien konnte gezeigt werden, dass der Kulturüberstand von Stammzellen und der Kulturüberstand von peripheren mononukleären Zellen vergleichbar ist.6 Basierend auf diesen Erkenntnissen wurde im Christian-Doppler-Labor für Diagnose und Regeneration von Herz- und Thoraxerkrankungen, Leitung: Assoc.-Prof. Univ.-Doz. Dr. Hendrik Jan Ankersmit, MBA, ein standardisierter Produktionsprozess des Präparats APOSEC entwickelt (Patentnr.: EP2201954, WO2010070105-A1). Bisher konnte ein therapeutischer Effekt des Präparats beim akuten Myokardinfarkt in Kleintier- und Großtiermodellen bewiesen werden.
Die oben beschriebenen Versuche stellen die Grundlage für eine erste Applikation im Menschen dar. In Analogie zu anderen „Biologicals“ wurden bereits toxikologische Untersuchungen bestanden und Virusinaktivierungsschritte erfolgreich in den Produktionsprozess implementiert. In Zusammenarbeit mit dem Roten Kreuz Oberösterreich wird zur Zeit eine vollständige GMP-konforme Produktion von APOSEC etabliert, um in naher Zukunft erste klinische Phase-I-Studien starten zu können.