Das Innsbrucker Lungentransplantationsprogramm
„Im April 1998, also genau vor 20 Jahren, haben Sie und Ihr Team bei mir eine Lungentransplantation durchgeführt. Ich danke Ihnen für die 20 wunderbaren Jahre, welche ich erleben durfte.“
Eine Postkarte mit diesem Schreiben erreicht mich am 24. April 2018 und ist ein Kondensat der Bemühungen von 25 Jahren Lungentransplantation. Ein sehr erfreuliches Kondensat und ein positives Zeugnis. Es zeigt nicht nur, was möglich ist, sondern auch, welche Schicksale damit verbunden sind und geformt werden. 20 Jahre ein „Lungentransplantierter“ zu sein, bedeutet das ganze Erwachsenenleben unter diesem Vorzeichen gelebt zu haben, bedeutet einen hervorragenden Erfolg der Transplantationsmedizin, bedeutet immer ein „geschenktes“ Leben zu leben, bedeutet unzählbar viele Tabletten, erlittene Komplikationen, immer wieder vor medizinisch schwierigsten Problemen zu stehen und in diesen „wunderbaren Jahren“ nicht nur glückbringende Wunder erlebt zu haben, sondern auch Wunder, die erschreckend sind, weil sie unerwartet kommen und lebensbedrohlich sein können.
Wie alles begann …
Schon 1985 wurde in Innsbruck durch Raimund Margreiter die erste isolierte Lungentransplantation (LTX) durchgeführt. Jedoch, die Zeit war noch nicht wirklich reif. Neben fehlender Infrastruktur an den Universitätskliniken in Innsbruck – es gab noch keine spezialisierte eigene Abteilung für Transplantationschirurgie und damit auch keine darauf spezialisierte Intensivstation, die involvierten chirurgischen Fächer wie Thoraxchirurgie, Herzchirurgie und Allgemeinchirurgie waren unter unterschiedlicher Leitung und daher schwer für die damals noch als experimentell anzusehende LTX zu gewinnen – war vor allem die chirurgische Technik noch nicht ausgereift.
Technische Fortschritte: LTX erfolgte damals noch en bloc, d. h., beide Lungenflügel wurden gleichzeitig im Block transplantiert, was neben technischen Herausforderungen und Schwierigkeiten auch mit Problemen der trachealen Anastomosenheilung verbunden war. Daneben bestand weder hinsichtlich der Empfänger- noch der Spenderselektion große Klarheit. Erst durch die bahnbrechenden Arbeiten von Joel Cooper und Alexander Patterson wurde die LTX zur Erfolgsgeschichte. Die Technik wurde durch die Einführung der Einzellungentransplantation entscheidend modifiziert. Zunächst erfolgt die Empfängerpneumonektomie auf einer Seite, dann wird der entsprechende Lungenflügel des Spenders in den Empfänger transferiert, und es werden nacheinander Hauptbronchus, Pulmonalarterie und Lungenvenencuff, d. h. die zu einer gemeinsamen Mündung vereinigten Lungenvenenstümpfe des Spenderorgans mit dem linken Vorhof des Empfängers anastomosiert. Nach Entlüftung der Spenderlunge wird die letzte Anastomose fertiggestellt und die Lunge wieder perfundiert und ventiliert. Damit nimmt das frisch transplantierte Organ auch schon seine volle Funktion auf, und die Operation kann auf der anderen Seite in analoger Weise fortgesetzt werden, die Oxygenierung erfolgt bereits ausschließlich durch die frisch transplantierte Lunge. Man kann aber auch nur eine Seite transplantieren (Single-Lung Transplant, SLTX), wenn die Grundkrankheit und die entsprechenden pathophysiologischen Verhältnisse dies zulassen (z. B. bei der Lungenfibrose oder bei manchen Formen des Emphysems), oder es werden eben beide Lungenflügel transplantiert (Bilateral Lung Transplant, BLTX), wenn dies wegen der zugrunde liegende Erkrankung erforderlich ist (alle infektiösen Erkrankungen wie zystische Fibrose, Bronchiektasen, pulmonale Hypertension oder stark bullöses Emphysem). Zudem weiß man heute, dass die bilaterale Transplantation bessere Langzeitergebnisse bringt als die SLTX. Etwa zwei Drittel der LTX konnten auf diese Weise durchgeführt werden.
Beim Rest war die Anwendung der extrakorporalen Zirkulation erforderlich, um einerseits die insuffiziente respiratorische Leistung nur einer Lunge während der Transplantation zu unterstützen, andererseits das Herz bei übermäßigem Anstieg des Pulmonalarteriendruckes während der unilateralen Ventilation und Perfusion zu unterstützen. Dies wurde in jenen Tagen durch Verwendung konventioneller HerzLungen-Maschinen (HLM) erreicht, was auch die notwendige Kooperation mit Herzchirurgen und Perfusionisten erklärt. In späteren Jahren konnte durch die neuen Entwicklungen auf dem Gebiet der extrakorporalen Zirkulation die Verwendung der HLM durch Anwendung der extrakorporalen Membranoxygenierung (ECMO) vielfach ersetzt werden, was mit verschiedenen Vor-, aber auch Nachteilen verbunden ist. Vor allem die geringere Antikoagulation ist bei der ECMO als Vorteil zu nennen, da dadurch die Blutungsproblematik entscheidend verringert wird. Da durch diese Kreislaufunterstützung ein Teil des Herzzeitvolumens (HZV) von einer Maschine übernommen wird, kommt es zu einer deutlichen Entlastung des rechten Herzens, was während der Klemmphase der Pulmonalarterie sehr vorteilhaft ist. Zudem muss nicht das ganze HZV durch das Gefäßstrombett nur einer Lunge gepumpt werden, was der Entwicklung eines Reperfusionsödems vorbeugt. Benötigt der Patient in den ersten Tagen noch eine ECMO-Unterstützung wegen primärer Organdysfunktion, ist nicht erst eine eigene Kanülierung erforderlich, und der Anschluss an das ECMO-System kann viel unkomplizierter erfolgen. Daher besteht heute eine Tendenz dazu, für die Transplantation die Kreislaufunterstützung mittels ECMO viel liberaler zu indizieren.
Empfänger- und Spenderselektion: Neben der standardisierten Technik wurde die Empfängerselektion neu definiert. Man hatte – was eigentlich naheliegend ist – herausgefunden, dass erfolgreiche LTX vor allem dann möglich ist, wenn es sich um ein isoliertes Einorganversagen handelt, d. h. der prospektive Empfänger keine wesentlichen Komorbiditäten aufweist. Der Transplantationskandidat sollte mobil und ausreichend rehabilitiert sein sowie frei von schweren Zusatzerkrankungen wie koronarer Herzkrankheit, Niereninsuffizienz und Ähnlichem. Ein Mehrorganversagen schwerstkranker Intensivpatienten stellt eine absolute Kontraindikation dar. Natürlich darf der prospektive Empfänger keine rezente Malignomanamnese haben und selbstverständlich kein Bronchuskarzinom. Intubation und mechanische Beatmung stellen in den meisten Fällen eine Kontraindikation dar. Ausgenommen sind mobilisierte Patienten mit Tracheostoma.
Ebenso wurden die Spenderselektionskriterien klar bestimmt: Neben Blutgruppe und Größe – definiert durch die totale Lungenkapazität (TLC) – spielen Oxygenierungsleistung (PaO2 bei 100 % FiO2), Alter, radiologischer und bronchoskopischer Befund sowie serologische Befunde die entscheidende Rolle.
Start des Innsbrucker LTX-Programms
1992 wurde dann für die neue Abteilung für Transplantationschirurgie eine eigene Station mit transplantationschirurgischer Intensivstation geschaffen, und es war möglich, das LTX-Programm mit idealen Voraussetzungen wieder aufzunehmen. Ich bekam als ausgebildeter Allgemein- und Thoraxchirurg, der gerade seine zusätzliche Ausbildung in Herzchirurgie begonnen hatte, den Auftrag, das LTX-Programm neu zu etablieren. Nach einem Studienaufenthalt bei Joel Cooper und Alexander Patterson in St. Louis, Missouri, folgten weitere umfangreiche Vorbereitungen: Ein umfassendes Team von Chirurgen, Pulmologen, Pädiatern, Anästhesisten, Perfusionisten, Pathologen, Radiologen, Intensivmedizinern, Physiotherapeuten und vielen anderen wurde gebildet. Erste Empfänger wurden selektiert und für eine uni- oder bilaterale Transplantation gelistet.
Am 1. 11. 1993, fast auf den Tag genau 4 Jahre nach der ersten österreichischen Lungentransplantation in Wien, wurde ein geeigneter Spender für einen Kandidaten für SLTX in einem auswärtigen Krankenhaus gefunden. Bei einem 56-jährigen Bergführer mit alpha-1-Antitrypsinmangel-bedingtem Emphysem konnte nun die linksseitige Einzellungentransplantation erfolgreich und komplikationslos durchgeführt werden. Nach einem unauffälligen postoperativen Krankenhausaufenthalt erfolgte die Rehabilitation, und der Mann konnte wieder in seine geliebten Berge zurückkehren und – wenn auch nicht mehr als Bergsteiger – sich in größerer Höhe ungehindert bewegen. Leider verstarb er nach 15 Monaten an den Folgen einer CMV-Erkrankung.
270 isolierte LTX in 25 Jahren
25 Jahre liegen zwischen der eingangs erwähnten Postkarte und diesem Datum – und exakt 270 Transplantationen. Naturgemäß haben sich in dieser langen Zeit viele Veränderungen zugetragen. Viele Mitglieder des Teams, insbesondere die Hauptverantwortungsträger in den meisten Disziplinen, haben mehrfach gewechselt, chirurgische Techniken und medikamentöse Behandlung, insbesondere zur Abstoßungsprophylaxe und -therapie haben sich geändert. Indikationen werden auf Grund der guten Ergebnisse heute viel weiter gestellt, sodass auch Patienten mit höherem Risiko in Betracht gezogen und gelistet werden. Die postoperative intensivmedizinische Behandlung ist erheblich modifiziert, und auch die Spenderselektion sowie insgesamt das Spenderaufkommen haben sich entwickelt.
Unverzichtbare Partner: Von Beginn an wurde die pulmologische Betreuung vorwiegend an der nichtuniversitären, aber sehr modernen Abteilung für Pneumologie im Landeskrankenhaus Natters durchgeführt. Abklärung von in Frage kommenden Patienten, gemeinsame Indikationsstellung und Nachbehandlung erfolgten von Anfang an vorwiegend in dieser Institution. Durch die hervorragende Kompetenz in dieser Abteilung können Patienten teilweise schon wenige Tage nach der TX direkt von der transplantationschirurgischen Intensivstation zur Weiterbehandlung an die pneumologische Station transferiert werden. Die gesamte Weiterbehandlung inklusive aller invasiven diagnostischen und therapeutischen Maßnahmen und die Rehabilitation erfolgen hier oder werden von hier aus koordiniert, wie zum Beispiel Dialyse oder Photopherese. Darüber hinaus besteht noch eine intensive Kooperation mit der Universitätsklinik für Innere Medizin sowie der Universitätsklinik für Pädiatrie in Innsbruck, welche sowohl in der Empfängerselektion als auch in der Nachbehandlung unverzichtbare Partner sind.
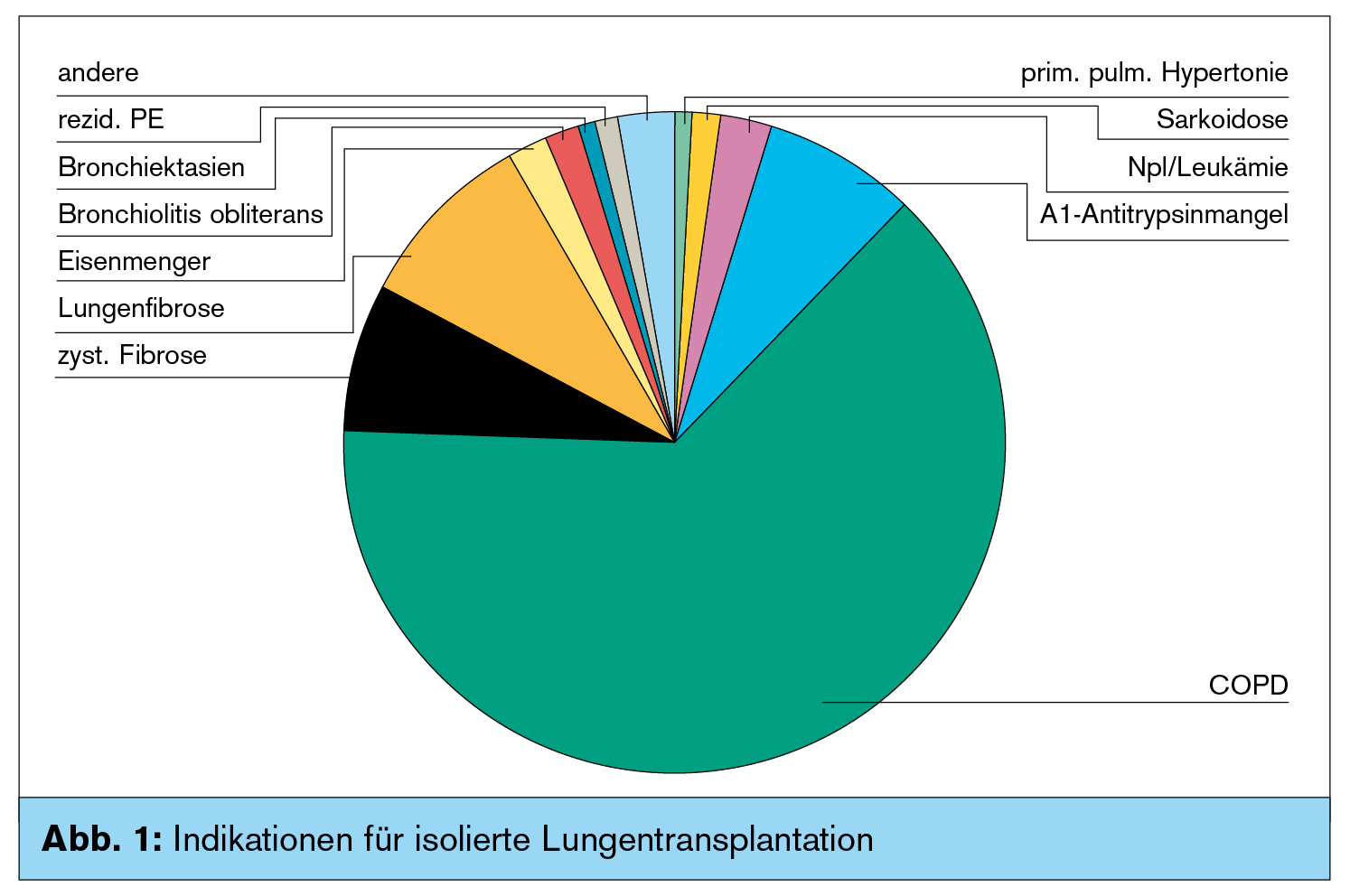
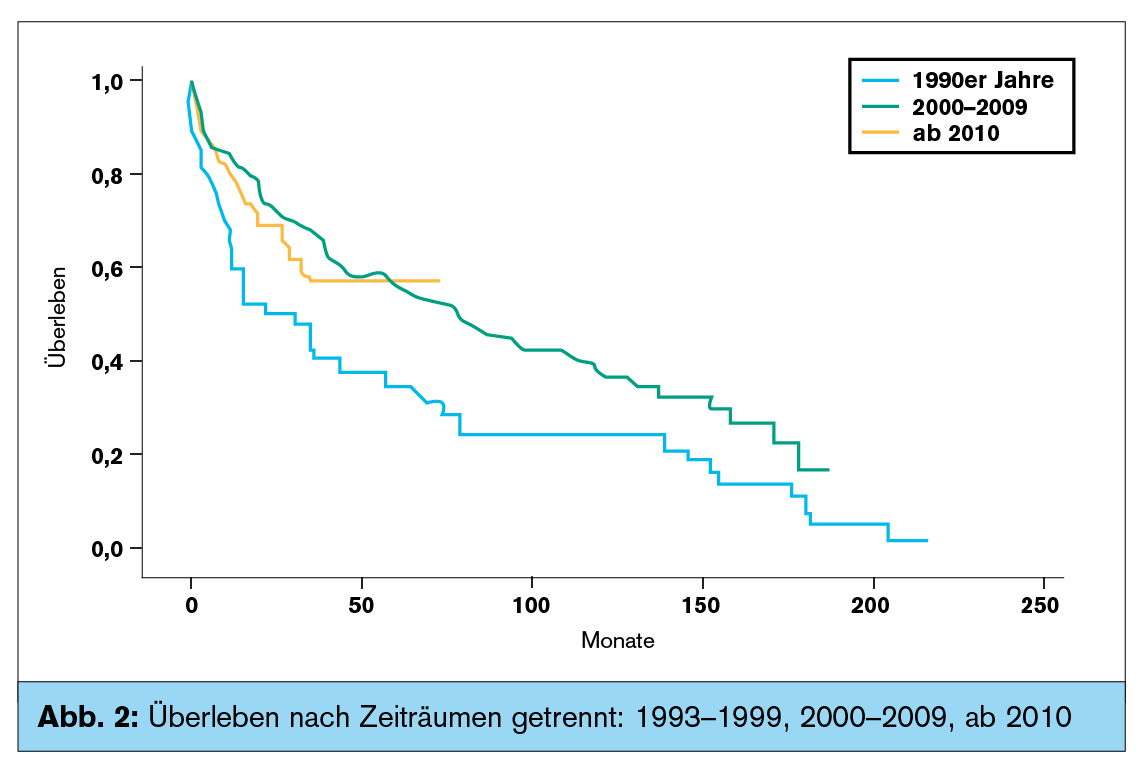
Erfolg in Zahlen: In Innsbruck werden derzeit jährlich 10–15 LTX durchgeführt. Dies entspricht dem Spenderaufkommen im Einzugsgebiet. Entsprechend wurden seit Beginn des Programms etwas über 260 isolierte LTX durchgeführt. Die Indikationen sind in Abbildung 1 dargestellt. Die Ergebnisse entsprechen den internationalen Standards. Aufgeschlüsselt nach den Zeiträumen von 1993 bis 1999, 2000 bis 2009 und ab 2010 sind sie in Abbildung 2 grafisch wiedergegeben.
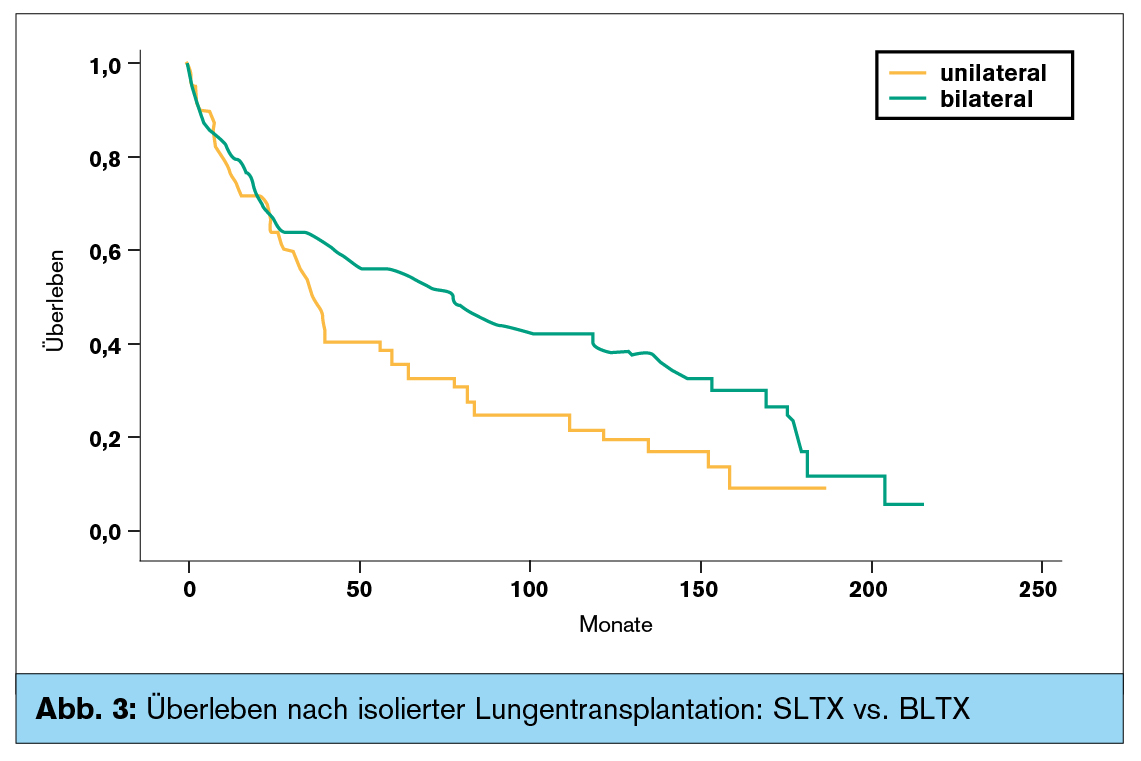
Auch im eigenen Patientengut zeigt sich klar, dass die BLTX deutlich bessere Langzeitergebnisse bringt als die SLTX (Abb. 3), sodass – wenn immer möglich – eine BLTX angestrebt wird. Obwohl die jährliche Zahl von Transplantationen überschaubar ist, werden durch die hohe Identifikation der einzelnen Teammitglieder mit dem Programm ausgezeichnete Ergebnisse erzielt. Insbesondere die in anderen Zentren kaum mögliche Behandlung aller Patienten mit soliden Organtransplantationen durch ein und dasselbe Team von Anästhesisten und Intensivmedizinern und in einer spezialisierten TX-Intensivstation bringt viele Vorteile. Große Konstanz besteht im chirurgischen Team, das seit Anbeginn unter derselben Leitung arbeitet und bei den anderen Mitgliedern nur geringe Fluktuationen aufweist.
Aktuelle Herausforderungen
Nach weitgehender Klarheit und vielfach internationaler Übereinstimmung in den oben angeführten Bereichen von Technik, Immunsuppression und Empfängerselektion liegen heute die besonderen Herausforderungen bei der Lungentransplantation in der Prophylaxe des Bronchiolitis-obliterans-Syndroms und der Erweiterung des Spenderpools durch sogenannte Non-Heart-beating Donors, also Patienten, die nicht nur einen Hirntod erlitten haben, sondern bei denen auch ein irreversibler Herzstillstand besteht sowie in der extrakorporalen Lungenperfusion. In all diesen Bereichen bestehen derzeit nur teilweise gelöste medizinische, aber auch organisatorische Herausforderungen.