Diabetes mellitus nach Nierentransplantation – Neue Erkenntnisse und bestehende Herausforderungen
Hintergrund und Bedeutung
Die Folgen eines NODAT sind insofern bedeutsam, als sowohl die Überlebenszeit des Transplantats, aber auch kardiovaskuläre Morbidität und Mortalität des Transplantatempfängers negativ beeinflusst werden. Eine reine Hyperglykämie (_ 200 mg/dl) tritt innerhalb der ersten Wochen nach Transplantation auch bei vorher nicht-diabetischen Patienten häufig auf und gilt per se als starker Prädiktor für die Entwicklung eines NODAT.
Ursachen und Risikofaktoren
Die Gründe für Störungen des Glukosestoffwechsels nach Nierentransplantation sind vielfältig. Dazu zählen:
- die Gabe von vor allem perioperativ hochdosiertem Kortison und
- Kalzineurininhibitoren (Tacrolimus oder Cyclosporin A)
- der chirurgische Operationsstress
- die Aktivierung von während der Dialyse durch die fehlende Nierenfunktion unentdeckt gebliebenen diabetischen Stoffwechsellagen mit beginnender Transplantatfunktion
- fehlende Bewegung und Sport sowie
- fehlerhafte Ernährung
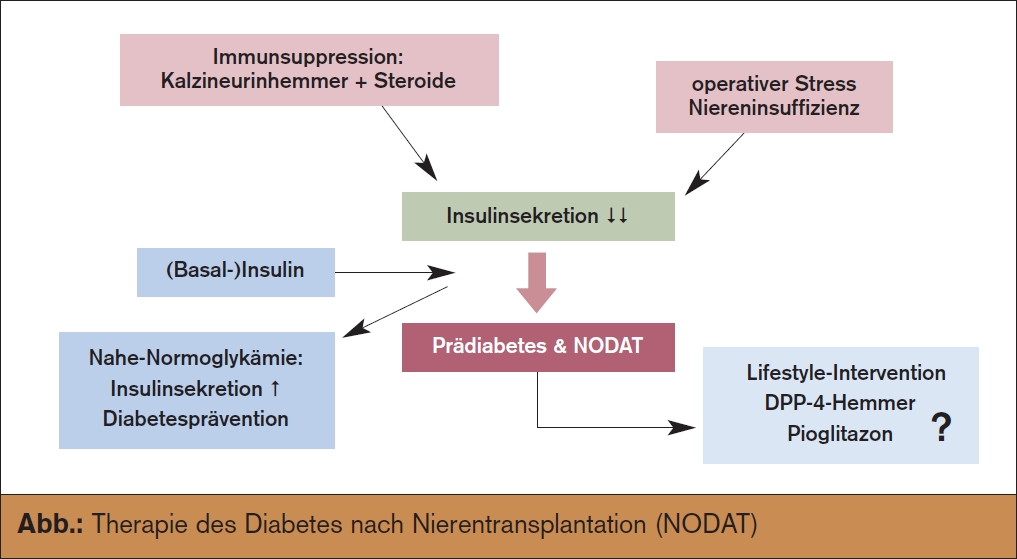
Gewichtet dürfen als Hauptauslöser die Immunsuppression und der chirurgische Stress gelten, wobei nach tradierter Sicht Steroide die Insulinresistenz erhöhen und Kalzineurinhemmer die Insulinsekretion supprimieren. Eine Reihe von Risikofaktoren gelten als besonders prädisponierend für einen NODAT: neben dem Empfängeralter etwa der Body Mass Index und diverse Koinfektionen, allen voran die Hepatitis-C-Infektion. Interessanterweise sind besonders Patienten mit polyzystischer Nierenerkrankung hoch gefährdet, einen NODAT zu entwickeln. Dennoch ist es – trotz Identifikation verschiedener Gene, die teilweise mit der Suszeptibilität für Typ-2- Diabetes übereinstimmen – nicht genau vorhersagbar, welche Patienten nach Transplantation einen Diabetes entwickeln.
Gestörte Nüchternglukose und Glukosetoleranz als Vorboten eines NODAT kommen naturgemäß in den ersten Wochen nach Transplantation sehr häufig vor, sind jedoch bei stabil Nierentransplantierten, d. h. mindestens 6–12 Monate nach der Transplantation, immerhin noch bei ca. 20–30 % der Patienten zu finden. Gerade in den letzten Monaten sind vermehrt Datensätze aus großen Kollektiven publiziert worden, wonach die gestörte Glukosetoleranz einen unabhängigen Prädiktor für eine drastisch gesteigerte Gesamtmortalität bei Nierentransplantierten darstellt (Valderhaug et al., Diabetes Care 2011).
Therapie bis dato insuffizient
Eines der zentralen Probleme des NODAT besteht neben dem fehlenden pathophysiologischen Verständnis in der bislang unklaren Therapie bzw. überhaupt der Prävention. Die derzeit noch gültigen Guidelines aus dem Jahr 2003 sehen nicht vor, eine perioperative Hyperglykämie zu therapieren. Vielmehr lehnen sie sich an die Richtlinien der schrittweisen Behandlung des Typ-2-Diabetes an, indem auch für NODAT eine nicht-pharmakologische Therapie (sog. Lifestyle-Intervention), gefolgt von oralen Antidiabetika, und erst bei deren therapeutischer Insuffizienz Insulinergänzung oder -substitution empfohlen wird (Davidson et al., Transplantation 2003).
Unserer Meinung nach ist eine Lifestylemodifikation mit v. a. Betonung der aeroben Fitness unmittelbar nach Transplantation schwer bis gar nicht umsetzbar, weiters ist die Zahl effektiver und besonders sinnvoller oraler Antidiabetika unmittelbar nach Transplantation sehr limitiert: Metformin als bislang bestes initiales orales Medikament ist naturgemäß in den ersten Wochen aufgrund der Niereninsuffizienz nicht verwendbar. Für Glitazone existieren im initialen Transplant- Setting einerseits keine studienbasierten Daten, zudem wäre der Einsatz aufgrund der pharmakodynamischen Effektivität sicher zu spät. Zu DPP-4-Hemmern (Dipeptidylpeptidase 4) liegen noch keine Daten vor. Daher haben aus Praktikabilitätsgründen, wie in den Guidelines empfohlen, die Sulfonylharnstoffe einen fixen Platz in der initialen, aber auch späteren Post-Transplant-Phase.
Aus unserer Sicht ist das beschriebene Therapieprinzip vermutlich nicht sinnhaft, da ge- rade die ersten Wochen nach erfolgter Organspende eine exzessive Inselzellbelastung darstellen. Aus diesem Dilemma heraus haben wir an der Klinischen Abteilung für Nephrologie der Inneren Medizin III an der Medizinischen Universität Wien ein Studienteam etabliert, welches sich der Beantwortung der essenziellen Fragen nach sinnvoller NODAT-Therapie widmet. Des Weiteren beschäftigt sich unsere Arbeitsgruppe mit dem Verständnis der Pathophysiologie des NODAT (> Abb.).
Die TIP-Studie
Die TIP-Studie (Treat-to-target Trial of Basal Insulin in Post-transplant Hyperglycemia) tes tete im Sinne eines „Bottom-up Approach“ die Hypothese, dass eine gegen die initiale postoperative Hyperglykämie gerichtete Therapie mit Basalinsulin die Betazellen des Pankreas vor der „elektiven“ Überlastung im Rahmen der Transplantation schützt und somit das Auftreten von NODAT verhindern kann (Hecking et al., J Am Soc Nephrol 2012). Voraussetzung für die Durchführung der TIP-Studie war, dass bei allen an der Studie teilnehmenden nierentransplantierten Patienten, die vor ihrer Operation in eine Insulin-Behandlungsgruppe sowie in eine kon – ventionell therapierte Kontrollgruppe ran do – misiert wurden, mehrmals täglich Blutzu – ckermessungen durchgeführt wurden.
Basalinsulin vs. konventionelle Therapie: Die Therapie in der Basalinsulin-Gruppe wurde erst bei Überschreiten abendlicher Blutzu – ckerwerte von 140 mg/dl begonnen, um der Wirkung des exogenen Kortisons über den Tagesverlauf, mit charakteristischen Blutzu – ckerspitzen in den späten Nachmittags- und frühen Abendstunden, Rechnung zu tragen. Aufgrund eben dieser speziellen Charakteristik des täglichen Blutzuckerverlaufs wie auch der Praktikabilität wurde prinzipiell als erster Schritt eine Behandlung mit einem Basalinsulin (Isophan-Insulin) eingeleitet, welches ein Wirkungsmaximum nachmittags bis frühabendlich aufweist. In der Kontrollgruppe oblag eine blutzuckersenkende The – rapie prinzipiell der behandelnden Betten – sta tion. Es wurde aber im Studienprotokoll empfohlen, erst ab einem Blutzucker von 180 mg/dl mit einer Therapie zu beginnen und primär orale Antidiabetika, wie in den immer noch gültigen Guidelines vorgesehen, einzusetzen (präferentiell Sulfonylharn – stoffe). Bei Blutzuckerwerten > 250 mg/dl musste laut Studienprotokoll aus ethischen Gründen auch in der Kontrollgruppe eine Therapie mit Insulin (präferenziell kurz wirksamem Insulin) initiiert werden.
Hohe Hyperglykämierate: An der TIP-Studie nahmen 2 x 25 Nierentransplantierte teil. Das erste Ergebnis war die Aufdeckung einer massiven unmittelbar postoperativen Hyperglykämierate: 23 Kontrollgruppenpatienten (92 %) hatten Blutzuckerwerte _ 200 mg/dl, und alle Behandlungsgruppe-Patienten (100 %) wiesen vor Ende des zweiten postoperativen Tages Blutzuckerwerte _ 140 mg/dl auf, so dass hier zügig mit Basalinsulin begonnen werden konnte. Die bereits bei Studiendesign antizipierte große Diskrepanz zwischen abendlichen gegenüber morgens gemessenen Blutzuckerwerten wurde klar bestätigt, denn im Durchschnitt waren die Blutzucker- Abendwerte in der Kontrollgruppe um 73 mg/dl höher als die Morgenwerte. Das Blutzuckerziel von 110–120 mg/dl in der Behandlungsgruppe wurde trotz einer durchschnittlichen Insulintagesdosis von 17 IE deutlich überschritten (Blutzuckertagesdurchschnitt in der Behandlungsgruppe: 139 mg/dl).
Es kam in der Behandlungsgruppe 5-mal und in der Kontrollgruppe 1-mal zum Auftreten einer rasch reversiblen Hypoglykämie (gemessener Blutzucker 41–60 mg/dl), die aber klinisch so geringgradig ausgeprägt war, dass sie keinem der Patienten vor der Messung aufgefallen war. Insgesamt musste Basalinsulin bei nahezu allen Studienpatienten ca. 3 Monate verabreicht werden, 2 Patienten benötigten das Basalinsulin deutlich länger als 3 Monate.
Basalinsulin effizient: Der HbA1c-Wert in der Behandlungsgruppe stieg – trotz Basalinsulin- Therapie – nach 3 Monaten um durchschnittlich 0,5 % (von 5,2 % ± 0,5 % auf 5,7 % ± 0,6 %) an. Die Basalinsulin-Therapie erwies sich aber trotzdem als äußerst effizient, da der HbA1c-Wert in der Behandlungsgruppe nach 3 Monaten immer noch um durchschnittlich 0,5 % niedriger war als in der Kontrollgruppe, wo er von 5,3 % ± 0,4 % auf 6,2 % ± 0,7 % anstieg. Somit wurde der primäre Endpunkt der Studie (signifikanter Unterschied im HbA1c zwischen Kontroll- und Behandlungsgruppe nach 3 Monaten im Sinne einer „Feasibility“-Studie) erreicht.
In der weiteren Folge, bis zum Ende des Beobachtungszeitraums nach 12 Monaten, blieb der HbA1c-Wert in der Behandlungsgruppe trotz Absetzen der Basalinsulin-Therapie robust auf dem gleichen Niveau. Des Weiteren hatten die Behandlungspatienten bei oralen Glukosetoleranztests (OGTTs) in den Monaten 3, 6 und 12 konsistent niedrigere Diabetes- und Prädiabetesraten (Odds Ratio = 0,27 für Diabetes in der Behandlungsgruppe im Vergleich zur Kontrollgruppe nach 12 Monaten). Außerdem war nach 12 Monaten keiner der Behandlungspatienten – aus klinischer Sicht – therapiebedürftig, wohingegen bei 7 der Kontrollpatienten (28 %) Antidiabetika verabreicht werden mussten. Der sog. insulinogene Index, ein Test der Betazellfunktion als Maß für die Insulinsekretion, abgeleitet aus den OGTTs nach 3, 6 und 12 Monaten, war in der Basalinsulin-Gruppe besser als in der Kontrollgruppe, wohingegen der sog. Orale-Glukose-Sensitivitäts-Index, ein Test der Insulinsensitivität als Maß für die Insulinresistenz, unverändert war. Dieses Ergebnis belegte nicht nur die Studienhypo – these, dass exogen zugeführtes Insulin die Betazellen des Pankreas vor chirurgisch und medikamentös ausgelöster Überlastung schützt, sondern könnte auch darauf hinweisen dass im frühen Transplantverlauf weniger die Insulinresistenz als vielmehr die akute Inselzelltoxizität, bedingt durch chirurgischen Stress und Immunsuppression, das entscheidende pathogenetische Prinzip darstellt.
TIP-Studien – Zusammenfassung und weiterführende Konzepte: Nach den Studienergebnissen der TIP-Studie ist die Therapie mit Basalinsulin ein einfaches wie auch praktikables therapeutisches Konzept, welches in der beschriebenen Untersuchung sehr nebenwirkungsarm und gleichzeitig hinsichtlich NODAT-Prävention sehr effizient scheint. Unsere weiterführenden Projekte zur postoperativen Insulintherapie bei Nierentransplantierten beinhalten die Durchführung einer von den National Institutes of Health (NIH, USA) geförderten internationalen Multicenter-Studie unter der Leitung der University of Michigan (Start 2012; Koordination der euro – päischen Zentren durch die Medizinische Universität Wien). Unser Konzept, die Post- Trans plant-Hyperglykämie per se mit Insulin zu thera pieren, würde im Fall multizentrischer Reproduktion einen therapeutischen Paradigmenwechsel ermöglichen. Eine Weiterentwicklung dieses Konzepts am Wiener Zentrum beruht auf neuester Insulinpumpentechnologie, nämlich dem Einsatz programmierter Insulinbasalraten und zusätzlicher kontinuierlicher Blutzuckermonitorisierung, die bei potenziell gefährlichen Blutzuckerwerten die Insulinabgabe vollautomatisch abstellt. Dieses Konzept könnte einen Schritt hin zu einem Closed-Loop-System darstellen: Die Tatsache, dass die Transplantation so – zusagen eine elektive Diabetesinduktion darstellt, bietet für den Einsatz solcher innovativer Technologien ein hervorragendes Einsatzgebiet mit der Möglichkeit eines beträchtlichen Erkenntnisgewinns.
Stabil Nierentransplantierte
Wie berichtet, sind metabolische Komplikationen bei Nierentransplantierten generell häufig. Um einen genaueren Einblick in Prävalenz, aber auch in die genauere Pathophysiologie des NODAT zu bekommen, haben wir in der sog. TAHG-Studie (Transplant-associated Hyperglycemia Study) insgesamt 1.064 Patienten an unserem Zentrum, welche mindestens 6 Monate eine stabile Transplantatfunktion aufweisen, studiert. Mit Hilfe von OGTTs die bei über 300 zufällig ausgewählten Patienten durchgeführt wurden, konnte gezeigt werden, dass neben 11 % schon vor bestehendem NODAT im gesamten TAHGKollektiv) sowie 12 % Typ-1- und Typ-2-Diabetikern immerhin 42 % aller durchgeführten OGGTs bei anamnestisch nicht als Diabetikern bekannten Patienten abnormal waren. Dabei wiesen sogar 9 % die Kriterien eines Diabetes mellitus auf. Eine detaillierte Analyse der Befunde wies interessanterweise auf einen generellen Defekt der Inselzellfunktion hin, wobei erstaunlicherweise die Insulinsensitivität der Patienten erhöht war verglichen mit nicht-transplantierten Kontrollpatienten (Hecking et al., Manuskript in Vorbereitung). Es ist nun naheliegend zu spekulieren, ob generell immunsupprimierte nierentransplantierte Patienten hinsichtlich ihres Pathomechanismus eher Patienten mit einem pankreopriven Diabetes ähneln als Typ-2- Diabetikern, welche als Kardinalcharakteris – tikum ihrer Stoffwechsellage eine deutlich erhöhte Insulinresistenz aufweisen. Diese und weitere Analysen sind essenziell, v. a. was die möglichen therapeutischen Optionen betrifft.
GCPD-Studie: Um stabil transplantieren Patienten, bei welchen im späteren Krankheitsverlauf Störungen im Glukosemetabolismus auftreten, zu helfen, haben wir zwei Studien an unserem Zentrum initiiert, die sowohl Prädiabetiker als auch overte Diabetiker betreffen. Die GCPD-Studie (Glucose Control in Prediabetes) wurde vor kurzem abgeschlossen. Hier handelt es sich um eine randomisierte, placebokontrollierte prospektive klinische Studie mit dem Ziel, die Sicherheit und Wirksamkeit des DPP-4-Hemmers Vildagliptin und des Thiazolidindions Pioglitazon bei 3 x 16 Patienten mit neu aufgetretener gestörter Glukosetoleranz nach Nierentransplantation zu testen (Werzowa et al., Manuskript submittiert). Nach lediglich 3 Monaten Therapie kam es unter Vildagliptin zu einer signifikanten Verbesserung des 2-Stunden- OGTT-Wertes sowie des HbA1c; unter Pioglitazon verbesserte sich zusätzlich auch noch der Nüchtern-Glukosewert. In der Placebogruppe kam es hingegen zu keiner signifikanten Verbesserung des Glukosestoffwechsels. Die Nebenwirkungsrate war in den 3 Gruppen ähnlich und es traten nur milde Nebenwirkungen auf. Diese Daten deuten somit darauf hin, dass eine pharmakologische Intervention mit Vildagliptin bzw. Pioglitazon bei Nierentransplantierten bereits bei prädiabetischer Stoffwechsellage sicher und effektiv und damit sinnvoll sein dürfte. Als Wirkmechanismus nehmen wir eine zusätzliche Verbesserung der Insulinsensitivität an.
VINODAT-Studie: In der sog. VINODAT-Studie (Vildagliptin bei NODAT) wird die Effektivität und Sicherheit von Vildagliptin bei neu aufgetretenem NODAT untersucht (Haidinger et al., Trials 2011). Primär wird bei dieser doppelblinden 2-armigen Studie (Vildagliptin vs. Placebo) bei 32 stabil Nierentransplantierten die Veränderung der Glukoseregulation unter Therapie nach 3 Monaten studiert, die Studie wird innerhalb dieses Jahres abgeschlossen sein. Bereits in der vorliegenden Zwischenanalyse ist eine deutliche Verbesserung der Stoffwechselsituation unter Vildagliptin zu beobachten: Ähnlich den existierenden Daten bei Typ-2-Diabetikern waren allfällige Nebenwirkungen auf Placeboniveau, Hypoglykämien waren bei dieser Substanzklasse überhaupt keine zu beo – bachten.
Erkenntnisse und Ausblick
Störungen des Blutzuckerstoffwechsels treten nach Organtransplantation regelhaft auf und sind als Prädiabetes und manifester Diabetes (NODAT) mit einem signifikant schlechteren Outcome, sowohl was Transplantatfunktion und -überleben als auch was Patientenüberleben betrifft, assoziiert. Leider sind die letzten Empfehlungen zu Diagnose und Therapie dieser Erkrankung überholt, besonders was das unmittelbare Management nach Nierentransplantation betrifft. Rezent publizierte Ergebnisse aus unserem Zentrum ermöglichen eine völlig neue Therapieperspektive, da durch frühzeitige Gabe von Basalinsulin offenbar eine Entlastung des Inselzellapparats ermöglicht wird, welche in hohem Maß zu einer Reduktion eines Post- Transplant-Diabetes führt. Weiterführende Studien zur Pathophysiologie des NODAT und zu alternativen Präventions- und Therapiestrategien sind unbedingt notwendig, um die Erfolgsaussicht für transplantierte Patienten weiter zu verbessern. Die Umsetzung dieses ehrgeizigen Zieles steht derzeit im Brennpunkt einiger internationaler Gruppen und sollte zu neuen Standards zur Betreuung nierentransplantierter Patienten innerhalb der kommenden Jahre führen können. Ein wesentlicher Schritt in diese Richtung ist der Wiener Transplantations-Chirurgie (Univ.- Prof. Dr. Ferdinand Mühlbacher und Mitarbeitern) zu verdanken, die nicht nur die TIPStude massiv unterstützt hat, sondern auch die Einberufung eines internationalen NODAT-Consensus Meetings beim Kongress der European Society for Organ Transplantation in Wien im Jahr 2013.