HIV, Gendermedizin und Combination Prevention
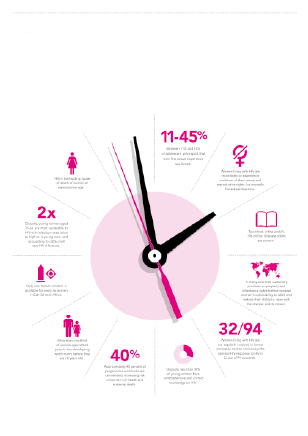
Das Wendejahr der HIV-Medizin war 1996. Die erfolgreichen Studiendaten der ersten HIV-Kombinationstherapie waren der Beginn der Transformation von AIDS hin zur chronischen HIV-Erkrankung. In reichen Ländern mit ausreichend zugänglichen Gesundheitssystemen führte dies zu einem signifikanten Rückgang der AIDS-assoziierten Todesfälle. Weltweit wird jede Minute eine Frau mit dem HI-Virus infiziert. Junge Frauen (Abb.) gelten als besonders vulnerable Gruppe, was das HIV-Infektionsrisiko betrifft, vor allem in Hochprävalenzländern. Nun wurde ein internationales Selbsthilfeprogramm namens SHE gegründet, welches besonders auf die Bedürfnisse von Frauen mit HIV fokussiert und die Zusammenarbeit zwischen medizinischem Personal und den Betroffenen fördern soll. SHE – Strong, HIV positive, Empowered women – startete 2012 in Österreich und Deutschland. Der Frauenanteil der in Österreich mit HIV infizierten Menschen beträgt 29 %.
Frauen in HIV-Studien unterrepräsentiert: HIV-positive Frauen leiden an einem signifikant höheren Level von Stress, Angstzuständen und Depressionen.1, 2, 3 Generell ist der Frauenanteil in HIV-Studien gering, er liegt bei 17 bis 31 %. So wurde erst in letzter Zeit damit begonnen, frauenspezifische Problemstellungen und Bedürfnisse in größerem Ausmaß wissenschaftlich aufzuarbeiten. In Zentral- und Osteuropa wird der Zugang zur Therapie nicht vom Geschlecht der HIV-positiven Person beeinflusst. Eine Therapie zu erhalten ist für Frauen wahrscheinlicher als für Männer.
Die Food and Drug Administration (FDA) publizierte eine Metaanalyse von HIV-Studien im Zeitraum zwischen 2000 und 2008, in der die Daten von 22.411 PatientInnen analysiert wurden. Der Frauenanteil betrug 20 %. Signifikante Geschlechtsunterschiede in Bezug auf Therapieansprechen zur Woche 48, Therapieabbruch wegen unerwünschter Ereignisse, „Loss to Follow-up“ oder Tod konnten nicht festgestellt werden.4, 5 Die Rate der Therapieabbrüche wegen Therapieversagens war bei Männern höher als bei Frauen, 8,15 % vs. 4,25 %. Geschlechtsspezifisch waren statistisch oder klinisch signifikante
Unterschiede in der Effektivität nicht nachweisbar.
Therapie: Geschlechtsspezifisches Nebenwirkungsprofil: Die Tolerabilität der HIV-Therapie hat sich im Vergleich zu den Anfangsjahren drastisch gebessert, allein die Anzahl der Tabletten kann je nach Situation auf ein Single-Tablet- Regimen reduziert werden. Die Nebenwirkungsrate zwischen Mann und Frau unterscheidet sich oft nicht, jedoch ist das Nebenwirkungsprofil anders. Frauen leiden häufiger an Übelkeit und Erbrechen, Männer an Durchfällen.
Eine der schwerwiegenden Nebenwirkungen der HIV-Therapie ist die Störung des Fettstoffwechsels mit einem nach außen hin sichtbarem Fettumbau, genannt Lipodystrophie. Unterteilt wird dieses Syndrom in zwei Hauptformen: die Lipoatrophie, welche den Schwund von vorwiegend Subkutanfett bezeichnet, besonders auffallend und stigmatisierend im Gesicht und die Lipohypertrophie, mit der nicht steuerbaren Zunahme von Fettgewebe im Bereich der Brüste, des Nackens und des Bauches. Isolierte Lipoatrophie tritt bei Frauen weniger häufig auf, vermehrt jedoch Lipohypertrophie.
HIV und Schwangerschaft: In der WHO-Europa-Region sind 77 % der HIV-positiven Frauen im gebärfähigen Alter. Die Lebenserwartung von HIV-positiven Menschen ist hoch und erreicht je nach statistischem Modell nahezu jenes HIV-negativer Menschen. Somit ist es nachvollziehbar, dass sich die Lebensplanung ändert und konsekutiv die Familienplanung. 2012 ist es möglich, HIV-positive Frauen mit Kinderwunsch so zu unterstützen, dass das Infektionsrisiko für das Neugeborene nahezu null beträgt. Wichtig ist hierbei der rechtzeitige Beginn der HIV-Therapie, sodass die Viruslast unter die Nachweisgrenze gesenkt werden kann und eine Infektion des Kindes verhindert wird. Ist während der Schwangerschaft keine Viruslast mehr nachweisbar, kann auch eine Spontangeburt in Betracht gezogen werden. Besteht bei einem serodiskordanten Paar (Mann HIV+, Frau HIV–) ein Kinderwunsch, so ist die Zeugung unter bestimmten Voraussetzungen auf natürlichem Wege möglich.
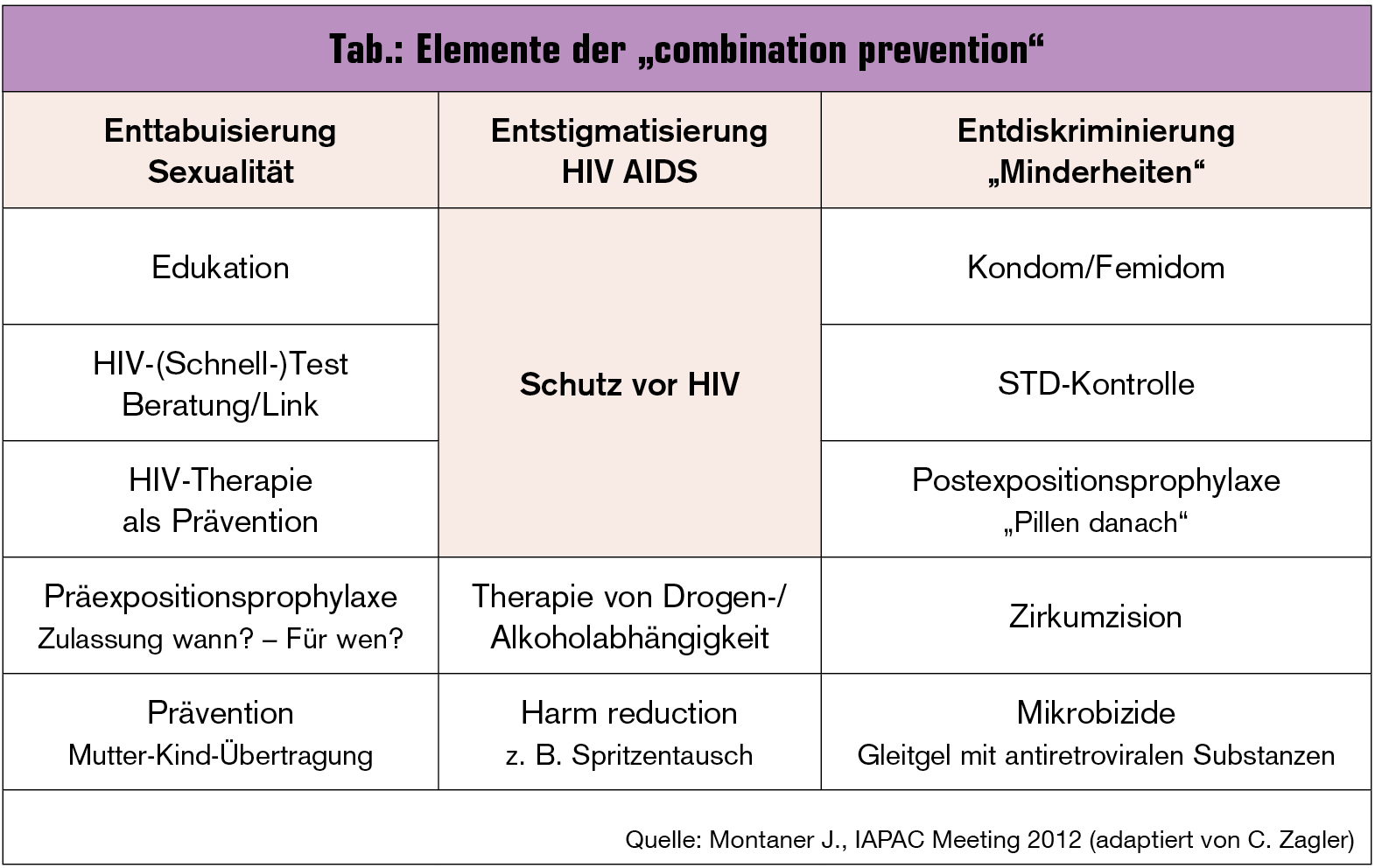
Paradigmenwechsel durch „combination prevention“: Die Strategien, die für serodiskordante Paare mit Kinderwunsch entwickelt, und die Erkenntnisse, die daraus gewonnen wurden, führten zu neuen Präventionsideen. Hilfsmittel wurden kreiert, die sinnvoll im Kampf gegen HIV/AIDS eingesetzt werden können. Dafür wird der Begriff „combination prevention“ verwendet. Der Einsatz von HIV-Medikamenten bei HIV-positiven und -negativen Menschen scheint besonders effektiv zu sein und wird zu einem Paradigmenwechsel in der Prävention von HIV führen. Diese setzt sich 2012 aus zwei wesentlichen Interventionen zusammen: der ärztlich-medizinischen Intervention und der psychologisch-edukativen Intervention. Präventionsmöglichkeiten können perfekt sein, wenn diese aber von den Betroffenen nicht angenommen und umgesetzt werden, sind sie sinnlos. In der Tab. sind die Elemente der „combination prevention“ angeführt. Education und Kondom-/Femidomgebrauch bleiben unerlässlich im Kampf gegen HIV. Obwohl dies seit Jahrzehnten kommuniziert und propagiert wird, stieg die Inzidenzrate der sexuell übertragenen HIV- Infektionen. So wurden neue Strategien gesucht und gefunden: Die Gabe einer 4-wöchigen HIV-Postexpositionsprophylaxe innerhalb von 72 Stunden nach Kontamination, Zirkumzision, HIV-Schnelltestung und im Falle eines positiven Testergebnisses die Vermittlung der PatientInnen an ein Behandlungszentrum.
Therapie als Prävention: Weltweit anerkannt wurde die „Therapie als Prävention – TASP“. Dahinter verbirgt sich die stark reduzierte Infektiosität HIV-positiver Menschen unter Therapie. Myron Cohen publizierte 2011 in NEJM die Ergebnisse der HPTN052-Studie.6 Der Frauenanteil der in Österreich mit HIV infizierten Menschen beträgt 29 %. In der Subgruppe der heterosexuell Infizierten liegt der Frauenanteil bei 50.8%.” Die HIV-positiven PartnerInnen in 1.763 serodiskordanten Paaren wurden in 2 Arme randomisiert: jene, die sofort mit antiretroviralen Medikamenten behandelt wurden (Frühtherapie), und jene, die erst nach einem CD4-Zellzahlabfall auf unter 250/µl oder dem Auftreten von AIDS-assoziierten Erkrankungen (Spättherapie) behandelt wurden. Von 28 PartnerIn-assoziierten Infektionen ereigneten sich 27 im Spättherapie-Arm und nur eine im Frühtherapie-Arm. Dies ergibt eine Reduktion des Transmissionsrisikos durch frühe HIV-Therapie um 96,3 %.
Präexpositionsprophylaxe: Die Präexpositionsprophylaxe (PrEP) sorgt seit geraumer Zeit für heftige Diskussionen unter HIV-BehandlerInnen. Hierbei handelt es sich um die Gabe von zwei antretroviralen Substanzen in einer Tablette 1-mal täglich. Eingenommen wird diese von HIV-negativen Menschen, die ein erhöhtes Risiko haben, sich mit HIV zu infizieren. Der PrEP-Einsatz bringt bei Men having Sex with Men (MSM) eine 44%ige Risikoreduktion7, je höher die Adhärenz, desto höher der protektive Effekt. Rezente Daten der FDA zeigen eine relative Risikoreduktion bei messbarem intrazellulären Medikamentenspiegel von 75 bis 100 %. Die Effektivität der PrEP für serodiskordante Paare und heterosexuelle Menschen wurde ebenso nachgewiesen. Damit kommen wir der Vision einer HIV-freien Gesellschaft wieder ein Stück näher.
Weitere Informationen: www.shetoshe.org