Klinische Highlights zur Brustkrebstherapie
 Studie 12 der ABCSG
Studie 12 der ABCSG
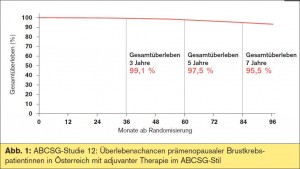
Eine der vielleicht bekanntesten ABCSGStudien wurde am SABCS von Univ.-Prof. Dr. Michael Gnant präsentiert und hat als wesentliches neues Ergebnis nach einem Follow- up von 84 Monaten nunmehr auch einen Überlebensvorteil darstellen können.1 Besonderheiten der Studie sind die kombinierte endokrine Therapie über 3 Jahre (Tamoxifen + ovarielle Suppression mit dem LH-RH-Analogon Goserelin) sowie die Zugabe des Bisphosphonats Zoledronsäure als Bestandteil der endokrinen Therapie upfront. Zoledronsäure ist in vieler Hinsicht eine wertvolle Maßnahme zur Prävention und Therapie des Knochenverlusts, zur Verbesserung des onkologischen Therapieerfolgs in der Postmenopause (AZURE- Studie), in der Prämenopause (ABCSG- 12) und zur Reduktion des Brustkrebsrisikos bei gesunden Frauen (Gnant M., J Clin Oncol 2010; 28:3548-3551). In die Studie inkludiert waren Patientinnen mit guter/intermediärer Prognose (mehrheitlich T1-Tumoren, nodal negativ, G1/2). Im Ergebnis zeigen die aktuellen Daten erneut, dass durch Zugabe von Zoledronsäure zur adjuvanten endokrinen Therapie eine Verbesserung des krankheitsfreien Überlebens (multivariate Auswertung: HR 0,71, p = 0,011) erreicht wird, was lokoregionale und kontralaterale Rezidive sowie Fernmetastasen betrifft. Die Risikoreduktion setzt zu einem frühen Zeitpunkt ein und zeigt im Follow-up einen nahezu gleichbleibenden Verlauf auf hohem Niveau quer durch verschiedene Subgruppen. Eine Ausnahme ist die Subgruppe der Patientinnen über 40 Jahre, bei denen der Benefit durch Zoledronsäure größer ist als bei Patientinnen unter 40 Jahren, was hypothetisch darauf zurückgeführt wird, dass eine komplette endokrine Suppression, die bei jüngeren Patientinnen u. U. nicht vollständig gelingt, eine Voraussetzung für die Bisphosphonat-Wirkung sein kann. Diese These lässt sich auch gut mit den Daten der AZURE-Studie in der Postmenopause in Einklang bringen. Wesentlich ist die Tatsache, dass die endokrine Therapie, wie sie in Österreich bei prämenopausalen Brustkrebspatientinnen praktiziert wird, ausgezeichnete 7-Jahres-Überlebensraten von 95,5 % erzielt (3-Jahres-Überleben: 99,1 %; ), durch Zoledronsäure noch einmal verbessert wird (multivariate Auswertung nach 84 Monaten: HR: 0,61; p = 0,033) und bei dem beschriebenen Patientengut ohne Chemotherapie auskommt. Ähnlich wie beim krankheitsfreien Überleben setzt der Benefit für das Gesamtüberleben früh ein und bleibt über die Zeit auf hohem Niveau stabil.
CLEOPATRA-Studie mit Pertuzumab
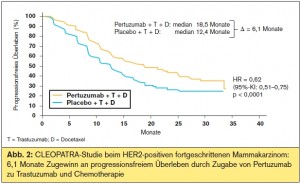
Im Namen der CLEOPATRA-Studienärzte wurden von J. Baselga die Ergebnisse der Phase- III-Zulassungsstudie mit Pertuzumab als First-Line-Therapie HER2-positiver Brustkrebspatientinnen vorgestellt.2 Pertuzumab bindet an ein anderes HER2-Epitop als Tras – tuzumab, verhindert die Dimerisierung des HER2-Rezeptors mit anderen Mitgliedern der HER-Familie, insbesondere die HER2-HER3- Dimerisierung, die unter den möglichen Optionen die stärksten proliferativen Signale hervorruft. Nachdem Trastuzumab die Dimerisierung nicht unterbindet, wurde mit Pertuzumab ein Wirksynergismus erwartet, der sich auch eindrucksvoll bestätigt hat. In der CLEOPATRA-Studie konnte die Kombination aus Pertuzumab + Trastuzumab + Docetaxel (gegenüber der Therapie ohne Pertuzumab) das progressionsfreie Überleben um 6,1 Monate verbessern (HR: 0,62; p < 0,0001), was als bislang größter Erfolg einer First- Line-Therapie des HER2-positiven Mammakarzinoms hervorgehoben und am SABCS entsprechend akklamiert wurde. Die Risikoreduktion war unabhängig davon, ob Patientinnen mit Trastuzumab (neo)adjuvant vorbehandelt waren oder nicht in beiden Fällen vergleichbar. Die Ansprechraten konnten auf 80,2 % gesteigert werden (p = 0,0011), und das Mortalitätsrisiko wurde in der vorab geplanten Interimsanalyse um 36 % verringert (p = 0,0053).
Update BOLERO-2-Studie mit Everolimus
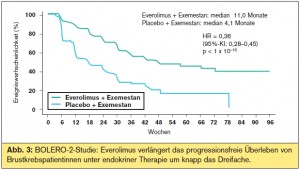
G. N. Hortobagyi hat ein Update der BOLERO- 2-Studie3 präsentiert, die den mTOR-Inhibitor Everolimus in Kombination mit Exemestan bei Hormonrezeptor-positiven, HER2- negativen postmenopausalen Patientinnen untersucht, die bereits mit einem nicht-steroidalen Aromatasehemmer (adjuvant oder als First- Line-Therapie oder beides), mit Fulvestrant oder mit Tamoxifen vorbehandelt waren. Die Studie kann einen Paradigmenwechsel insofern einleiten, als das Standardvorgehen im metastasierten Setting HER2-negativer hormonsensitiver Mammakarzinome bislang aus der sequenziellen Gabe antihormoneller Monotherapien bestand, wobei der Therapieerfolg mit jeder nachfolgenden Therapielinie geringer wird und Resistenzsituationen eintreten können. Everolimus hat bereits in der neoadjuvanten Phase-II-Studie in Kombination mit Letrozol die Ansprechraten auf die endokrine Therapie erhöht und antiproliferative Effekte erzielt (Ki67-Reduktion) und in Kombination mit Tamoxifen in der Phase-II-Studie TAMRAD das progressionsfreie und das Gesamtüberleben von Aromatasehemmer-vorbehandelten Patientinnen verlängert. Die aktuelle Auswertung inkludiert Patientendaten bis Juli 2011 mit einem medianen Follow-up von 12,5 Monaten. Im Ergebnis bestätigt die Auswertung des unabhängigen Review-Panels die Verbesserung des progressionsfreien Überlebens durch die Zugabe von Everolimus von 4,1 auf 11,0 Monate (HR: 0,36; p < 1 x 10–16) innerhalb sämtlicher prognostisch relevanter Subgrup pen, die Erhöhung der Ansprechraten von 1,3 auf 12,0 % (p < 0,0001) – relativ wenig, aber mehr als die Hälfte der Patienten haben die Therapiekombination als 4.-Linien- Therapie erhalten – und eine Verbesserung des klinischen Benefits von 25,5 auf 50,5 % (p < 0,0001). Es wäre nicht unwahrscheinlich, dass diese Daten zu einem Überlebensvorteil führen werden, zumal ein Unterschied im Gesamtüberleben bereits vorhanden ist, auch wenn erst ein Drittel der Ereignisse eingetreten ist. Ein anderer Punkt ist die Tatsache, dass aus einer bislang nebenwirkungsarm verabreichten endokrinen Therapie (seien es Aroma – tasehemmer, Fulvestrant oder Tamoxifen) nunmehr eine Therapie wird, bei der Toxizitäten (Pneumonie, Stomatitis, Fatigue, Diarrhö) zu beachten sind, auch wenn die Lebensqualität in beiden Armen der BOLERO-2-Studie vergleichbar war. Interessant ist die Beobachtung, dass Marker der Knochenresorption, die im Exemestan-Arm erwartungsgemäß erhöht waren, im Kombinations-Arm mit Everolimus erniedrigt waren, was auf einen potenziell knochenprotektiven Effekt schließen lässt (vgl. Kommentar Univ.-Prof. Dr. Günther Steger).
1 Gnant M et al.: Long-term follow-up in ABCSG-12: Significantly improved overall survival with adjuvant zoledronic acid in premenopausal patients with endocrine- receptor-positive early breast cancer. SABCS 2011; Abstract S1-2
2 José Baselga for the CLEOPATRA Study: Group Pertuzumab plus Trastuzumab plus Docetaxel for Metastatic Breast Cancer. N Engl J Med 2012; 366:109-119
3 José Baselga, Martine Piccart, Michael Gnant et al.: Everolimus in Postmenopausal Hormone-Receptorpositive Advanced Breast Cancer. N Engl J Med 2011, 10.1056/NEJMoa1109653 74
Kommentar: Studie ABCSG-12, Prämenopause, kombinierte endokrine Therapie plus Zoledronsäure
In der neuerlichen Präsentation eines Updates der ABCSG-Studie 12 konnte nunmehr, nach 84 Monaten Follow-up, ein Überlebensvorteil durch Zoledronsäure zusätzlich zur endokrinen Therapie (Goserelin und Tamoxifen) erreicht werden. Mit diesem Ergebnis war nicht mehr unbedingt zu rechnen, es zeigt aber, wie sehr eine Intervention in den ersten 3 Jahren nach der Diagnose tatsächlich in der Lage ist, die Biologie des prämenopausalen hormonabhängigen Mammakarzinoms im weiteren Verlauf zu beeinflussen. Die Ergebnisse können ferner als Bestätigung der Subgruppenanalyse der AZURE-Studie in der Postmenopause gesehen werden, in der das Bisphosphonat einen Vorteil beim progressionsfreien Überleben erzielen konnte – wenngleich die Evidenz der AZURE-Daten aufgrund der Subgruppenauswertung eines doch heterogenen Patientenkollektivs schwächer ist. Für ein Kollektiv wie in der Studie 12 der ABCSG ist das Bisphosphonat in niedriger Dosierung, die praktisch keine Nebenwirkungen verursacht – so ist kein einziger Fall einer Kieferosteonekrose aufgetreten –, durchaus als möglicher neuer Therapiestandard aufzufassen und wurde am SABCS auch in diesem Sinn kommentiert. Allfällige Diskussionen betreffen oft die Frage der 3-jährigen endokrinen Therapie. Tatsache ist, dass wir in dieser Studie nicht die Therapiedauer untersucht haben, sondern die Zugabe des Bisphosphonats zur endokrinen Therapie. Man kann festhalten, dass der Studienbeginn zu einer Zeit erfolgte, in der ein Hormonentzug mit Goserelin noch nicht Standard war (Standard war Chemotherapie), bei einer späteren Brustkrebskonferenz in St. Gallen aber als valide Option bestätigt wurde, sodass eine 3-jährige kombinierte endokrine Therapie sicher keine Unterbehandlung ist. Darüber hinaus hat Zoledronsäure nicht nur die Knochendichte erhalten, sondern auch die Tumorbiologie verändert. Ein Diskussionspunkt, dass man durch Hormonentzug sozusagen erst eine pathologische Knochenstruktur schafft, in der das Bisphosphonat dann zur Wirkung kommt, greift insofern nicht, als Zoledronsäure ja von Anfang an eingesetzt wurde, das heißt eine Verminderung der Knochendichte war keine Voraussetzung für den therapeutischen Effekt: Die Knochendichte wurde erhalten und gleichzeitig ein Überlebensvorteil erzielt.
Studie CLEOPATRA, HER2-positives Mammakarzinom, Pertuzumab in Kombination mit Trastuzumab
Zur neuen Generation der HER2-Inhibitoren zählt neben TDM1, einem Fusionsprotein aus Trastuzumab mit einem Zytostatikum, aktuell vor allem Pertuzumab, das an den HER2-Rezeptor bindet und die Dimerisierung mit anderen Rezeptoren der HER-Familie verhindert, insbesondere mit HER3. Es ist zu erwarten, dass die Substanz bald zur Verfügung stehen wird, zumal in der CLEOPATRA-Studie durch Zugabe von Pertuzumab ein eindeutiger Wirkvorteil erzielt wurde, was den Zulassungsprozess der FDA sicher beschleunigen wird. Der Therapiebedarf HER2-positiver Patientinnen nimmt zu, nachdem im Multiple-Line-Konzept durch Beibehalten HER2-aktiver Substanzen immer wieder Wirksynergismen mit verschiedenen Chemotherapien oder durch Chemotherapie- freie Kombinationen untereinander möglich sind. Seitens der ABCSG können wir auf eine Kooperation mit der BIG-Studiengruppe verweisen, mit der wir Pertuzumab in der adjuvanten Situation zusätzlich zu Trastuzumab plus Chemotherapie evaluieren wollen, die Studie soll noch dieses Jahr starten. Die Datenlage spricht dafür, dass wir mit der neuen Therapieoption eine weitere relevante Prognoseverbesserung HER2-positiver Patientinnen erreichen können.