Medikamententoxizität – Antibiotika und Leber
Grundlagen der Hepatotoxizität
Präexistente hepatische Komorbiditäten und extrahepatische Kofaktoren wie Polymedikation, Adipositas (BMI) und Alter erhöhen die Sensibilität für die medikamentöse Toxizität („second hit“) und können den Verlauf ungüns – tig beeinflussen. Antibiotika stehen in der Reihenfolge der Medikamentengruppen mit häufiger Hepatotoxi – zität gemeinsam mit den NSAR im Vordergrund, während die „Hitliste“ der Einzelsubstanzen als Ursache schwerer Leberschäden von Paracetamol und Phenprocoumon ange – führt wird.
Nach der Pathogenese werden zwei Formen der Hepatotoxizität (HT) unterschieden:
• Die intrinsische HT ist dosisabhängig und damit bis zu einem gewissen Grad vorhersehbar (z. B. Paracetamol).
• Die idiosynkratische HT ist nicht dosisabhängig und damit nicht vorhersehbar. Sie wird durch andere Faktoren wie Genpolymorphismen metabolisierender Enzym – systeme (Cytochrom-P450-Enzym), HLA-Typ und Medikamenteninteraktionen beeinflusst.
Rolle des Cytochrom-P450-Enzymsystems: Die Leber ist das Organ mit dem höchsten CYPGehalt, wovon das CYP3A4 der wichtigste Vertreter ist, etwa 60 % der Arzneimittel sind Substrat dieser Enzymisoform. Antibiotika können über das CYP-System metabolisiert werden, sie können es dabei auch induzie ren (z. B. Rifampicin, aber auch Alkohol) oder hemmen (z. B. Makrolide). Aktivität und Kapazität des CYP-Systems nehmen mit steigendem Alter ab. Die Enzyminduktion dauert meist länger (Wochen) und äußert sich häufig in einem induktiv geprägten Enzymmuster mit überwiegender Erhöhung der _-GT ohne klinische Signifikanz und ist Ausdruck einer adaptiven Reaktion. Bedeutsam ist der Umstand, dass durch die Induktion oder Inhibition metabolisierender Enzymsysteme andere gleichzeitig verabreichte Arzneimittel und deren Metaboliten beeinflusst werden können (potenziell erhöhte Isoniazid- Toxizität durch CYP450-Induktoren wie Rifampicin).
Formen der Antibiotika-induzierten Hepatotoxizität (nach Zollner):
• unspezifische Erhöhung von _-GT u. ALT (50 % bei Clindamycin, bis 20 % bei Isoniazid, 15 % bei Ciproxin)
• akute/fulminante/chronische Hepatitis
• akute/chronische Cholestase:
– blande Cholestase: Fusidinsäure
– inflammatorische Cholestase: Flucloxacillin, Erythromycin, AmoxiClav
– Duktopenie (VBDS – Vanishing Bile Duct Syndrome): Tetrazykline, Trimethoprim/Sulfamethoxazol
– „Pseudo“-Cholelithiasis: Ceftriaxon
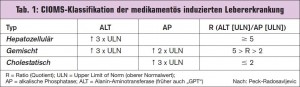
Nach der CIOMS-Klassifikation (Council for International Organisation of Medical Sciences) lassen sich anhand der Konstellation von ALT (GOT) und alkalischer Phosphatase (AP) 3 typische Kategorien der medikamentös induzierten Hepatotoxizität unterscheiden: hepatozellulär, gemischt und cholestatisch (> Tab. 1).
Diagnostik: Risikopatienten für eine AB-induzierte Hepatotoxizität sind vor allem jene mit vorausgegangener hepatotoxischer Reaktion auf Antibiotika, ältere Patienten (> 65 J.) mit Polymedikation (einschließlich alternativer und herbaler Arzneien), exzessiver Alkoholkosum sowie Patienten mit präexistierender Lebererkrankung (Risiko der Dekompensation der Leberfunktion).
Ein Anstieg der Transaminasen über das Dreifache des oberen Normwertes (Upper Limit of Norm – ULN) in Verbindung mit Ikterus (Bilirubin > 2 x ULN) ist mit einer schlechten Prognose und mit einer Mortalität von ~10 % assoziiert („Hy’s Law“, benannt nach dem Pathologen Hyman Zimmermann).
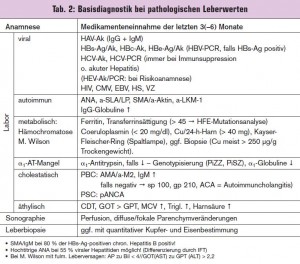
Da der Leberschaden mit einer beträchtlichen Latenz auftreten kann (idiosynkratische Toxizität nach wenigen Tagen bis zu mehreren Monaten möglich), kommt der exakten Medikamenten – anamnese über einen Zeitraum der letzten 6 Monate besondere Bedeutung zu.
Die laborchemische hepatologische Basisdiagnostik (> Tab. 2) dient vor allem dem differenzialdiagnostischen Ausschluss anderer Lebererkrankungen und wird durch die bildgebende Diagnostik und Leberbiopsie komplettiert.
Einzelne Antibiotikagruppen: klinische Besonderheiten
Betalaktame (Penicilline, Cephalosporine, Carbapeneme u. Monobaktame): Schwere Leberschäden sind insgesamt sehr selten und können sowohl hepatozellulär als auch cholestatisch bzw. gemischt sein. Für Flucloxacillin scheint ein etwas höheres Risiko einer cholestatischen Hepatitis zu bestehen.
• Amoxillin/Clavulansäure: Die Kombination des Betalaktamaseinhibitors Clavulan- säure mit Amoxicillin erhöht das Risiko für eine Hepatoxizität erheblich (5–9-fach höher für die Kombination als für Amoxicillin allein). AmoxiClav ist für 13–23 % der medikamenteninduzierten Leberschäden verantwortlich. Typisch ist das verzögerte Auftreten der Symptome, was die frühe Diagnose erschweren kann. Der klinische Verlauf ist meist benigne und zeigt üblicherweise ein cholestatisches oder gemischt hepatozellulär-cholestatisches Reaktionsmuster.
Bei verlängerten oder wiederholten Therapien und einem Alter > 65 Jahren ist das Risiko einer Hepatotoxizität besonders deutlich erhöht.
Weibliches Geschlecht, Alter und die Assoziation zu gewissen HLA-Haplotypen scheinen einen cholestatischen Verlauf zu begünstigen.
• Ceftriaxon: Erwähnenswert ist die für diese Substanz spezifische „Pseudocholeli – thiasis“ durch Ceftriaxon-Bilirubin-Kalzium- Präzipitate in großen Gallengängen und der Gallenblase, die manchmal zufällig, bisweilen auch mit biliären Komplikationen einhergehen können. Junge Frauen scheinen von dieser Nebenwirkung besonders betroffen zu sein.
Makrolide, Ketolide, Lincosamide: Makrolide (Erythromycin eher als Clarithromycin, Azithromycin und Roxithromycin) können eine cholestatische Hepatitis oder ein Vanishing Bile Duct Syndrome (VBDS) auslösen.
Die Erythromycin-induzierte Hepatotoxizität beruht vermutlich auf einer intrinsischen Reaktion und Hypersensitivität. Cholestatische und gemischte Verläufe wurden beschrieben. Überdies scheint die Art der chemischen Verbindung eine Rolle zu spielen (häufigere Toxizität von Erythromycin-Estolat). Telithromycin (Ketek®), ein Ketolid, sollte auf Grund seiner ausgeprägten Hepatotoxizität nur in Ausnahmefällen verwendet werden.
Chinolone: können moderate Anstiege der Transaminasen verursachen, schwere Leberschäden werden auch bei fortgeschrittenen Lebererkrankungen nur selten berichtet. Da sie in der Galle hohe Konzentrationen erreichen, sind sie für die Therapie der bakteriellen Cholezystitis und Cholangitis geeignet. Moxifloxacin wird als einziger Vertreter dieser Substanzklasse über die Leber metabolisiert.
Tetrazykline, Sulfonamide, Trimethoprim: Frühere Meldungen über schwere Lebertoxizitäten von Tetrazyklinen waren durch die hochdosierte intravenöse Applikation bedingt, während die orale Therapie in „normaler“ Dosierung nur selten signifikante Leberschäden verursacht. Minocyclin kann eine idiosynkratische Sofortreaktion mit ALT-Anstieg, Eosinophilie und Dermatitis, aber auch eine Spätreaktion mit SLE-ähnlichem Syndrom auslösen. Doxycyclin ist geringer hepatotoxisch als Tetracyclin. Die Hepatotoxizität der Sulfonamide ist gut dokumentiert und durch eine cholestatische oder gemischt cholestatisch-hepatozelluläre Reaktion geprägt. Das gilt auch für Cotrimoxazol, die Fixkombination eines Sulfonamids mit Trimethoprim, das auf Grund des seltenen aber bedrohlichen Lyell-Syndroms ohnehin nur mehr für die Prophylaxe und Therapie der Pneumocystis-Infektion verwendet werden sollte.
Einzelsubstanzen:
• Linezolid: Eine prolongierte Therapie mit Linezolid wurde mit schweren Leberschäden und histologischem Nachweis einer mikrovesikulären Steatose assoziiert, andererseits zeigten zwei rezente Publikationen aus Japan, dass die Koexistenz einer chronischen Lebererkrankung das Risiko für eine Thrombozytopenie unter Linezolid (meist bei Therapiedauer > 14 Tage) signifikant erhöht.
• Clindamycin: Meistens (50 %) treten nur asymptomatische Anstiege der Transaminasen und der GGT auf, die sich auch bei fortgesetzter Therapie normalisieren, aber es sind auch schwere cholestatische Hepatitiden beschrieben.
Tuberkulostatika: Da die tuberkulostatische Therapie (mit Ausnahme der INH-Prophylaxe bei latenter Tbc und immunsuppressiver Therapie) eine Kombination mehrerer Substanzen erfordert, ist die Identifikation der hepatotoxischen Komponente schwierig. Risikofaktoren für eine gesteigerte Hepatotoxizität sind Alter > 60 y, Alkoholabusus, chronische Lebererkrankungen (bes. Virushepatitis), weibliches Geschlecht, Malnutrition, HIV-Infektion und potenziell hepatotoxische Ko-Medikationen (z. B. Paracetamol).
• Isoniazid, Pyrazinamid: Beide Substanzen besitzen eine gut dokumentierte Hepatotoxizität, die sich vor allem in der Kombination mit Rifampicin manifestiert (Rifampicin induziert das CYP450-System und kann dadurch die Produktion von reaktiven INH-Metaboliten erhöhen).
• Rifampicin: Im Vergleich zu Pyrazinamid und Isoniazid ist Rifampicin geringer hepatotoxisch, wobei in einer rezenten Studie < 2 % der Patienten erhöhte Transaminasen aufweisen (im Vergleich 4–5 % für INH und Pyrazinamid).
• Ethambutol und Streptomycin gelten als nur sehr gering hepatotoxisch.
FACT-BOX
• In Relation zur Häufigkeit des Einsatzes von Antibiotika verbleiben relevante assoziierte Leberschäden selten und sehr schwere Lebertoxizitäten sehr selten.
• Das verzögerte Auftreten der Leberdysfunktion kann die Diagnose erschweren und erfordert häufig eine umfangreiche differenzialdiagnostische Abklärung bis hin zur Leberbiopsie.
• Eine temporäre niedrig dosierte Steroidtherapie kann bei protrahiertem oder schwerem Verlauf von Vorteil sein.
Literatur: – Leitner, Graninger, Thalhammer: Hepatotoxicity of Antibacterials – Pathomechanisms and Clinical Data; Infection 2010; 38 – R. Andrade, P. Tulkens: Hepatic safety of antibiotics used in primary care. J Antimicrob Chemother 5/2011 – Roth, Ganey: Intrinsic vs. Idiosyncratic Drug-induced Hepatotoxicity. J Pharmacol Exp Ther 3/2010 – Canbay et al.: Acute Liver Failure in a Metropolitan Area in Germany. Z Gastroenterol 2009; 47:807-813 – Larson A.: Drugs and the Liver – Patterns of druginduced liver injury. UpToDate 5/2011 – Graninger et al.: Experten-Statement – Hepatotoxizität von Antibiotika. ÖAZ Supplementum, Juli 2008