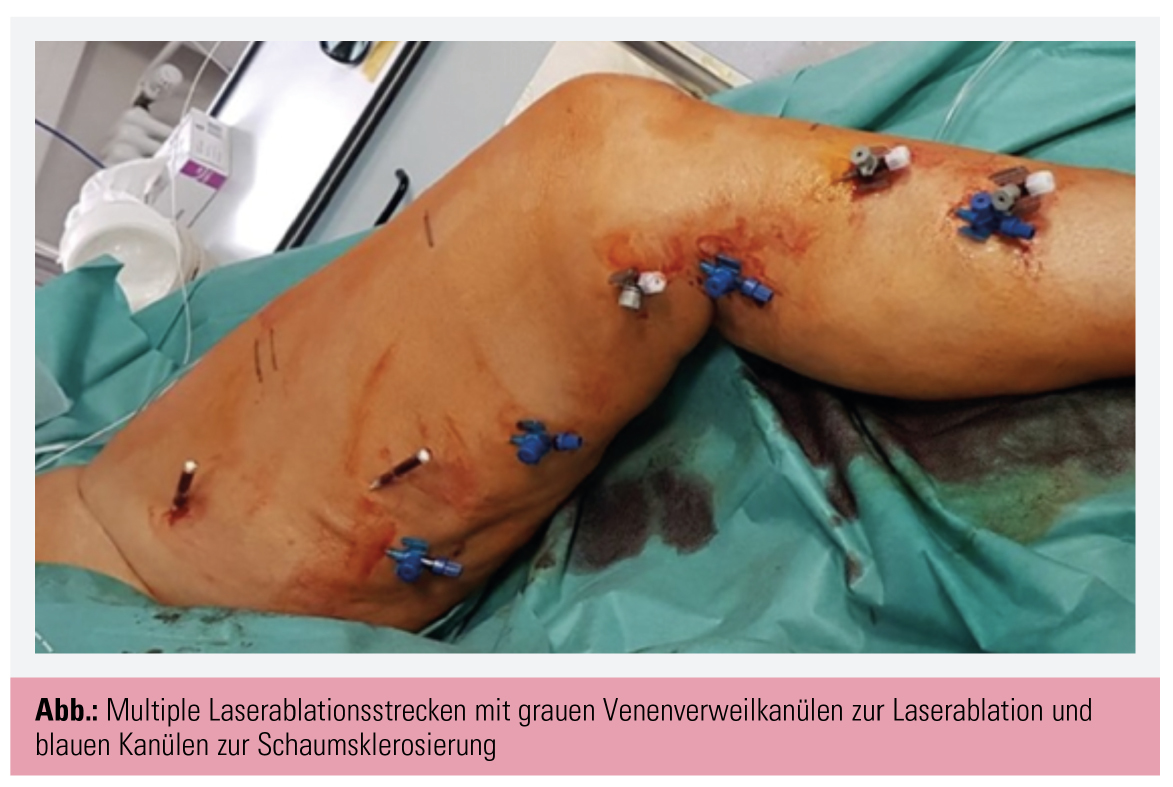
Minimalinvasive Therapie der Varikose
Unter dem Begriff der chronisch venösen Insuffizienz werden alle Krankheitsbilder der Beinvenen zusammengefasst, bei denen es durch Klappenundichtigkeit zur Ausbildung von pathologischen Veränderungen der Venen selbst, aber auch des umliegenden Gewebes kommt. Beinschwellung, Druckempfindungen und sekundäre Hautwachstumsschäden (Stauungsdermatose, Dermato-Lipo-Fascio-Sklerose und Atrophie blanche) – bedingt durch den erhöhten Gewebsturgor – kennzeichnen höhere Erkrankungsstadien bis hin zum Ulcus cruris venosum an typischer Lokalisation im retromalleolären medialen und lateralen Knöchel. In diesen Fällen wird eine Behandlung empfohlen.
Therapieoptionen
Operation
Der klassische Behandlungsansatz der Varikosis stellt bei Stammvenenerkrankungen das Stripping-Manöver nach Babcock, die Seitenastexhairese und die Perforansvenenligatur dar. Modifizierte Operationsverfahren wie das Kryostripping der Stammvene, die endoskopische Perforansligatur (SEPS) sowie die Operation nach SHIVA-Methode haben sich im deutschsprachigen Raum in der Gefäßmedizin nicht breit durchsetzen können. Als minimalinvasiver Ansatz wird für ausgewählte Anatomien die extraluminale Valvuloplastie angeboten, bei der eine Polyurethan-Manschette um die erste insuffiziente Stammvenenklappe gelegt wird, um so die Klappenfunktion wiederherzustellen. Die Erfolgsrate ist mit ca. 80 % beschrieben, die Reinterventionsrate liegt bei 15 %; gelegentlich treten Thrombophlebitiden der Zielvene auf.1, 2
Endothermisch
Die endothermischen Therapieverfahren der Varikosis basieren auf dem Prinzip der Erhitzung der Venenwände und des in der Vene vorhandenen Blutes. Endziel ist die vollständige Denaturierung von Kollagenfasern der Venenwand (92 °C intravasal führen zur totalen Denaturierung), was zum einen mit einer starken Schrumpfung des Gefäßlumens und zum anderen mit einer kompletten Koagulation des Blutes und anderer intravasaler Eiweiße einhergeht.3 Um das umliegende Gewebe zu schonen und den Energieeintrag in das blutgefüllte Lumen der Vene zu minimieren, wird diese mittels 5 °C kalter Tumeszenzlösung komprimiert und gekühlt. Nach dem Ablationsvorgang ist die Vene in der Regel sofort komplett okkludiert.
Endovenöse Laserablation: Die erste Publikation zum Therapieverfahren der endovenösen Laserablation (EVLA) von Krampfadern erschien im Jahr 1999.4 Seitdem sind diverse Arbeiten zum Thema veröffentlicht worden. Diese wurde mit unterschiedlichen Lasergeneratoren, dickeren oder dünneren Laserfasern unterschiedlicher Abstrahlungscharakteristiken, Energiedichten und -pulsdauern und in wechselnden Zielgefäßen (Vena saphena magna, -parva, Seitenastvarizen, Perforansvenen) durchgeführt. Hauptsächlich wurde der Ablationserfolg in den großen und kleinen Stammvenen evaluiert. Die Studienergebnisse der letzten Jahre sehen Laser im höheren Wellenlängenbereich (1.470–2.000 nm) hinsichtlich der Ablationserfolge im Vorteil, da hier H2O Energieabsorptionsmaxima aufweist und so die Venenwand und das Lumen effektiv erhitzt werden. Ältere Lasergeneratoren waren auf Hämoglobin als Absorptionsspektrum ausgelegt, dies war weniger effektiv.5 Auch erbrachte der Schritt von Laserfasern ohne Optik im Spitzenbereich (mit Temperaturen um 1.000 °C an der Faserspitze und Karbonisierung und teils Absprengung von Glasfaserfragmenten als Folge) hin zu einfach und später mehrfach radial abstrahlenden Kathetern, welche den hochenergetischen Lichtstrahl auffächern, eine Verbesserung der postinterventionellen Schmerzen, da Perforationen und Einblutungen ins Gewebe weniger wurden.6 Moderne Laserfasern können über 16G-Venenverweilkanülen in die Zielvene vorgeschoben werden, Schleusensysteme sind nicht mehr notwendig. Mittlerweile zeigen Langzeitverschlussraten für die Lasertherapie nach 5 Jahren eine sehr gute Effektivität von 96,7 %.7
Endovenöse Radiofrequenzablation: Das zweite weit verbreitete Ablationsverfahren in Europa stellt die Radiowellenablation – auch Radiofrequenzablation (RFA) genannt – dar. Im Gegensatz zum Laserverfahren wird hier die Hitze über ein Thermoelement unter Temperaturmonitoring an der Sondenspitze appliziert. Vorteil dieses Verfahrens ist die kurzzeitige, kontrollierte automatische Erhitzung der Vene auf 120 °C. Der Erhitzungserfolg kann während der Ablation kontrolliert werden. Dies hat in großlumigen Venensegmenten den Vorteil des gesicherten Ablationserfolges. Mittlerweile sind verschiedene Ablationssegmentlängen vorhanden, wodurch verschiedene Anatomien behandelt werden können. Die Langzeitresultate sind vergleichbar mit denen der Lasertherapie.8
Die endovenöse „bipolare“ Radiofrequenzablation nutzt hochenergetische Felder ähnlich einer Bipolar-Zange zur Erhitzung, die Energiesteuerung (und damit der Koagulationserfolg) geschieht automatisch via Impedanzmessung an der Katheterspitze. Auch bei diesem Verfahren konnten hervorragende Ablationserfolge nach 5 Jahren gezeigt werden.9
Die Heißdampfablation war ein Nischenverfahren, bei dem unter Hochdruck 120 °C Heißdampf über einen Katheter eingeblasen werden konnte. In Studien konnten gute Ablationserfolge nach einem Jahr dokumentiert werden, auch war der postoperative Schmerz in einer Studie geringer als bei anderen thermischen Verfahren.10 Aufgrund vergleichsweiser komplexer Technik und Problemen mit Verbrennungswunden durch den heißen Katheter bei ungeübten Anwendern hat sich das Verfahren am Markt nicht breit durchsetzen können. Das Nachfolgegerät eines französischen Herstellers, welches sowohl mit Radiofrequenzkathetern als auch Dampfkathetern arbeiten kann, wird aktuell in Studien evaluiert.
Chemisch
Sämtliche endothermische Verfahren eignen sich vor allem für die Stammvene oder den Haupt-Seitenast, von dem kleinere, oberflächlichere Seitenastvarizen entspringen. Ohne die Behandlung der Seitenastvarizen würde ein „unfertiges“ Behandlungsergebnis entstehen, bei dem kleine Seitenastvarizen zurückbleiben. Nicht selten sind auch lediglich Seitenastvarizen ohne Stammvarikosis vorhanden, welche aus dem Venennetz entspringen. Diese Fälle sind die Domäne der Schaumsklerosierung. Die neue S2-Leitlinie zur Sklerotherapie von 05/2019 enthält neuerdings detaillierte Empfehlungen zur Auswahl der geeigneten Konzentration von Aethoxysklerol® (Polidocanol) für die jeweilige Venenanatomie.11 Bei größere Seitenastvarizen über 8–10 mm sollte erwogen werden, diese mit Seitenastexhairese operativ zu entfernen, da hier die Abbaureaktion (Postablationsreaktion) nach Schaumsklerosierung mit thrombophlebitisähnlicher Symptomatik langwierige und teils schmerzhafte Beschwerden hervorrufen kann. Einen anderen Behandlungsansatz stellt die Venaseal®/VariClose®-Therapie dar. Die Okklusion wird hier durch das Verkleben mit modifiziertem „Sekundenkleber“ (N-Butyl-2-Cyanoacrylat) über einen Katheter von der Crosse her nach distal erreicht. Es konnten mittlerweile gute Langzeit-Verschlussraten von 96,4 % in den Stammvenen dokumentiert werden.12 Allerdings treten hin und wieder allergische Fremdkörperreaktionen auf den Klebstoff auf.13
Mechano-chemisch (MOCA)
Das ClariVein®-System ist ein Katheterverfahren, welches die mechanische Schädigung des Endothels durch einen mit 3.500 U/min rotierenden Draht an der Katheterspitze mit der Applikation von Aethoxysklerol® kombiniert. Es kann flüssiger oder aufgeschäumter Wirkstoff injiziert werden. Der Vorteil des Verfahrens liegt in der fehlenden Notwendigkeit einer Tumeszenzanästhesie, da keine schweren Schmerzen durch den Eingriff zu erwarten sind. Die Langzeit-Verschlussraten nach dem Eingriff erreichen nicht ganz die Ergebnisse der thermischen Verfahren.
Nachsorge
In der Regel sind Strümpfe der Klasse II nach einer Varizenbehandlung zur Thromboseprophylaxe und Schmerztherapie für Zeiträume von 1 Woche bis zu 3 Monaten empfohlen. Aus gleichem Grund folgt nach dem Eingriff oft für einige Tage die Gabe von niedermolekularem Heparin. Um eine endovenöse hitzeinduzierte Thrombose (EHIT) als mögliche Komplikation zu entdecken, empfiehlt sich eine Nachkontrolle im Abstand einiger Tage.14
Resümee
Mit Verbesserungen der sonografischen Bildqualität sind in den letzten 20 Jahren große Fortschritte in der minimalinvasiven Therapie der Varikosis möglich geworden. Eine komplett neue, nichtoperative Behandlungsstrategie mit Kathetereinsatz unter permanenter Sonografiekontrolle hat sich etabliert und wird weiter optimiert. Deren Ergebnisse sind im Vergleich mit der klassischen Operationstechnik gleichwertig oder teils überlegen. Die ärztliche Kunst ist es, aus der Vielzahl der Behandlungsoptionen die für die jeweilige Anatomie und den Patienten beste Wahl zu treffen. Zur Vertiefung dieser Übersicht sei auf die erst kürzlich aktualisierte AWMF-S2-Leitlinie zur Therapie der Varikosis15 hingewiesen.