Multimorbidität und Polypharmazie
Multimorbidität bei steigender Lebenserwartung
Studien zeigen klar, dass mit steigender Lebenserwartung auch die Krankheitslast der Bevölkerung zunimmt. Dabei ist die Multimorbidität auch Ergebnis des medizinischen Fortschritts, da wir heute mit der modernen Medizin die krankheitsassoziierte Mortalität verringern, aber dadurch auch chronische Krankheiten „produzieren“.
Damit einhergehend nimmt die Anzahl der im Einzelfall verordneten Medikamente zu, womit das Problem der Polypharmazie sich ebenso stetig ausweitet.1 Die Herausforderung besteht darin, eine Vielzahl von Erkrankungen mit möglichst wenigen Medikamenten und möglichst effektiv zu behandeln.
Polypharmazie, Arzneimittelinteraktionen und UAWs
Polypharmazie und Mortalität gehen Hand in Hand, wobei sich bei dieser Korrelation natürlich die Frage stellt, ob es die mehrfachen Erkrankungen oder die vielen Medikamente sind, die das Sterblichkeitsrisiko erhöhen.2 Hinzu kommt, dass gerade bei älteren Menschen die Therapieadhärenz und Compliance immer kritisch zu betrachten sind. Mehr als 40 % der Betroffenen können nicht alle Medikamente aufzählen, 2/3 wissen auch nicht die richtige Dosierung. Mehrere Untersuchungen belegen, dass unerwünschte Arzneimittelwirkungen (UAWs) häufig der Grund für Hospitalisierung sind.3–6
Pharmakodynamische und pharmakokinetische Interaktionen nehmen mit der Anzahl der eingenommenen Medikamente natürlich zu, bei vielen Patienten können bei genauerer Betrachtung häufig eine oder mehrere kritische Kombinationen in dieser Hinsicht gefunden werden.7 Darüber hinaus können UAWs fälschlicherweise auch als neue Erkrankungen gedeutet werden und die Verordnung eines weiteren Medikaments zur Folge haben.7 Es ist evident, dass mit steigendem Alter der Anteil der stationären Aufnahmen wegen UAWs stetig zunimmt.6 Die häufigsten Symptome, die auf Nebenwirkungen zurückzuführen sind, stellen Stürze und Hypotension, Lungenödem, kardiale Dekompensation und Delir dar. Die Liste der Medikamente, die Stürze begünstigen oder delirogen wirken, ist umfangreich.
Bei polypharmazeutisch versorgten Patienten ist immer zu hinterfragen, ob durch die Interaktion der Medikamente potenziell lebensbedrohliche Folgen auftreten könnten oder im Alter häufig vorliegende Symptome oder Erkrankungen ausgelöst oder verstärkt werden können. Verschiedene Laborparameter bzw. deren Auslenkungen können ebenso (Warn-)Signale für UAWs sein und als solche dienen (Tab. 1).
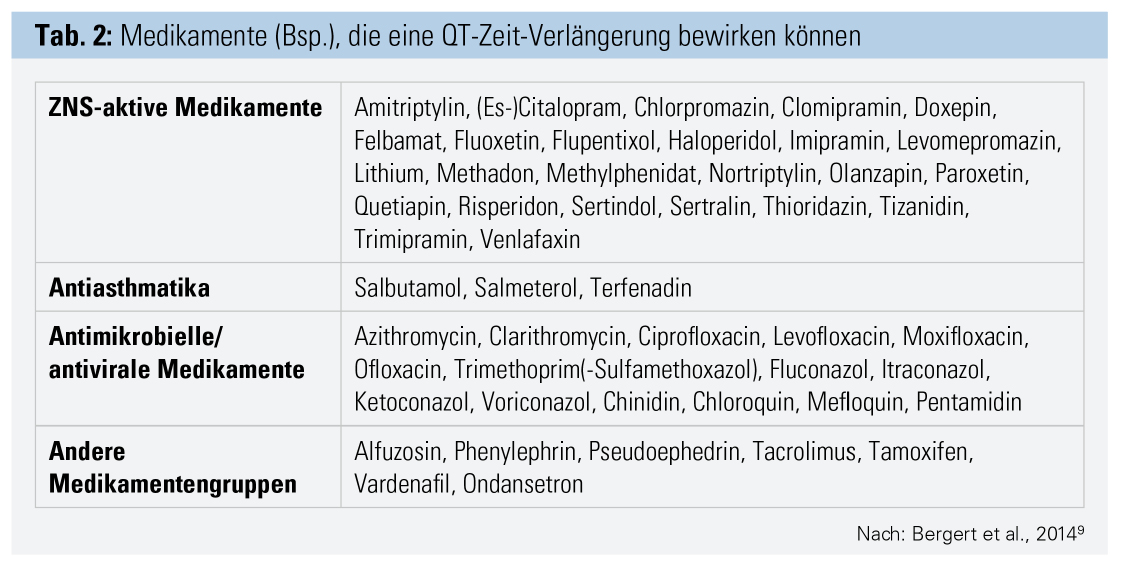
Ebenso sind Organfunktionen, insbesondere die Nieren- und Leberfunktion, zu überwachen, aber auch die Auswirkung auf die kardiale Reizleitung kann bedrohliche Folgen haben. Eine gefürchtete UAW bei nichtkardialen Medikamenten ist eine Verlängerung der QT-Zeit. Medikamente, die eine solche verursachen können, reichen von ZNS-aktiven Substanzen über antimikrobielle/-virale Therapien bis hin zu Immunsuppressiva (Tab. 2).
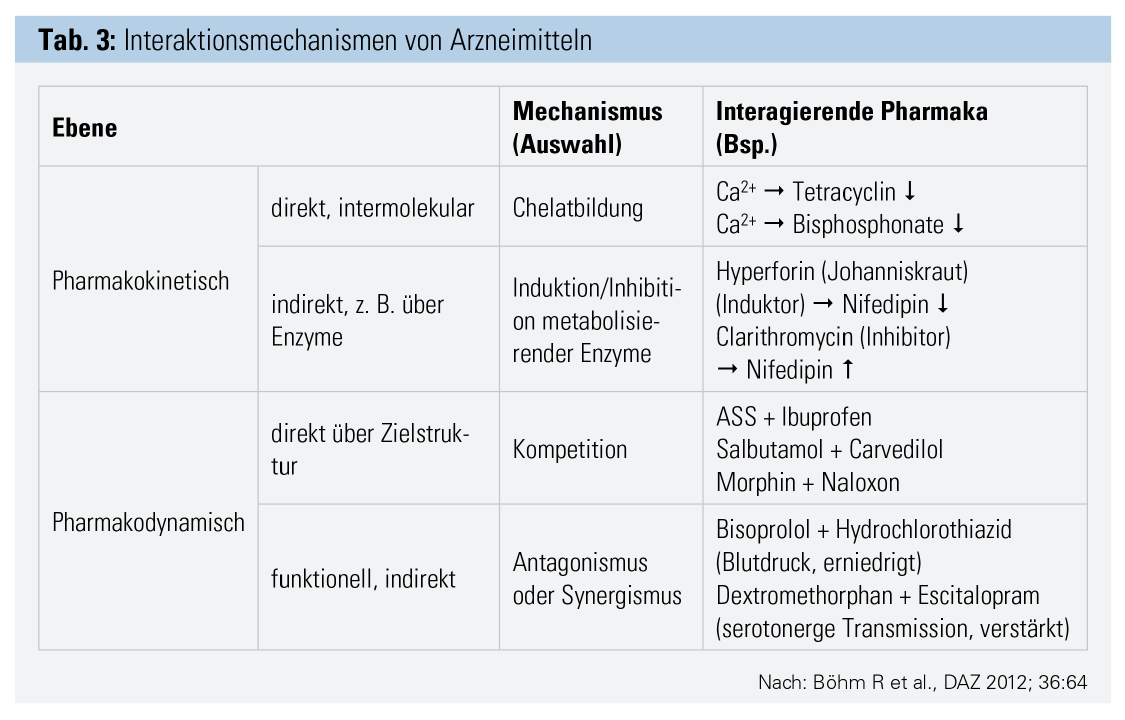
Die Möglichkeiten der Interaktionen sind mehrfach gegeben. So können direkte intermolekulare Reaktionen wie z. B. Chelatbildung die Freisetzung der einzelnen Substanzen aus ihren Formulierungen beeinflussen.
Pharmakokinetische Mechanismen direkt oder indirekt durch Ansatz am gleichen Transportersystem oder Enzymhemmung oder Enzyminduktion beim Metabolismus führen über die veränderte Verteilung bis hin zum beschleunigten oder verlangsamten Metabolismus mit entsprechender Störung oder Beschleunigung der Exkretion.10 Dadurch können Wirkungen verstärkt oder abgeschwächt werden, Gleiches gilt natürlich auch für UAWs (Tab. 3).
Metabolismus und Interaktionen
Daher ist auch immer zu berücksichtigen, ob ein Medikament vorwiegend renal eliminiert wird bzw. wie stark es in der Leber metabolisiert und ebenso ausgeschieden wird.
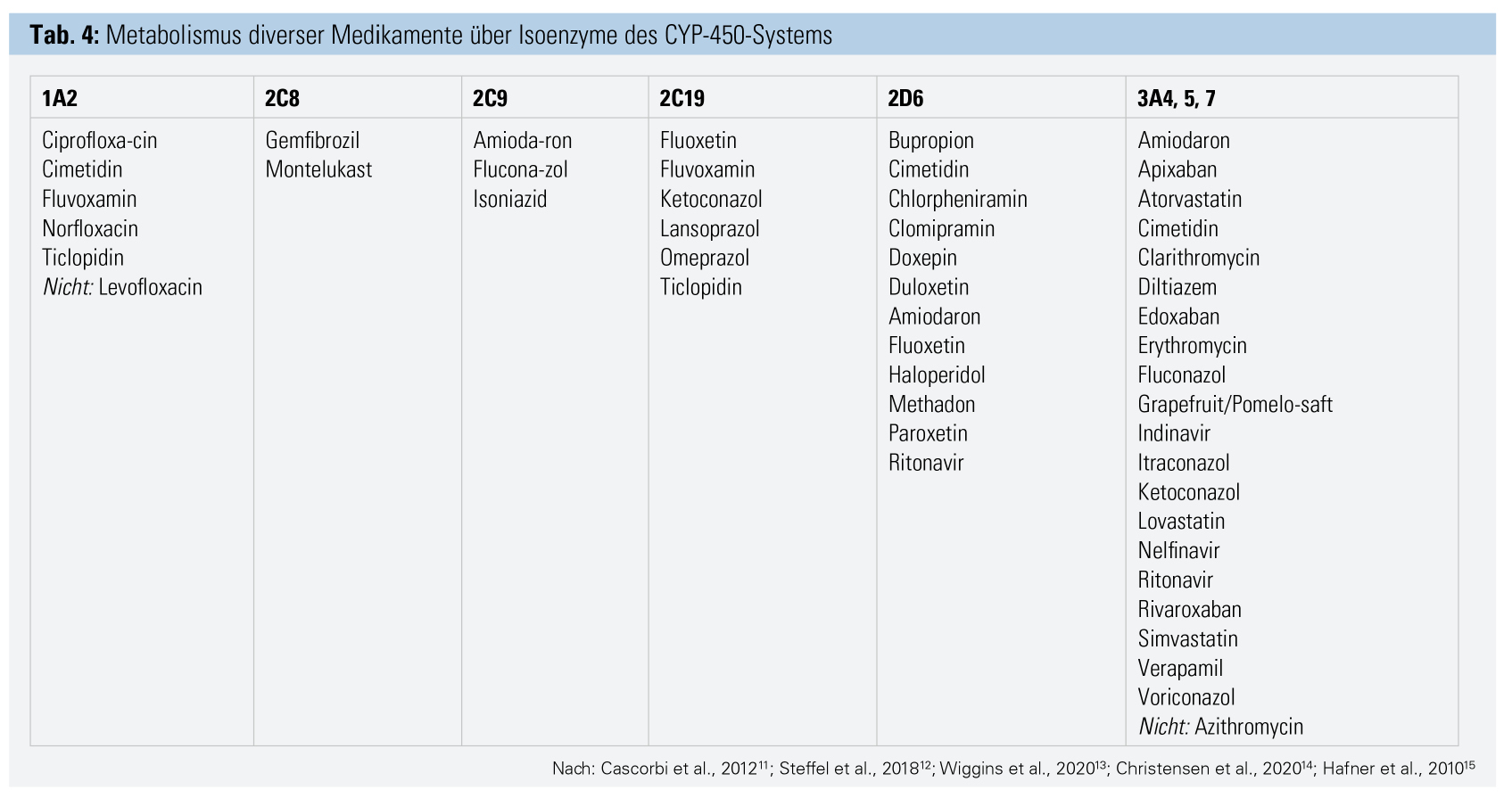
CYP-450-Metabolisierung, P-Glykoprotein: Über das Cytochrom-P-(CYP-)450-System führen die wichtigsten Metabolismuswege bei Arzneimitteln. Interaktionen in diesem Bereich sind meist kompetitiv hemmend, seltener enzyminduzierend. Das Cytochrom-P450-System umfasst mehrere Isoenzyme11, über die zahlreiche Medikamente unterschiedlich metabolisiert werden (Tab. 4). Selbst harmlos erscheinende Phytotherapeutika oder Fruchtsäfte werden über dieses Enzymsystem metabolisiert und können somit den Stoffwechsel vieler Medikamente ungünstig beeinflussen.
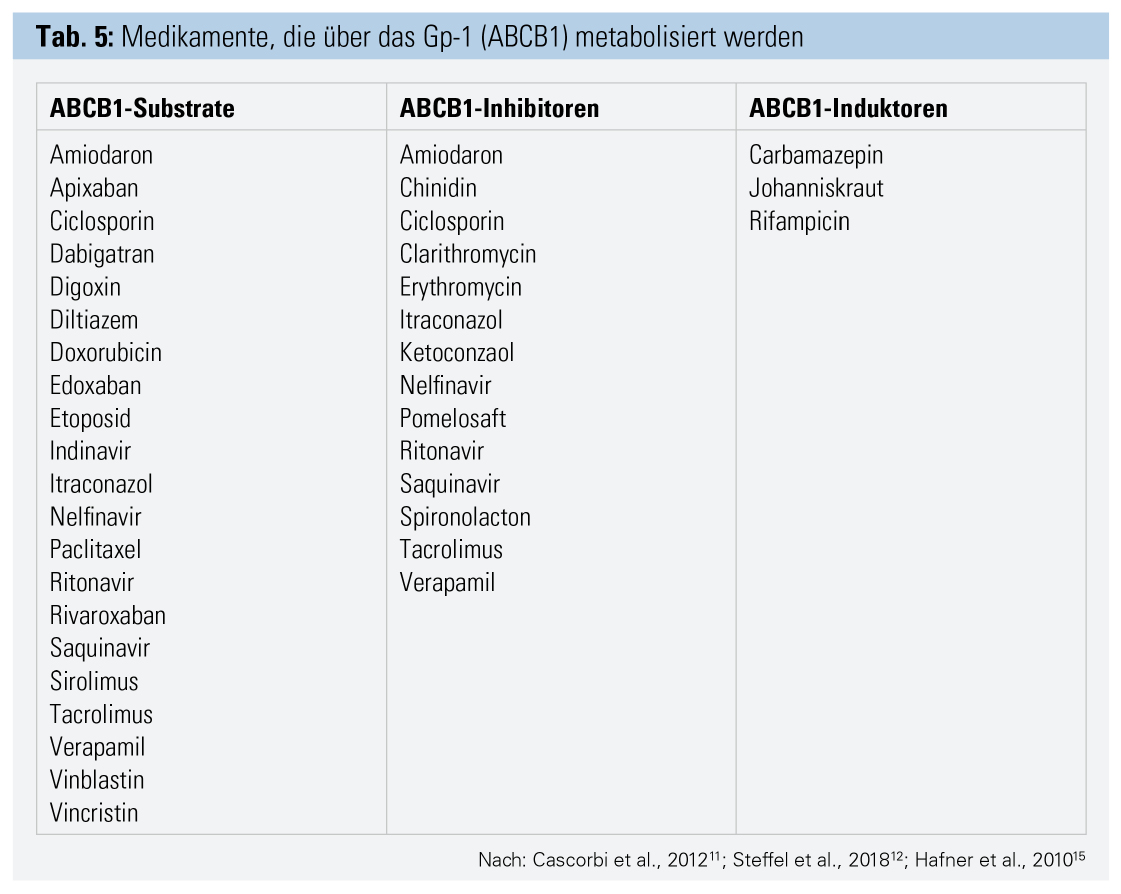
Ein weiterer wichtiger Mechanismus, der oft zu Interaktionen führt, ist die Hemmung eines Transporterproteins, des sogenannten P-Glykoproteins (P-gp). Auch hier sind zahlreiche Medikamente Inhibitoren, vereinzelt auch Induktoren, die sich damit bei gleichzeitiger Verabreichung gegenseitig beeinflussen und so ihr positives wie auch negatives Wirkungsprofil verändern können (Tab. 5).
So sind beispielsweise bei den neuen direkten oralen Antikoagulanzien (DOACs) manche signifikanten Interaktionen bekannt, die durch die Beeinflussung des Metabolismus deren Wirkspiegel und damit das Blutungsrisiko erhöhen. Selbst Antiarrhythmika wie Amiodaron, die ja häufig bei Vorhofflimmern in Kombination mit einer oralen Antikoagulation indiziert sind, können hier interagieren. Eine antimykotische Therapie (insbesondere Itraconazol, Ketoconazol) kann ebenso die Wirkspiegel der DOACs erhöhen. Hingegen verringert Johanniskraut als Gp-1-Induktor die Wirkspiegel und sollte bei Patienten unter DOAC nicht eingesetzt werden.12, 13
Ein weiteres Beispiel ist die Interaktion von Clarithromycin und verschiedenen Statinen über den CYP-450-Abbauweg. Unter Kombination des Antibiotikums mit dem Lipidsenker steigt das Risiko für die dadurch induzierten Myopathien.14
Anticholinerg wirksame Medikamente und Delir: Ein in der Geriatrie allgegenwärtiges Problem insbesondere bei akuten Erkrankungen stellt das Delir dar. Neben der Ortsveränderung, dem akuten Krankheitsprozess und so manchen anderen Umwelteinflüssen können gerade demente Menschen rasch ein Delir entwickeln, das oft durch Arzneimittel verstärkt oder gar induziert wird. Es sind die anticholinergen Wirkungen der Medikamente, welche die Entwicklung des Delirs begünstigen. Je nach Stärke ihrer anticholinergen Last werden die Substanzen heute in 3 Gruppen eingeteilt, insbesondere jene mit anticholinerger Last Grad III sollten bei geriatrischen Patienten vermieden werden (Tab. 6).
Insbesondere die Verabreichung von gastroprotektiven Medikamenten scheint in der modernen Medizin gang und gäbe und oft allein im Umstand einer Polypharmazie begründet zu sein. Bei näherer Betrachtung ist dieser Zugang jedoch kritisch zu hinterfragen. Mittlerweile sind Protonenpumpenhemmer durch ihre niedrigen Kosten zu einer Art Basismedikament für fast jeden Patienten geworden, der mehrere Medikamente einnimmt. Ursprünglich dafür gedacht, den Magen vor ulzerogenen Medikamenten zu schützen (NSAR), werden sie heute aufgrund der freien Verordnung unkritisch breit eingesetzt. Mittlerweile gibt es Daten dafür, dass die Blockade der durchaus physiologisch notwendigen Säurebarriere im Magen mit anderen Risken wie Aspirationspneumonie, Clostridienenteritis, Osteoporose und natürlich auch schlechter Eisenresorption einhergeht. Daher gilt es auch hier insbesondere nur jene Risikopatienten zu identifizieren, die aufgrund bestimmter Medikamente oder aufgrund ihrer Anamnese ein höheres Ulkusrisiko aufweisen.17–19
Umgang mit Polypharmazie im klinischen Alltag
Nicht jede potenziell mögliche Interaktion führt zu klinisch relevanten UAWs. Es gilt die Symptome richtig zu erfassen und zu bewerten, die Kausalität von Nebenwirkungen als Folge einer Interaktion ist nicht immer eindeutig herzustellen, darüber hinaus ist die Entscheidungsfindung sehr aufwändig. Mittlerweile gibt es verschiedene Möglichkeiten (Onlinelisten, Datenbanken), die dazu dienen, die Entscheidungsfindung und Beurteilung dem behandelnden Arzt zu erleichtern. Für den Alltag in der klinischen Praxis haben sich die sogenannte PIM-Liste (Potentially Inappropriate Medication), die FORTA-Liste (Fit fOR The Aged) oder die PRISCUS-Liste als unterstützend erwiesen.
Aber ständig neue Erkenntnisse über die Pharmakologie bis hin zu pharmakokinetischen Unterschieden zwischen einzelnen Individuen machen es immer komplexer, hier eine klare Entscheidungshilfe zu finden. Daher sind wir gefordert, in der Verordnung unserer Medikamente möglichst zurückhaltend zu sein, aber auch die Patienten engmaschig zu kontrollieren und behutsam zu beobachten, ob sie physische, psychische oder laborchemische Veränderungen zeigen, die auf mögliche Arzneimittelnebenwirkungen hindeuten können, um rechtzeitig korrigierend einzugreifen. Wie die Geriatrie generell, so ist auch die Verordnung von Medikamenten im Alter eine Gratwanderung zwischen Nihilismus und Beflissenheit, der bei älter werdenden Menschen naturgemäß immer schmäler wird.