Therapie der chronischlymphatischen Leukämie (B-CLL)
Während sich in der Erstlinientherapie der CLL zuletzt auf Basis eines randomisiert erhobenen Überlebensvorteiles für fitte Patienten FCR (Fludarabin, Cyclophosphamid und Rituximab) als klarer Standard erwiesen hat, sind weiterhin viele Bereiche der CLL-Therapie im Fluss, insbesondere bleiben Fragen nach Maintenance-Strategien, nach geeigneten Konzepten für die relabierte und refraktäre Erkrankung und nach der zukünftigen Rolle von Signaltransduktionsinhibitoren offen.
Wenn bei einer diagnostizierten B-CLL nach den aktuellen Behandlungsleitlinien aufgrund Aktivität oder Stadium eine Therapieindikation vorliegt, sollte die Therapie optimalerweise als kombinierte Chemoimmuntherapie durchgeführt werden. Die Auswahl des Therapieregimes erfolgt hierbei je nach Belastbarkeit und Komorbidität des Patienten. Ein kurzer Überblick über einige sinnvolle mögliche und mit Studiendaten belegbare Therapieabfolgen soll im Folgenden gegeben werden.
First-Line-Therapie
Bei fitten Patienten ist aktuell die Kombination Fludarabin, Cyclophosphamid und Rituximab als Therapie der ersten Wahl anzusehen, da sich in der deutschen CLL8-Studie mittlerweile ein Überlebensvorteil für die mit FCR behandelte Gruppe gezeigt hat. Hier ist jedoch darauf hinzuweisen, dass das Kollektiv, das in der Studie untersucht wurde, durchaus stark nach Fitness selektioniert war und dass auch für diese fitte Gruppe FCR eine durchaus toxische Therapie darstellt. So konnten in der Studie bei 25 % der Patienten nicht alle geplanten 6 Zyklen Therapie mit FCR durchgeführt werden, in fast 50 % der Fälle wurde auch eine Dosisreduktion nötig, und das in einem relativ „gesunden“ und gut belastbarem Patientenkollektiv (charakterisiert durch CIRS < 6 [Cumulative Rating Illness Scale] sowie einer eGFR von > 70 ml/min/KO). In der Praxis lässt sich der Vorteil der Rituximab- Behandlung (die ja der randomisierte Anteil in der CLL8-Studie war) bei weniger belastbaren Patienten allenfalls mit weniger intensiven Chemotherapie „backbones“ verwirklichen. Die Zulassung erlaubt dabei ja die Kombination mit allen anwendbaren Chemotherapeutika (z. B. Bendamustin, Fludarabin, Cyclophosphamid oder auch Chlorambucil).
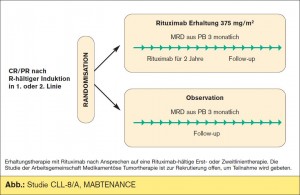
AGMT-Studien CLL-4, CHAIROS, und CLL-8/A, MABTENANCE: Ein durchaus relevantes Problem stellt das Problem des early relapse nach FCR dar, hier ist das Patientensurvival aus bislang dokumentierten Serien (die erste davon aus der Kohorte des MD Anderson Cancer Center) beunruhigend schlecht. Es ist dabei anzunehmen, dass die Relapsrate bei weniger intensiver Initialtherapie (wie oben für weniger fitte Patienten angedeutet) höher sein wird. Für beide Situationen könnte eine Strategie zur Remissionserhaltung Vorteile bringen. Wir haben daher im Rahmen der österreichischen Studiengruppe in der Phase- II-Studie CLL-4 der AGMT (CHAIROS) nach leicht reduzierter FCR-artiger Induktion die Machbarkeit einer 2-jährigen Erhaltung (8 x Rituximab alle 3 Monate) getestet. In der letztes Jahr beim ASH präsentierten vorläufigen Endauswertung zeigte sich eine gute Tolerabilität, mit einer Rate an Infektionen, die nicht über der nach FCR zu erwartenden lag. In der Auswertung des Ansprechens zeigte sich eine signifikante Verbesserung der Responsetiefe, sowohl im klinischen Ansprechen als auch in der Auswertung der MRD-Messungen, sodass das im indirekten Vergleich mit der CLL8 sehr gute PFS durchaus plausibel erscheint. Insbesondere für die Hochrisikogruppe der Patienten mit del11q war das Ergebnis überraschend gut. Aus diesen Daten haben wir die Rationale für eine randomisierte Studie bezogen. Im Rahmen der AGMT-CLL-8/AStudie (MABTENANCE) wird somit aktuell eine Erhaltungstherapie mit Rituximab nach Ansprechen auf eine Rituximab-hältige Erstoder Zweitlinientherapie evaluiert (> Abb.). Wir laden alle herzlich ein, in diese von Österreich aus geführte internationale Studie zu rekrutieren, um diese wichtige Frage beantworten zu können. Alternative Erhaltungsstrategien mit Lenalidomid sind ebenfalls in Testung, die dazu laufenden Studien haben aber einige Probleme in Design und Rekrutierung.
AGMT-Studie CLL5, REVLIRIT: Eine weitere, zuletzt international beachtete Studie der AGMT befasste sich mit einer möglichen Weiterentwicklung von FCR. Die so genannte REVLIRIT-Studie (AGMT-CLL5) hat dabei ein alternatives Erstlinienschema mit Fludarabin, Rituximab sowie der immunmodulatorischen Substanz Lenalidomid etabliert und dabei ein deutlich repräsentativeres Kollektiv rekrutiert (medianes Alter 66 Jahre) als z. B. die deutsche CLL8-Studie (medianes Alter 61 Jahre). Während die Wirksamkeit in dieser Phase-I/II-Studie sehr überzeugend war, zeigten sich überraschenderweise zwei Patientengruppen mit sehr unterschiedlicher Toleranz für Lenalidomid in der Kombination. Diesbezüglich ist es gelungen, aus T-Zell-Analysen einen prädiktiven Faktor für die Tolerabilität zu etablieren, der einen optimierten Einsatz von Lenalidomid in der Zukunft ermöglichen könnte. Diese Daten werden in einem Vortag am ASH 2011 präsentiert werden.
Therapie der relabierten Erkrankung
Im Relaps einer CLL nach vorangegangener Therapie in erster oder auch späterer Linie sind zwei Gruppen zu unterscheiden: Patienten mit längerem rezidivfreien Intervall, für die eine Wiederholung der vorangegangenen Therapie für adäquat gehalten wird und für die oft auch in der Folge weitere Optionen aktiv sind, und Patienten mit relativ raschem Rezidiv, für die die therapeutischen Entscheidungen rasch schwierig werden. In dieser letzten Gruppe sammeln sich oft Patienten mit molekularen Hochrisikofaktoren wie einer Deletion 17p oder mit Mutationen im p53- Lokus. Für solche Patienten ist eine allogene Transplantation je nach klinischer Machbarkeit eine wichtige Option (allenfalls nach OFAR- [Oxaliplatin, Fludarabin, Ara C, Rituximab] oder R-DHAP-Induktion [Rituximab, Dexamethason, Ara C, Cisplatin]).
Antikörpertherapien: Insgesamt sind für Folgetherapien einige Optionen zur Verfügung, darunter erfolgversprechende Therapien mit Antikörpern, allenfalls auch in Kombination mit einem Chemotherapeutikum. Zugelassene Antikörper sind Alemtuzumab (CD52-Antikörper) und Ofatumumab (CD20-Antikörper) (letzteres überwiegend in Monotherapie). In der Vergangenheit ist in Österreich eine Kombination von Alemtuzumab mit Fludarabin getestet worden. Hier zeigte sich, ähnlich einer deutschen Studie, eine recht gute Krankheitskontrolle und ein gutes therapiefreies Überleben vor allem für Patienten, die eine MRD-(Minimal Residual Disease)- Negativität erreichten. Die Toxizität war dabei durchaus beachtenswert, wenn auch mit Erfahrung vernünftig zu handhaben, sodass solche Therapien eher in die Hände erfahrener Zentren gehören. Gerade abgeschlossen ist das Folgeprojekt dieser Studie, eine Kombination mit Bendamustin und Alemtuzumab. Wir erwarten eine erste Auswertung zur Effektivität Mitte kommenden Jahres. Für Patienten mit mehrfachen Rezidiven wird die Situation zunehmend komplex: Hier sind eine Reihe von Optionen in Erprobung, jedoch oft nicht außerhalb von Studien zugänglich. Relevante Erfolge (bei auch bemerkenswerten Toxizitäten) sind mit Kombinationen von Alemtuzumab mit sehr hoch dosierten Steroiden erzielt worden. Als zusätzlich Option erscheint hier Lenalidomid eine Rolle zu erwerben, allenfalls auch in Kombinationen mit CD20-Antikörpern. Besondere Aufregung im Feld verursachen derzeit erste Daten aus der Behandlung mit Inhibitoren des B-Zell-Rezeptorsignalweges, also von Kinasen wie Syk, PI3K und Btk. Diese haben teilweise bemerkenswerte Ansprechraten, vor allem der Lymphknoten, in stark vorbehandelten Kollektiven. Hier ist insbesondere kritisch, dass es bei diesen Substanzen initial durch eine Umverteilung zu massiven Leukozytosen kommen kann, die nicht mit einem Progress verwechselt werden dürfen. Die weitere Entwicklung dieser Substanzen, wohl teilweise in Kombination mit Antikörpern, hat durchaus das Potenzial, die Therapie der CLL im kommenden Jahrzehnt zu revolutionieren.
FACT-BOX
Die Erstlinientherapie fitter CLL-Patienten mit FCR (Fludarabin, Cyclophosphamid, Rituximab) ist derzeit die bestabgesicherte Entscheidung in der CLL-Therapie. Komplexer sind Therapieentscheidungen für weniger fitte Patienten, wo Erhaltungsstrategien oder die Hinzunahme neuer Medikamente eine wichtige Rolle spielen werden. Im Rezidiv wird die Situation durch eine Reihe molekularer Risikofaktoren noch komplexer und wir hoffen auf neue Signaltransduktions- Inhibitoren, die in ersten Studien vielversprechend waren.