Thrombose und COVID-19
Mit über 40 Millionen registrierten Fällen, mehr als 1 Million Toten (Stand: November 2020) und einem weiterhin drastischen Anstieg von weltweit auftretenden Neuinfektionen bleibt der Ausbruch von COVID-19, hervorgerufen durch SARS-CoV-2, eine immense globale Herausforderung für Staaten und ihre Gesundheitssysteme.1 Die Krankheitsverläufe bei Infektion mit SARS-CoV-2 zeigen ein deutlich heterogenes Muster, welches von asymptomatischen Fällen bis hin zu schweren intensivpflichtigen Verläufen reicht.
COVID-19, in vielen Fällen eine rein respiratorische Erkrankung, gilt bei moderater bis schwerer Symptomatik als eine Multisystemerkrankung und betrifft neben Lunge auch Herz, zentrales Nervensystem, Niere und das Gefäßsystem. Bei schwererkrankten PatientInnen findet sich zudem häufig ein derangiertes Blutgerinnungssystem, bezeichnet als „COVID-19-assoziierte Koagulopathie“.2 Das Resultat dieses hämostaseologischen Ungleichgewichts ist ein erhöhtes Thromboserisiko. Speziell tiefe Beinvenenthrombosen und Lungenembolien, welche unter der Krankheitsentität „venöse Thromboembolie“ (VTE) zusammengefasst werden, gehören zu den häufigsten Komplikationen bei PatientInnen mit COVID-19.3 Auch Mikrothrombosen, häufig in situ in den kleinsten Gefäßen der Lunge auftretend, sind pathognomonische Veränderungen, die im Zusammenhang mit COVID-19 beschrieben wurden.
Häufigkeit venöser Thromboembolien bei COVID-19
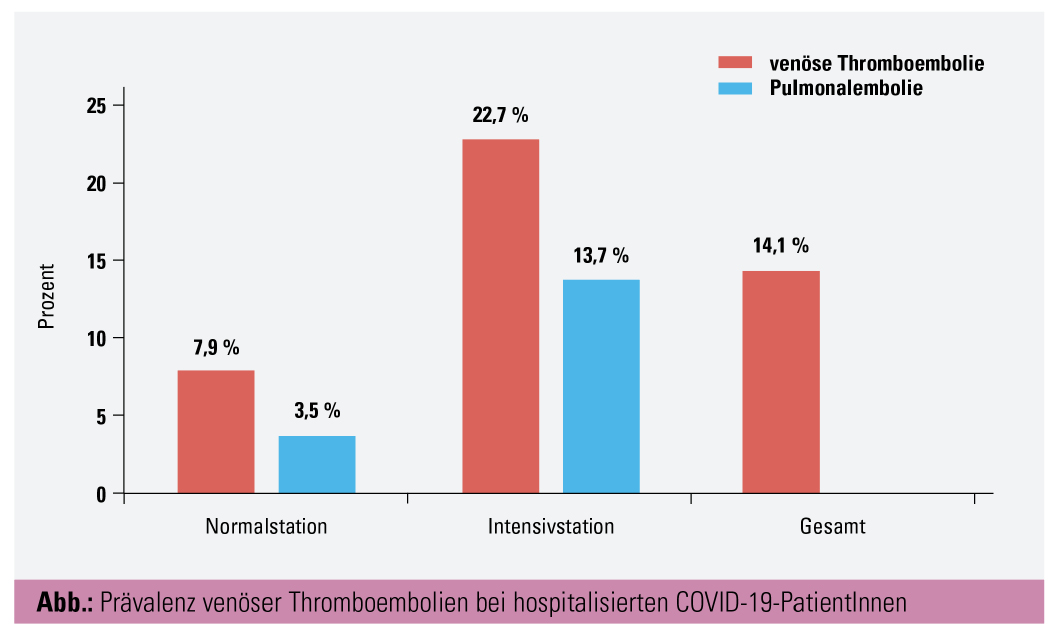
Erste Beobachtungsstudien, vor allem jene bei PatientInnen mit schweren intensivpflichtigen Krankheitsverläufen, zeigten bereits zu Beginn der Pandemie ein deutlich erhöhtes Thromboserisiko.4 Die berichteten Thromboseraten zwischen den einzelnen Studien variierten jedoch stark. In einer systematischen Übersichtsarbeit, welche 86 Studien und über 30.000 PatientInnen umfasst, konnten wir nun erstmals genaue Daten zum Thromboserisiko von hospitalisierten COVID-19-PatientInnen ermitteln (Abb.). PatientInnen, die zwar stationär, aber nicht auf einer Intensivstation betreut werden müssen, haben ein VTE-Risiko zwischen 5 und 11 Prozent. COVID-19-PatientInnen mit schwerem Verlauf erleiden hingegen in 18 bis 28 Prozent der Fälle eine tiefe Beinvenenthrombose oder Lungenembolie.5 Im Vergleich mit ähnlich kritisch kranken PatientInnen mit anderen zugrundeliegenden Erkrankungen scheint das Risiko für eine Thrombose bei COVID-19 erhöht zu sein. Erstaunlicherweise konnte außerdem bei beinahe der Hälfte der stationären COVID-19-PatientInnen durch systematisches Ultraschall-Screening eine Thrombose detektiert werden. Diese Ergebnisse sowie vergleichbare Thromboseraten bei Infektion mit SARS-CoV-1, dem für den Ausbruch der Pandemie von 2003 verantwortlichen Virus, deuten auf einen speziellen zugrundeliegenden Pathomechanismus hin, der für die erhöhte Rate kardiovaskulärer Komplikationen verantwortlich ist.6
Pathomechanismus: Thrombose bei COVID-19
Hohe Werte des Fibrinspaltproduktes D-Dimer, welches als gutes Korrelat für den Schweregrad der Erkrankung identifiziert wurde, weisen auf eine deutliche Verschiebung des hämostaseologischen Gleichgewichts hin, hervorgerufen durch ein sich potenzierendes Zusammenspiel von Inflammation und Blutgerinnung.7 Die durch SARS-CoV-2 verursachte Endothelzellaktivierung und erhöhte Ausschüttung proinflammatorischer Zytokine („cytokine storm“) setzen eine Kettenreaktion in Gang, die das Gerinnungssystem stimuliert, welches wiederum zu vermehrter Aktivierung von inflammatorischen Zellen und Thrombozyten führt und für das prokoagulatorische Zustandsbild dieser Erkrankung verantwortlich ist.8
Der folgende Endothelzellschaden, die unkontrollierte Thrombozytenaktivierung und die durch Immobilisierung hervorgerufene Veränderung des Blutflusses erfüllen somit die Virchow-Trias, welche schon im 19. Jahrhundert als Grundlage für die Entstehung von Thrombosen postuliert wurde. Für die ungewöhnlich hohe und alarmierende Rate an Lungenembolien dienen zwei Erklärungsmodelle: Die hohe Prävalenz tiefer Beinvenenthrombosen in Studien, in denen ein Ultraschall-Screening durchgeführt wurde, deutet einerseits auf ein thromboembolisches Geschehen als Ätiologie der Lungenembolie hin. Andererseits mehren sich die Hinweise, dass in der Computertomografie diagnostizierte segmentale oder subsegmentale Lungenembolien pathophysiologisch eher „In situ“-Thrombosen der Lungengefäße entsprechen. Autopsiestudien legen nahe, dass es sich hierbei um eine lokale, durch die überbordende Inflammation und Immunantwort mediierte, pulmonale Thrombenentstehung handelt. Man spricht in diesem Zusammenhang daher auch von einer „pulmonalen Immunothrombose“.9, 10
Der Einfluss von COVID-19 auf das Gerinnungssystem hat auch eine prognostische Bedeutung. Mittels regelmäßiger Messung (im Abstand von 2 bis 3 Tagen) von Gerinnungsparametern (z. B. D-Dimer, Fibrinogen) lassen sich hospitalisierte PatientInnen mit hohem Risiko für einen schwerwiegenden Verlauf und einer ungünstigen Prognose identifizieren. Therapeutische Konsequenzen bei solchen PatientInnen in Bezug auf eine intensivere Thromboseprophylaxe werden derzeit intensiv diskutiert.
Thromboseprophylaxe und Therapie der VTE bei COVID-19
In Anbetracht der hohen VTE-Raten besteht bereits seit Beginn der Pandemie ein allgemeiner Konsensus für eine Empfehlung zur prophylaktischen Antikoagulation aller hospitalisierten COVID-19-PatientInnen ohne Kontraindikation für eine medikamentöse Blutverdünnung. Niedermolekulares Heparin, die Standard-VTE-Prophylaxe bei internistischen PatientInnen, wird hier als bevorzugtes Agens eingesetzt. Aufgrund fehlender Evidenz aus randomisierten kontrollierten Studien bleibt die Datenlage für eine eskalierte Dosierung und Antikoagulationsstrategie (z. B. verlängerte Prophylaxe nach Spitalentlassung) jedoch nach wie vor schwach. Die Daten aus Beobachtungsstudien legen jedoch nahe, eine höhere, also intermediäre Dosis als Thromboseprophylaxe zu wählen – zumindest bei PatientInnen mit schwerem Verlauf, die eine intensivmedizinische Behandlung benötigen, oder bei PatientInnen mit hohem Risiko für eine VTE. Für eine therapeutische Dosis als Prophylaxestrategie liegt hingegen keine Empfehlung vor. Eine fortlaufende Thromboseprophylaxe für 2–6 Wochen nach Spitalaufenthalt bei PatientInnen mit Risikofaktoren für eine Thrombose, aber niedrigem Blutungsrisiko, kann laut Empfehlungen mancher ExpertInnen und internationaler Fachgesellschaften in Erwägung gezogen werden (Tab.).11 Allerdings melden die ersten Beobachtungsstudien, dass das Thromboserisiko nach der Spitalentlassung deutlich abfällt und niedrig bleibt.12 Neue Studien zu diesen Fragestellungen werden in Kürze erwartet, um die Grundlage für eine Therapieempfehlung zu verbessern.13
Für PatientInnen mit einem leichten bzw. milden Verlauf, die nicht hospitalisiert werden müssen, liegen keine konkreten Empfehlungen für eine primäre Thromboseprophylaxe vor. Die Indikation für eine Thromboseprophylaxe kann jedoch im Einzelfall großzügig gestellt werden, wenn andere Risikofaktoren für eine VTE bekannt sind und das Blutungsrisiko niedrig ist.14
Niedermolekulares Heparin – mehr als nur ein Antikoagulans?
Vor allem in schweren Fällen von COVID-19 spricht man auch von einer „thromboinflammatorischen Erkrankung“. Eine Senkung der inflammatorischen Komponente durch Therapien mit immunmodulierenden Medikamenten gilt somit als maßgebliche Therapiesäule, um das Thromboserisiko zu senken. Die antiinflammatorische Komponente der Heparintherapie könnte somit ein wichtiger Bestandteil der Therapie sein.15 Weiters wird spekuliert, dass die antikoagulatorische Komponente des Heparins nicht nur eine VTE verhindern könnte, sondern auch über eine Reduktion der lokalen Fibrinablagerungen in Organen wie Lunge und Niere dazu beitragen kann, Organversagen zu verhindern.
Liegt ein Verdacht auf eine VTE vor, soll die sonst übliche diagnostische Abklärung eingeleitet werden, um eine tiefe Beinvenenthrombose bzw. Pulmonalembolie auszuschließen. Ein Screening ohne Symptome, zur Detektion einer asymptomatischen VTE, ist nicht empfohlen, auch um das Risiko einer Ansteckung des Gesundheitspersonals zu vermeiden. Bei diagnostizierter VTE sind die Empfehlungen jedoch klar: Eine therapeutische Antikoagulation für mindestens 3 Monate ist indiziert. Diese kann in den meisten Fällen nach spätestens 6 Monaten wieder abgesetzt werden.
Resümee
Das Gerinnungssystem spielt im Verlauf einer COVID-19-Erkrankung eine zentrale Rolle, und Gerinnungsveränderungen können eine prognostische Information für den Krankheitsverlauf liefern. Aufgrund eines Ungleichgewichts des Gerinnungssystems zulasten eines prothrombotischen Zustandsbildes findet sich neben der respiratorischen Hauptsymptomatik ein hohes Thromboserisiko als häufigste kardiovaskuläre Komplikation. 5 bis 11 Prozent der auf einer Normalstation hospitalisierten COVID-19-PatientInnen und 18 bis 28 Prozent der PatientInnen auf einer Intensivstation erleiden im Verlauf des stationären Aufenthalts eine VTE. Eine Thromboseprophylaxe – bevorzugt mit einem niedermolekularen Heparin – ist daher während der Hospitalisierung indiziert, wenn keine Kontraindikation (z. B. akute Blutung oder erhöhtes Blutungsrisiko) dagegen vorliegt. Über die Intensität der Prophylaxetherapie wird jedoch mangels ausreichender Evidenz noch diskutiert. Bei Hochrisiko-PatientInnen könnte eine intermediäre Dosis statt der sonst üblichen Standard-Prophylaxedosis zu einer Verbesserung des Outcomes führen. Um konkrete Empfehlungen zur Thromboseprophylaxe für PatientInnen mit COVID-19, auch in Abhängigkeit des Erkrankungsschweregrads aussprechen zu können, werden die bald abgeschlossenen randomisiert kontrollierten Studien erwartet.