Update – NSAID für die Praxis
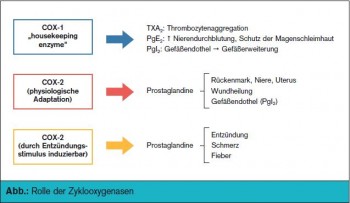
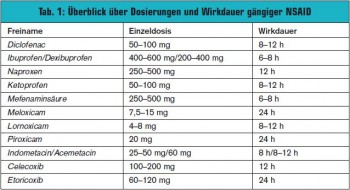
NSAID (Non-steroidal Antiinflammatory Drugs; Synonym: NSAR, nicht-steroidale Antirheumatika) wirken peripher und zentral, wobei ein wesentlicher Anteil der therapeutisch genutzten Effekte und der unerwünschten Wirkungen auf die Hemmung der Cyclooxygenase (COX), die in zwei Isoformen (COX-1 und COX-2) vorliegt, und der daraus resultierenden Hemmung der endogenen Prostaglandinsynthese zurückzuführen sind (> Abb.). Die antiphlogistische Dosis ist typischerweise höher als die analgetische Dosis. Die Kinetik der NSAID zeichnet sich durch gute enterale Resorption, hohe Plasmaeiweißbindung, Akkumulation in saurem Milieu, unterschiedliche Abbauwege, renale und biliäre Elimination aus. Die Halbwertszeiten der einzelnen Substanzen bestimmen meist, ob eine Substanz eher für kurz dauernden oder intermittierend auftretenden Schmerz verwendet wird oder eher für chronische Leiden mit permanentem Schmerz. Allerdings können Retardpräparate eine kurze Halbwertszeit ausgleichen (> Tab. 1).
Neben dem Nebenwirkungs-Symptomenkomplex gastrointestinale Symptome, wie sichtbare Mukosaläsionen und ernsthafte gastrointestinale Komplikationen, rückte das kardiovaskuläre Risiko mit dem schwerwiegendsten Ereignis Myokardinfarkt, insbesondere bei der längerfristigen NSAID-Anwendung, zunehmend ins Zentrum des Interesses.
Mechanismus der NSAID-induzierten gastrointestinalen und kardiovaskulären Nebenwirkungen: Für die gastrointestinalen Nebenwirkungen ist in erster Linie die COX-Hemmung, und hier insbesondere die Hemmung der COX-1, die konstitutiv im Magen exprimiert wird, verantwortlich. Dadurch wird die Bildung von protektiven Faktoren der gastrointestinalen Mukosa im Säuremilieu beeinträchtigt. Hohe lokale Substanzkonzentrationen der NSAID mit Säurecharakter können auch direkt nach Bindung an Zellbestandteile oder Anreicherung in Mukosazellen zu einer Schädigung der gastrointestinalen Mukosa führen. COX-2-Inhibitoren führen demgemäß im Vergleich zu den unselektiven COX-Hemmern zu weniger gastrointestinalen Nebenwirkungen. Der Mechanismus der kardiovaskulären Nebenwirkungen wird dagegen im Überwiegen der COX-2-Hemmung gesehen. Auch bei den meisten nicht-selektiven NSAID wird die plättchenaggregationsfördernde und vasokonstriktorische COX-2-Hemmung nur unvollständig oder nur intermittierend durch die COX-1- Hemmung dieser Substanzen ausbalanciert. Lediglich Naproxen weist durch seine ausgeglichene und über den gesamten Tagesverlauf andauernde COX-1- und COX-2-Hemmung einen kardiovaskulären Vorteil gegenüber den anderen Substanzen auf.
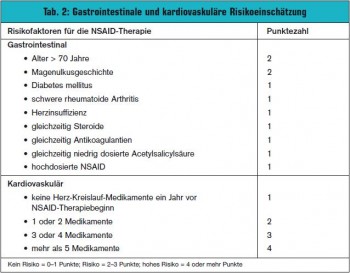
Einschätzung des Risikos vor Beginn der NSAIDTherapie: Idealerweise sollte die Auswahl eines bestimmten NSAID, die Auswahl einer gastroprotektiven Begleitmedikation, bzw. die Auswahl alternativer Therapien schon aufgrund eines vorbestehenden Risikos erfolgen. In eine derartige Auflistung der gastrointestinalen Risikoscores, die bereits in großer Zahl pub – liziert sind, fließen Patientenfaktoren und Medikationsfaktoren mit ein (> Tab. 2).
Bei der kardiovaskulären Risikoeinschätzung kann man sich einerseits an kardiovaskulären Ereignissen im abgelaufenen Jahr orientieren, so z .B. gab es Hospitalisierungen aufgrund von Koronarerkrankung oder Herzinsuffizienz, bzw. liegt eine zerebrovaskuläre oder periphere arterielle Erkrankung oder eine Hypertonie vor. Noch einfacher ist es, man orientiert sich an der bereits bestehenden Medikationsliste (Beispiel in > Tab. 2).
Empfehlungen für verschiedene Risikogruppen: Zur Risikoreduktion gibt es eine Reihe von Maßnahmen. Sie beinhalten je nach Höhe des gastrointestinalen Risikos den Zusatz eines Magenschutzes zu traditionellen bzw. unselektiven NSAID oder die Auswahl eines selektiven COX-2-Inhibitors ohne oder mit Magenschutz. Bei hohem kardiovaskulärem Risiko bietet sich Naproxen an. Sind sowohl gastrointestinales als auch kardiovaskuläres Ri siko sehr hoch, ist auf eine alternative Schmerzmedikation auszuweichen (Paracetamol oder Opioide für die Langzeitgabe, Metamizol für kurzfristige Gaben). Eine Empfehlung ist in > Tab. 3 aufgelistet.
Mehrere Beobachtungsstudien zeigen allerdings, dass die Risikoscores bei der Verordnung von NSAID leider nicht berücksichtigt werden. Es ließ sich kein Unterschied im NSAID-Verordnungsprofil zwischen Patienten ohne und Patienten mit hohem gastrointestinalen und/oder kardiovaskulären Risiko erkennen. Obwohl Patienten mit hohem gastrointestinalen und kardiovaskulären Risiko eigentlich überhaupt kein NSAID oder COX-2-Hemmer erhalten dürften, war dies doch der Fall. Entsprechend dieser Vorgangsweise fand sich auch bei der Erfassung der Epidemiologie oberer gastrointestinaler Blutungen, dass Gastroprotektiva in der NSAID-Therapie viel zu selten genutzt wurden.
Niedrig dosierte Acetylsalicylsäure und Clopidogrel sind gastrointestinale Risikofaktoren (aber verhindern oder reduzieren kardiovaskuläre Ereignisse) und erfordern daher bei der NSAID-Therapie eine gastroprotektive Komedikation. PPI sind Magenschutzpräparate erster Wahl, jedoch gibt es Warnhinweise der europäischen Zulassungsbehörde EMA, dass sie möglicherweise durch Wechselwirkungen mit Clopidogrel belastet sind. Famotidin ist bei Patienten mit NSAID-Therapie genauso gut wirksam wie PPI und hat keine Interaktionen mit Clopidogrel. Möchte man auf die Gabe von Clopidogrel und PPI nicht verzichten, bietet sich aufgrund der nicht zu langen Halbwertszeiten beider Substanzen an, ein 12-h- Intervall einzubauen: Einnahme von PPI vor dem Frühstück und Clopidogrel nach dem Abendessen. Damit vermeidet man weitgehend mögliche pharmakokinetische Wechselwirkungen.
FACT-BOX
Das ideale NSAID gibt es nicht, alle haben
aufgrund ihres Wirkmechanismus Nebenwirkungen.
Gastrointestinale und kardiovaskuläre Risikofaktoren
werden bei der NSAID-Therapie
noch zu wenig berücksichtigt.
Die Auswahl eines bestimmten NSAID,
die Auswahl einer gastroprotektiven Begleitmedikation
bzw. die Auswahl alternativer
Therapien sollte einem vorbestehenden
Risiko entsprechend erfolgen.